Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Sau phản ứng, thu được hỗn hợp kim loại, suy ra kẽm dư.
$n_{CuSO_4} = \dfrac{80.30\%}{160} = 0,15(mol)$
$Zn + CuSO_4 \to ZnSO_4 + Cu$
$n_{Zn\ pư} = n_{CuSO_4} = 0,15(mol)$
$\Rightarrow m_{Zn\ pư} = 0,15.65 = 9,75(gam)$
Sau phản ứng, $m_{dd} = 9,75 + 80 - 0,15.64 = 80,15(gam)$
$C\%_{ZnSO_4} = \dfrac{0,15.161}{80,15}.100\% = 30,13\%$

3. CuO +H2SO4 -->CuSO4 +H2O
nCuO=64/80=0,8(mol)
theo PTHH :nCuO =nH2SO4=nCuSO4=0,8(mol)
=>mddH2SO4 20%=0,8.98.100/20=392(g)
mCuSO4=0,8.160=128(g)
mdd sau phản ứng =64 +392=456(g)
mH2O=456 -128=328(g)
giả sử có a g CuSO4.5H2O tách ra
trong 250g CuSO4 tách ra có 160g CuSO4 và 90g H2O tách ra
=> trong a g CuSO4.5H2O tách ra có : 160a/250 g CuSO4 và 90a/250 g H2O tách ra
=>mCuSO4(còn lại)=128 -160a/250 (g)
mH2O (còn lại)=328 -90a/250 (g)
=>\(\dfrac{128-\dfrac{160a}{250}}{328-\dfrac{90a}{250}}.100=25\)
=>a=83,63(g)

a,\(n_{H_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
PTHH: Zn + 2HCl → ZnCl2 + H2
Mol: x x
PTHH: Fe + 2HCl → FeCl2 + H2
Mol: y y
Ta có: \(\left\{{}\begin{matrix}65x+56y=30,7\\x+y=0,5\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,3\left(mol\right)\\y=0,2\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\%m_{Zn}=\dfrac{0,3.65.100\%}{30,7}=63,52\%;\%m_{Fe}=100\%-63,52\%=36,48\%\)
b,
PTHH: Zn + 2HCl → ZnCl2 + H2
Mol: 0,3 0,6
PTHH: Fe + 2HCl → FeCl2 + H2
Mol: 0,2 0,4
nHCl = 0,6+0,4 = 1 (mol)
\(V_{ddHCl}=\dfrac{1}{2}=0,5\left(l\right)=500\left(ml\right)\)

mCuSO4 = 80.30% = 24 gam ==> nCuSO4 = 0,15 mol
dung dịch có 80-24 = 56 gam H2O
Zn + CuSO4 → ZnSO4 + Cu
Sau phản ứng thu được 16,1 hỗn hợp kim loại nên sau phản ứng phải có Zn dư và CuSO4 phản ứng hết.
nZn phản ứng = nCuSO4 = 0,15 ==> mZn = 0,15.65=9,75 gam
Chất tan trong dung dịch thu được là ZnSO4 = 0,15mol
mZnSO4 = 0,15.161= 24,15 gam
m dung dịch sau phản ứng = mH2O + mZnSO4 = 80,15 gam
C%ZnSO4 = \(\dfrac{24,15}{24,15+56}.100\)= 30,13%
b.
Hỗn hợp kim loại A gồm Zn dư và Cu : 0,15 mol
=> mZn = 16,1 - 0,15.64= 6,5 gam <=> nZn = 0,1 mol
Cho A tác dụng với HCl chỉ có Zn phản ứng
Zn + 2HCl --> ZnCl2 + H2
0,1 --------------> 0,1
==> VH2 = 0,1 .22,4 = 2,24 lít

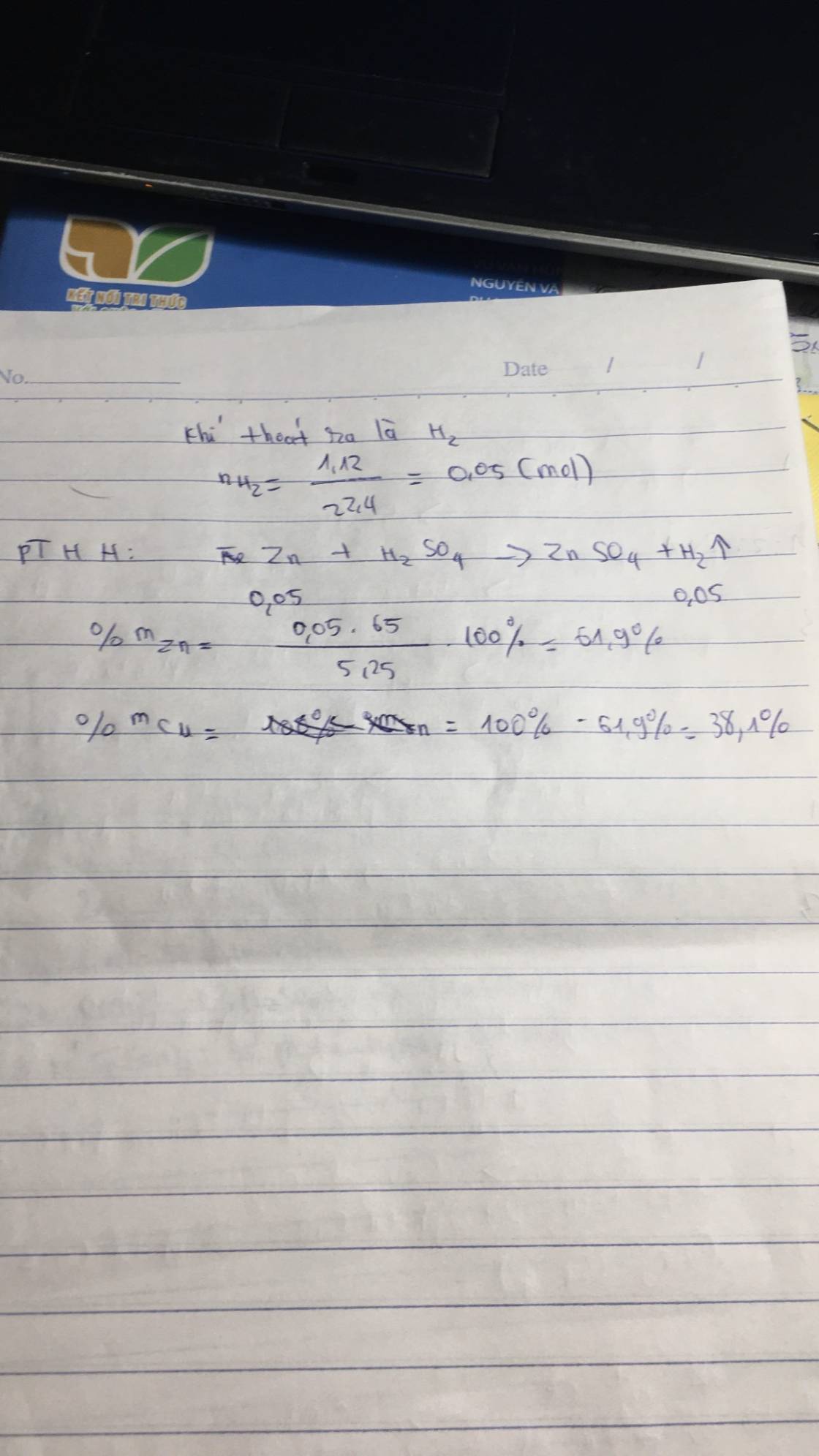



2) Zn (0,025) + CuSO4 (0,025) -----> ZnSO4 (0,025) + Cu (0,025)
- kẽm ko tan được nữa => CuSO4 đã phản ứng hết
mCuSO4 = 4 gam
=> nCuSO4 = 0,025 mol
- Theo PTHH: nZn = 0,025 mol
=> mZn = 1,625 gam
- Các chất sau phản ứng gồm: \(\left\{{}\begin{matrix}Zn_{dư}\\ZnSO_4:0,025\left(mol\right)\\Cu:0,025\left(mol\right)\end{matrix}\right.\)
mZnSO4 = 0,025 . 161 = 4,025 gam
mdd sau = 40 + 0,025.65 = 41,625 gam
=> C% ZnSO4 = 9,6697%
3) Zn + H2SO4 ----> ZnSO4 + H2
nH2 = 0,05 mol
- Theo PTHH: nZn = 0,05 mol
=> mZn = 3,25 gam
=> mCu = 2 gam
=> \(\%mZn=\dfrac{3,25.100\%}{5,25}=61,9\%\)
=> \(\%mCu=100\%-61,9\%=38,1\%\)
- Phần trăm khối lượng mỗi kim loại trong hỗn hợp X ban đầu tương ứng với phần trăm khối lượng mỗi kim loại trong 5,25 gam hỗn hợp X.
Vậy phần trăm khối lượng của kim loại Zn và Cu trong hỗn hợp X ban đầu lần lượt là 61,9% và 38,1%