Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(X\left(Z=20\right):\left[Ar\right]4s^2\rightarrow KL\) ( do có `2e` ở lớp ngoài cùng)
\(Z\left(Z=17\right):\left[Ne\right]3s^23p^5\rightarrow PK\) ( do có `7e` ở lớp ngoài cùng)
Do là một kim loại và một phi kim nên liên kết tạo thành là liên kết ion
\(X\rightarrow X^++e\)
\(Y+e\rightarrow Y^-\)
\(X^++Y^-\rightarrow XY\)

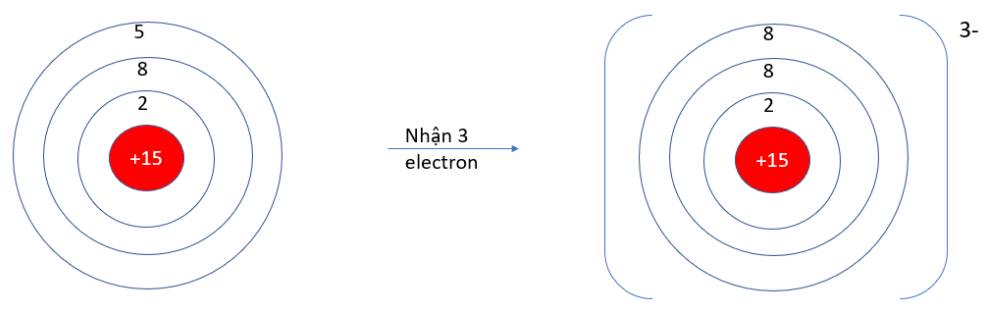
- Cấu hình electron B (Z = 5): 1s22s22p1 => Có 3 electron ở lớp ngoài cùng => Xu hướng nhường đi 3 electron
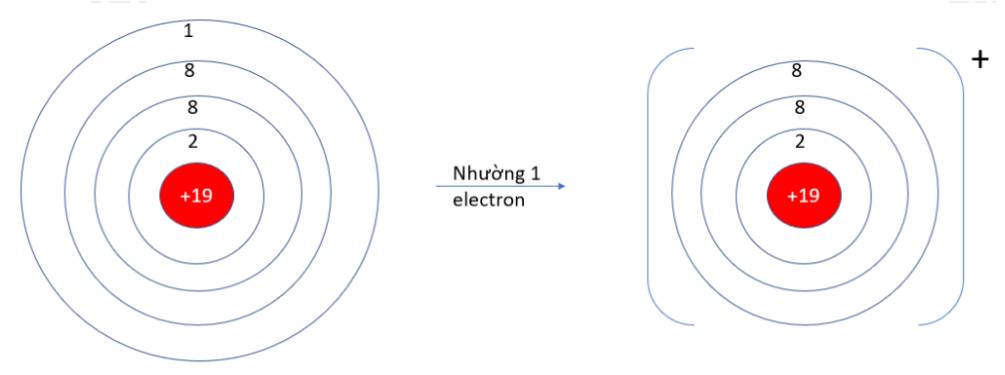
- Cấu hình electron K (Z = 19): 1s22s22p63s23p64s1 => Có 1 electron ở lớp ngoài cùng => Xu hướng nhường đi 1 electron
- Cấu hình electron He (Z = 2): 1s2 => Đạt cấu hình bền vững
- Cấu hình electron F (Z = 9): 1s22s22p5 => Có 7 electron ở lớp ngoài cùng => Xu hướng nhận thêm 1 electron
=> Nguyên tử nguyên tố Potassium (K, Z = 19) có xu hướng nhường đi 1 electron khi hình thành liên kết hóa học
Đáp án B

a)
- K (Z = 19): 1s22s22p63s23p64s1 => Có 1 electron ở lớp vỏ ngoài cùng => Xu hướng nhường 1 electron
- O (Z = 8): 1s22s22p4 => Có 6 electron ở lớp vỏ ngoài cùng => Xu hướng nhận 2 electron

b)
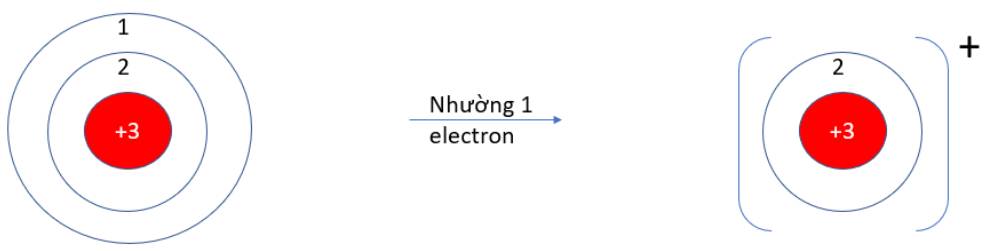
- Li (Z = 3): 1s22s1 => Có 1 electron ở lớp vỏ ngoài cùng => Xu hướng nhường 1 electron
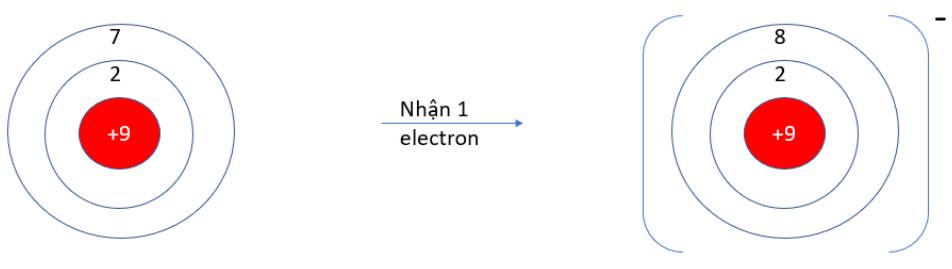
- F (Z = 9): 1s22s22p5 => Có 7 electron ở lớp vỏ ngoài cùng => Xu hướng nhận 1 electron
c)
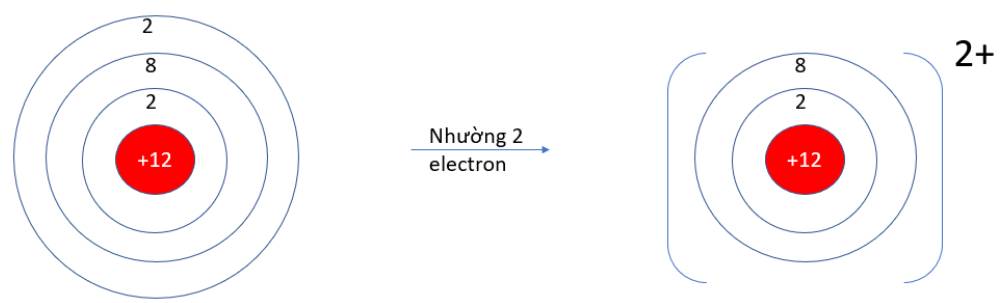
- Mg (Z = 12): 1s22s22p63s2 => Có 2 electron ở lớp vỏ ngoài cùng => Xu hướng nhường 2 electron
- P (Z = 15): 1s22s22p63s23p3 => Có 5 electron ở lớp vỏ ngoài cùng => Xu hướng nhận 3 electron

Tính chất hóa học cơ bản của clo: Clo là chất oxi hóa mạnh.
- Tác dụng với kim loại : clo oxi hóa trực tiếp hầu hết các kim loại tạo muối clorua, phản ứng xảy ra ở nhiệt độ thường hoặc không cao lắm, tốc độ nhanh, tỏa nhiều nhiệt.
2Fe + 3Cl2  2FeCl3
2FeCl3
- Tác dụng với hiđro: Phản ứng xảy ra khi chiếu sáng bởi ánh sáng mặt trời:
H2 + Cl2 → 2HCl.
- Tác dụng với nước:
Trong phản ứng với nước, clo vừa là chất oxi hóa vừa là chất khử.
Cl2 + H2O ⇆ HCl + HClO
Sở dĩ có những tính chất hóa học cơ bản trên vì khi tham gia phản ứng, nguyên tử clo dễ nhận thêm 1 electron để thành ion Cl-. Vì vậy tính chất hóa học cơ bản của clo là tính oxi hóa mạnh.

Nguyên tử Li có 3 proton mang điện tích dương và 3 electron mang điện tích âm. Khi mất một electron thì ion có dư một điện tích dương nên ion được hình thành mang một điện tích dương (1+).
Ion mang điện tích dương nên thuộc loại ion dương hay cation
Ion của nguyên tố liti thì được gọi là ion liti (tên nguyên tố).
Phương trình : Li → Li + + e

Nguyên tử F có 9 proton mang điện tích dương và 9 electron mang điện tích âm. Khi nhận thêm một electron thì ion có dư một điện tích âm nên ion được hình thành mang một điện tích âm (1-).
Ion mang điện tích âm nên thuộc loại ion âm hay anion.
Ion của flo được gọi là ion florua.
Phương trình: F + e → F -
- Nguyên tử oxygen có Z = 8 => Oxygen có 8 electron
=> Cấu hình electron: 1s22s22p4
=> Oxygen có 6 electron ở lớp vỏ ngoài cùng
=> Xu hướng cơ bản của nguyên tử oxygen khi hình thành liên kết hóa học là nhận thêm 2 electron để đạt được lớp vỏ có 8 electron ở lớp vỏ ngoài cùng
- Sơ đồ nguyên tử O nhận 2 electron vào lớp vỏ ngoài cùng