Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a)PTHH:2KClO3KClO3------->2KCl+3 O2O2(1)[/SIZE][/FONT][/I][/B]
3 Fe+2O2O2------>Fe3O4Fe3O4(2)[/SIZE][/FONT][/I][/B]
b)nKClO3KClO3=m:M=49:122,5=0.4mol
ta có PTHH (1):2KClO3KClO3------->2KCl+3 O2O2
Theo PTHH : 2 mol 3 mol
Theo bài ra : 0,4 mol -------> 0,6 mol
Vậy lượng O2O2 thu được là 0,6 mol
Ta có Phương trình hoá học (2):3Fe+2O2O2------>Fe3O4Fe3O4
Theo phương trình hoá học: 2 mol 1 mol
Theo đề bài ta có : 0,6 ---> 0,3 mol
Vậy lượng Fe3O4Fe3O4 : 0,3.232=69,6g

a) Phương trình hóa học của phản ứng:
3Fe + 2O2 → Fe3O4.
nFe3O4 = 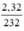 = 0,01 mol.
= 0,01 mol.
nFe = 3.nFe3O4 = 0,01 .3 = 0,03 mol.
nO2 = 2.nFe3O4 = 0,01 .2 = 0,02 mol.
mFe = 0,03.56 = 1,68g.
mO2 = 0,02.32 = 0,64g.
b) Phương trình phản ứng nhiệt phân KMnO4:
2KMnO4 → K2MnO4 + MnO2 + O2
nKMnO4 = 2.nO2 = 0,02.2 = 0,04 mol.
mKMnO4 = 0,04 .158 = 6,32g.

a. \(n_{Fe_3O_4}=\dfrac{6,96}{232}=0,03\left(mol\right)\)
PTHH : 3Fe + 2O2 -to-> Fe3O4
0,09 0,06 0,03
\(m_{Fe}=0,09.56=5,04\left(g\right)\)
\(V_{O_2}=0,06.22,4=1,344\left(l\right)\)
b. PTHH : 2KCl + 3O2 -> 2KClO3
0,06 0,04
\(m_{KClO_3}=0,04.122,5=4,9\left(g\right)\)

a)PTHH:KClO3------->2KCl+3 O2
3 Fe+2O2------>Fe3O4(2)
b)nKClO3=m:M=49:122,5=0.4mol
ta có PTHH (1):2KClO------->2KCl+3 O2O2
Theo PTHH : 2 mol 3 mol
Theo bài ra : 0,4 mol -------> 0,6 mol
Vậy lượng O2 thu được là 0,6 mol
Ta có Phương trình hoá học (2):3Fe+2O2----->Fe3O4
Theo phương trình hoá học: 2 mol 1 mol
Theo đề bài ta có : 0,6 ---> 0,3 mol
Vậy lượng Fe3O4 : 0,3.232=69,6g

a) \(n_{Fe}=\dfrac{3,36}{56}=0,06\left(mol\right)\)
PTHH: 3Fe + 2O2 --to--> Fe3O4
0,06->0,04------->0,02
=> mFe3O4 = 0,02.232 = 4,64 (g)
b) VO2 = 0,04.22,4 = 0,896 (l)

a, \(n_{Fe_3O_4}=\dfrac{23,2}{232}=0,1\left(mol\right)\)
PT: \(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
Theo PT: \(n_{Fe}=3n_{Fe_3O_4}=0,3\left(mol\right)\Rightarrow m_{Fe}=0,3.56=16,8\left(g\right)\)
b, \(n_{O_2}=2n_{Fe_3O_4}=0,2\left(mol\right)\Rightarrow V_{O_2}=0,2.22,4=4,48\left(l\right)\)
\(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
0,3 0,2 0,1
\(n_{Fe_3O_4}=\dfrac{23,2}{232}=0,1\left(mol\right)\)
\(a,m_{Fe}=0,3.56=16,8\left(g\right)\)
\(b,V_{O_2}=0,2.22,4=4,48\left(l\right)\)

n Fe3O4=\(\dfrac{4,64}{232}=0,02mol\)
3Fe+2O2-to>Fe3O4
0,06----0,04---0,02
=>m O2=0,04.32=1,28g
\(n_{Fe_3O_4}=\dfrac{m}{M}=\dfrac{4,64}{232}=0,02mol\)
\(3Fe+2O_2\rightarrow\left(t^o\right)Fe_3O_4\)
0,06 0,02 ( mol )
\(m_{Fe}=n_{Fe}.M_{Fe}=0,06.56=3,36g\)

a.\(\%Fe=\dfrac{56.3}{56.3+16.4}.100=72,41\%\)
b.\(n_{Fe_3O_4}=\dfrac{4,64}{232}=0,02mol\)
\(3Fe+2O_2\rightarrow\left(t^o\right)Fe_3O_4\)
0,04 0,02 ( mol )
\(m_{O_2}=0,04.32=1,28g\)
c.\(2KMnO_4\rightarrow\left(t^o\right)K_2MnO_4+MnO_2+O_2\)
0,08 0,04 ( mol )
\(m_{KMnO_4}=0,08.158=12,64g\)

\(n_{Fe_3O_4}=\dfrac{4,64}{232}=0,02\left(mol\right)\)
3Fe + 2O2 \(\underrightarrow{t^o}\) Fe3O4
0,04 0,02 ( mol )
\(m_{O_2}=0,04.32=1,28\left(g\right)\)
=> Đáp án A
Khi đốt cháy sắt trong oxi ở nhiệt độ cao, thu được oxit sắt từ. Để điều chế 4,64 gam oxit sắt từ thì khối lượng oxi đem dùng là *
1,28 gam.
3,24 gam.
4,56 gam.
2,25 gam.
ui da lỗi rồi
sai rồi bạn ơi, copy thì đungè có trách