Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Ta có:
\(n_{Fe} = \dfrac{5,6}{56} = 0,1(mol)\\ n_{FeS_2} = \dfrac{12}{120} = 0,1(mol)\)
Gọi \(n_{SO_2} = a(mol) \to n_{NO_2} = 2a(mol)\)
Quá trình oxi hóa khử :
\(Fe^0 \to Fe^{+3} + 3e\\ FeS_2 \to Fe^{+3} + 2S^{+6} + 15e\\ S^{+6} + 2e \to S^{+4}\\ N^{+5} + 1e \to N^{+4}\)
Bảo toàn electron : 3nFe + \(15n_{FeS_2}\) = \(2n_{SO_2} + n_{NO_2}\)
⇒ 0,1.3 + 0,1.15 = 2.a + 2a
⇒ a = 0,45(mol)
Suy ra : V = (0,45 + 0,45.2).22,4 = 30,24(lít)

Đáp án C
![]()
Vì ![]() nên chỉ có hai trường hợp là SO2 thiếu hoặc phản ứng tạo hai muối. Đề bài yêu cầu tìm giá trị lớn nhất của m nên khi cho SO2 vào dung dịch X sẽ tạo hai muối
H
S
O
-
3
và
S
O
2
-
3
nên chỉ có hai trường hợp là SO2 thiếu hoặc phản ứng tạo hai muối. Đề bài yêu cầu tìm giá trị lớn nhất của m nên khi cho SO2 vào dung dịch X sẽ tạo hai muối
H
S
O
-
3
và
S
O
2
-
3
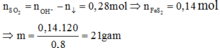
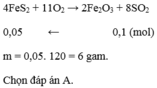

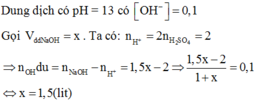
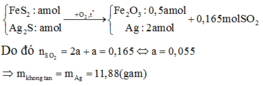
`4FeS_2+11O_2-> 2Fe_2O_3+8SO_2`(to)
`1,44--3,96mol`
`->m_(FeS_2)=1,44.120=172,8g`