Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

1 , \(n_{Na}=\frac{4,6}{23}=0,2\left(mol\right)\)
\(m_{HCl}=200.2,92\%=5,84\left(mol\right)\) => \(n_{HCl}=\frac{5,84}{36,5}=0,16\left(mol\right)\)
\(2Na+2HCl->2NaCl+H_2\left(1\right)\)
vì \(\frac{0,2}{2}>\frac{0,16}{2}\) => Na dư , HCl hết
dung dịch thu được là dung dịch NaCl
theo (1) \(n_{NaCl}=n_{HCl}=0,16\left(mol\right)\) => \(m_{NaCl}=0,16.58,5=9,36\left(g\right)\)
\(n_{H_2}=\frac{1}{2}n_{HCl}=0,08\left(mol\right)\)
khối lượng dung dịch sau phản ứng là
4,6+200-0,08.2=204,44(g)
\(C_{\%\left(NaCl\right)}=\frac{9,36}{204,44}.100\%\approx4,58\%\)

Ta có: \(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
a. PTHH: \(Zn+H_2SO_4--->ZnSO_4+H_2\uparrow\left(1\right)\)
b. Theo PT(1): \(n_{Zn}=n_{H_2}=0,3\left(mol\right)\)
\(\Rightarrow m_{Zn}=65.0,3=19,5\left(g\right)\)
c. Theo PT(1): \(n_{H_2SO_4}=n_{Zn}=0,3\left(mol\right)\)
Đổi 300ml = 0,3 lít
\(\Rightarrow C_{M_{H_2SO_4}}=\dfrac{0,3}{0,3}=1M\)
d. PTHH: \(2NaOH+H_2SO_4--->Na_2SO_4+2H_2O\left(2\right)\)
Theo PT(2): \(n_{NaOH}=2.n_{H_2SO_4}=2.0,3=0,6\left(mol\right)\)
\(\Rightarrow m_{NaOH}=0,6.40=24\left(g\right)\)
\(\Rightarrow m_{dd_{NaOH}}=\dfrac{24.100\%}{20\%}=120\left(g\right)\)

a) Gọi hóa trị của kim loại cần tìm là n
A-----> A+n + ne
S+6 +2e -----> S+4
Áp dụng bảo toàn e : \(n_A=\dfrac{n_{SO_2}.2}{n}=\dfrac{0,6}{n}\)
Ta có: \(\dfrac{19,2}{A}=\dfrac{0,6}{n}\)
Chạy nghiệm theo n:
n=1 --------> A=32 (lọai)
n=2 -------> A=64 ( chọn - Cu)
n=3 ------->A=96 (loại)
Vậy kim loại A là Đồng (Cu)
b) Giả sử phản ứng tạo 2 muối
Gọi x, y lần lượt là số mol KHSO3 và K2SO3
=> \(\left\{{}\begin{matrix}x+y=0,3\\120x+158t=39,8\end{matrix}\right.\)
=> x=0,2, y=0,1 (thỏa mãn)
=> \(n_{KOH}=0,2+0,1.2=0,4\left(mol\right)\)
=> \(CM_{KOH}=\dfrac{0,4}{0,4}=1M\)

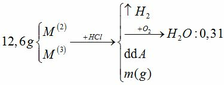
Đồng nhất dữ kiện để thuận lợi cho tính toán, bằng cách nhân đôi khối lượng H2O.
a.
BTNT H: nH2 = nH2O = 0,31 mol
=> nHCl = 0,62mol
BTKL: m kim loại + mHCl = mA + mB => 12,6 + 36,5 . 0,62 = m + 2 . 0,31 => m = 34,61g
b.
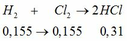
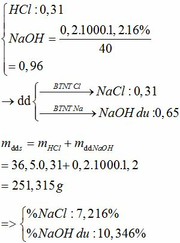

Bài 1:
\(2Na+2H_2O\rightarrow2NaOH+H_2\\ n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\\ n_{Na}=n_{Na_2O}=0,2.2=0,4\left(mol\right)\\ a.m_{Na}=0,4.23=9,2\left(g\right)\\ b.C_{MddA}=\dfrac{0,4}{0,5}=0,8\left(M\right)\\ C\%_{ddA}=\dfrac{0,4.40}{500.1,2}.100\approx2,667\%\)

PT: \(2Al+3Cl_2\underrightarrow{t^o}2AlCl_3\)
\(AlCl_3+3AgNO_3\rightarrow Al\left(NO_3\right)_3+3AgCl\)
Ta có: \(n_{AgNO_3}=0,1.0,6=0,06\left(mol\right)\)
Theo PT: \(n_{Al}=n_{AlCl_3}=\dfrac{1}{3}n_{AgNO_3}=0,02\left(mol\right)\)
⇒ m = mAl = 0,02.27 = 0,54 (g)
\(C_{M_{AlCl_3}}=\dfrac{0,02}{0,15}=\dfrac{2}{15}\left(M\right)\)
\(BTNT\left(S\right):n_{SO3}=n_{SO2}=\dfrac{V}{22,4}=\dfrac{5}{14}\left(mol\right)\)
Ta có : \(n_{H2SO4}=\dfrac{9}{25}\left(mol\right)\)
\(\Rightarrow\Sigma n_{H2SO4}=\dfrac{5}{14}+\dfrac{9}{25}=\dfrac{251}{350}\left(mol\right)\)
\(\Rightarrow C\%=\dfrac{m_{H2SO4}}{m_{dd}}.100\%=64,7\%\)
Sai r ak