Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

nKMnO4 = 9,48/158 = 0,06 (mol)
PTHH: 2KMnO4 -> (t°) K2MnO4 + MnO2 + O2 (p/ư phân hủy)
nO2 = 0,06/2 = 0,03 (mol)
nFe = 11,2/56 = 0,2 (mol)
PTHH: 3Fe + 2O2 -> (t°) Fe3O4
LTL: 0,2/3 > 0,03/4 => Fe dư
nFe3O4 = 0,03 : 2 = 0,015 (mol)
mFe3O4 = 0,015 . 232 = 3,48 (g)

a. \(n_{KClO_3}=\dfrac{24,5}{122,5}=0,2\left(mol\right)\)
PTHH : 2KClO3 -to> 2KCl + 3O2
0,2 0,3
\(V_{O_2}=0,3.22,4=6,72\left(l\right)\)
b.\(n_{O_2}=0,3\left(mol\right)\left[cmt\right]\)
\(m_{O_2}=0,3.32=9,6\left(g\right)\)
PTHH : 3Fe + 2O2 -to> Fe3O4
Theo ĐLBTKL
\(m_{Fe}+m_{O_2}=m_{Fe_3O_4}\\ \Rightarrow11,2+9,6=20,8\left(g\right)\)
a: \(2KClO_3\rightarrow2KCl+3O_2\)
\(n_{KClO_3}=\dfrac{24.5}{122.5}=0.2\left(mol\right)\)
\(\Leftrightarrow n_{O_2}=\dfrac{3}{2}\cdot0.2=0.3\left(mol\right)\)
\(V_{O_2}=0.3\cdot22.4=6.72\left(lít\right)\)
b: \(4Fe+3O_2\rightarrow2Fe_2O_3\)
\(n_{Fe}=\dfrac{11.2}{56}=0.2\left(mol\right)\)
\(\dfrac{n_{Fe}}{4}=\dfrac{0.2}{4}=0.05< \dfrac{n_{O_2}}{3}\) nên O2 dư
=>Tính theo Fe
\(n_{Fe_2O_3}=0.1\left(mol\right)\)
\(m_{Fe_2O_3}=0.1\cdot160=16\left(g\right)\)

a) 2KClO3--->2KCl+3O2
b) n KClO3=24,5/122,5=0,2(mol)
Theo pthh
n O2=3/2n KClO3=0,3(mol)
V O2 (đktc)=0,3.22,4=6,72(l)
c) 4P+5O2--->2P2O5
n P=4/5 n O2=0,24(mol)
m P=0,24.31=7,44(g)
n P2O5=2/5n O2=0,12(mol)
m P2O5=0,12.142=17,04(g)

a)
\(4P + 5O_2 \xrightarrow{t^o} 2P_2O_5\)
Sản phẩm : Điphotpho pentaoxit.
b)
\(n_P = \dfrac{6,2}{31} = 0,2(mol)\\ \Rightarrow n_{P_2O_5} = \dfrac{1}{2}n_P = 0,1(mol)\\ \Rightarrow m_{P_2O_5} = 0,1.142 = 14,2(gam)\)
c)
\(n_{O_2} = \dfrac{5}{4}n_P = 0,125(mol)\\ \Rightarrow V_{O_2} = 0,125.22,4 = 2,8(lít)\)
d)
\(V_{không\ khí} = \dfrac{2,8}{20\%} = 14(lít)\)

a.\(n_{KMnO_4}=\dfrac{m}{M}=\dfrac{31,6}{158}=0,2mol\)
\(PTHH:2KMnO_4\underrightarrow{np}K_2MnO_4+MnO_2+O_2\)
2 1 1 1 ( mol )
0,2 0,1
\(V_{O_2}=n.22,4=0,1.22,4=2,24l\)
b.\(n_{Fe}=\dfrac{m}{M}=\dfrac{11,2}{56}=0,2mol\)
\(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
3 2 1 ( mol )
0,2 0,1
0,1 0,1 0,05 ( mol )
\(m_{Fe_3O_4}=n.M=0,05.232=11,6g\)

a)\(n_{Fe}=\dfrac{22,4}{56}=0,4mol\)
\(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
0,4 \(\dfrac{4}{15}\) \(\dfrac{2}{15}\)
\(V_{O_2}=\dfrac{4}{15}\cdot22,4=5,973l\)
b)\(2KClO_3\underrightarrow{t^o}2KCl+3O_2\)
\(\dfrac{8}{45}\) \(\dfrac{4}{15}\)
\(m_{KClO_3}=\dfrac{8}{45}\cdot122,5=21,78g\)

a, nZn = 13/65 = 0,2 (mol)
PTHH: 2Zn + O2 -> (t°) 2ZnO
Mol: 0,2 ---> 0,1 ---> 0,2
b, VO2 = 0,1 . 22,4 = 2,24 (l)
c, mZnO = 0,2 . 81 = 16,2 (g)
d, PTHH: 2KMnO4 -> (t°) K2MnO4 + MnO2 + O2
nKMnO4 = 0,1 . 2 = 0,2 (mol)
mKMnO4 = 0,2 . 158 = 31,6 (g)

a)PTHH:2KClO\(_3\)➞\(^{t^o}\)2KCl+3O\(_2\)
b) n\(_{KClO_3}\)=\(\dfrac{m_{KClO_3}}{M_{KClO_3}}\)=\(\dfrac{12,15}{122,5}\)\(\approx\)0,1(m)
PTHH : 2KClO\(_3\) ➞\(^{t^o}\) 2KCl + 3O\(_2\)
tỉ lệ : 2 2 3
số mol : 0,1 0,1 0,15
V\(_{O_2}\)=n\(_{O_2}\).22,4=0,15.22,4=3,36(l)
c)PTHH : 2Zn + O\(_2\) -> 2ZnO
tỉ lệ : 2 1 2
số mol :0,3 0,15 0,3
m\(_{Zn}\)=n\(_{Zn}\).M\(_{Zn}\)=0,3.65=19,5(g)

a.b.
\(n_{Fe}=\dfrac{16,8}{56}=0,3mol\)
\(3Fe+2O_2\rightarrow\left(t^o\right)Fe_3O_4\)
0,3 0,2 0,1 ( mol )
\(m_{Fe_3O_4}=0,1.232=23,2g\)
\(V_{O_2}=0,2.22,4=4,48l\)
\(V_{kk}=4,48.5=22,4l\)
c.
\(2KMnO_4\rightarrow\left(t^o\right)K_2MnO_4+MnO_2+O_2\)
0,4 0,2 ( mol )
\(m_{KMnO_4}=\dfrac{0,4.158}{\left(100-20\right)\%}=79g\)
a/ Số mol Fe là : nFe = 16,8: 56 = 0,3 mol
PTPƯ:
3Fe + 2O2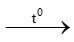 Fe3O4 (1)
Fe3O4 (1)
0,3 mol → 0,2mol → 0,1 mol
Từ (1) ta có số mol Fe3O4 = 0,1mol
→ m Fe3O4 = n.M = 0,1.232 = 23,2gam
b/ Từ (1) ta có số mol O2 đã dùng nO2 = 0,2 mol
Thể tích khí oxi đã dùng ở đktc: VO2 = n.22,4 = 0,2.22,4 = 4,48 lít
Thể tích không khí đã dùng: Vkk = 5. VO2= 5.4,48 = 22,4 lít.
c/ PTPƯ
2 KMnO4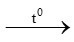 K2MnO4 + MnO2 + O2 (2)
K2MnO4 + MnO2 + O2 (2)
0,4444mol ← 0,222mol
Vì lượng Oxi thu được hao hụt 10% nên số mol O2 cần có là:
nO2 = 0,2mol.100/90 = 0.222 mol
Từ (2) ta có số mol KMnO4 = 0,444mol
Khối lượng KMnO4 bị nhiệt phân
mKMnO4 = n.M = 0,444.158 = 70.152 gam
\(n_{KClO_3}=\dfrac{24,5}{122,5}=0,2mol\)
a)\(2KClO_3\underrightarrow{t^o}2KCl+3O_2\)
0,2 0,3
b)\(V_{O_2}=0,3\cdot22,4=6,72l\)
c)Bảo toàn khối lượng:
\(m_{Fe}+m_{O_2}=m_{sp}\)
\(\Rightarrow m_{sp}=11,2+0,3\cdot32=20,8g\)