Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Bài 1:
A + Cl2 → ACl2 (1)
Fe + ACl2 → FeCl2 + A (2)
x x x (mol)
gọi số mol của Fe phản ứng với một số mol của ACl2 là x
khối lương thanh sắt sau phản ứng là:11,2 - 56x + xMA = 12
=> x =
Ta có:
= 0,25.0,4 = 0,1 (mol)
=> MA = 64 g/mol; Vậy kim loại A là Cu
= nCu =
= 0,2 (mol) =>
= 0,5M
bài 2:
(C17H35COO)3C3H5 + 3NaOH -> 3 C17H35COONa + C3H5(OH)3
890 kg 918 kg
x kg 720 kg
=> x = 698,04 kg.

Đáp án D
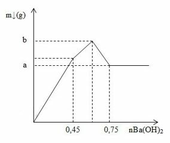
GĐ 1: Kết tủa tăng mạnh nhất do vừa tạo thành BaSO4 và Al(OH)3
GĐ 2: Kết tủa BaSO4 đạt cực đại nên lượng kết tủa tăng chậm đi
GĐ 3: Al(OH)3 bắt đầu bị hòa tan nên lượng kết tủa giảm
nAl2(SO4)3 = x
nAlCl3 = y
+ Tại nBa(OH)2 = 0,45 mol thì BaSO4 đạt cực đại
nSO42- = nBa(OH)2 => 3x = 0,45
=> x = 0,15
+ Tại nBa(OH)2 = 0,75 mol thì Al(OH)3 vừa bị hòa tan hết
nOH- = 4nAl3+ => 0,75.2 = 4.(2.0,15 + y)
=> y = 0,075 mol
a = mBaSO4 max = 0,45.233 = 104,85 gam
b = mBaSO4 max + mAl(OH)3 max = 104,85 + 78(2.0,15 + 0,075) = 134,1 gam
=> a + b = 104,85 + 134,1 = 238,95 gam

Giải thích:
GĐ 1: Kết tủa tăng mạnh nhất do vừa tạo thành BaSO4 và Al(OH)3
GĐ 2: Kết tủa BaSO4 đạt cực đại nên lượng kết tủa tăng chậm đi
GĐ 3: Al(OH)3 bắt đầu bị hòa tan nên lượng kết tủa giảm
nAl2(SO4)3 = x
nAlCl3 = y
+ Tại nBa(OH)2 = 0,45 mol thì BaSO4 đạt cực đại
nSO42- = nBa(OH)2 => 3x = 0,45 => x = 0,15
+ Tại nBa(OH)2 = 0,75 mol thì Al(OH)3 vừa bị hòa tan hết
nOH- = 4nAl3+ => 0,75.2 = 4.(2.0,15 + y) => y = 0,075 mol
a = mBaSO4 max = 0,45.233 = 104,85 gam
b = mBaSO4 max + mAl(OH)3 max = 104,85 + 78(2.0,15 + 0,075) = 134,1 gam
=> a + b = 104,85 + 134,1 = 238,95 gam
Đáp án D

nOH- = 0,04 mol
Vì nAlO2- = 0,02 mol mà chỉ thu được 0,01 mol kết tủa nên nHCl = 4n kết tủa + nAlO2- dư = 0,05 mol
=> tổng nH+ = 0,09 mol => V = 45ml
Vậy : B đúng
H+ + OH- => H2O 1
0,02......0,02
H+ + AlO2 - + H2O => Al(OH)3 2
0,02.....0,02.........................0,02
3H+ + Al(OH)3 => Al3+ +3H2O 3
0,03.........0,01
do cần V lớn nhất nên xét TH tạo kết tủa xong hòa tan 1 phần kết tủa
n Al(OH)3 =0,01 => nAl(OH)3 ở 3 =0,01
=> nHCl= 0,03 +0,02 +0,02 =0,07 => V=0,035 => C

Đáp án B
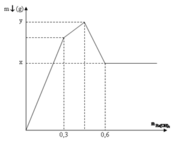
Tại điểm 0,6 mol Ba(OH)2: Al(OH)3 tan hết
![]()
Tại điểm H kết tủa Al(OH)3 đạt cực đại nên ![]()
Tại điểm 0,3 mol Ba(OH)2 thì n S O 4 2 - hết nên n S O 4 2 - = 0,3 mol
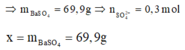
![]()
= 93,3 g
x+ y = 163,2 g

Đáp án B
Nhận thấy tại thời điểm 0,3 mol thì Ba(OH)2 kết tủa vừa đủ với Al2(SO4)3
Khi đó kết tủa gồm BaSO4 : 0,3 mol và Al(OH)3 : 0,2 mol
→ nAl2SO4 = 0,3 : 3= 0,1 mol
Tại thời điểm 0,6 mol Ba(OH)2 thì kết tủa chỉ còn BaSO4 : 0,1 mol, toàn bộ lượng Al(OH)3 bị hòa tan hết → x = 0,3. 233= 69,9 gam
→ 4∑nAl3+ = nOH- = 0,6.2 = 1,2 → ∑nAl3+ = 0,3 mol
Vậy kết tủa cực đại gồm BaSO4 : 0,3 mol và Al(OH)3 : 0,3 mol
→ y = 0,3. 233+ 0,3. 78= 93,3 gam
→ x+ y = 69,9 + 93,3 = 163,2 gam

Đáp án B
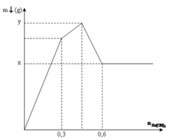
Tại điểm 0,6 mol Ba(OH)2: Al(OH)3 tan hết
![]()
Tại điểm H kết tủa Al(OH)3 đạt cực đại nên
![]()
Tại điểm 0,3 mol Ba(OH)2 thì S O 4 2 - hết nên n S O 4 2 - = 0 , 3 m o l
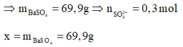
![]()
= 69,9 + 78.0,3 = 93,3 g
x+ y = 163,2 g

Đáp án A
Ta thấy đồ thị được hình thành bởi 3 đường: (1) là kết tủa tạo thành khí Al2(SO4)3 phản ứng với Ba(OH)2 ; (2) là kết tủa tạo thành khi AlCl3 phản ứng với Ba(OH)2 ; (3) là kết tủa Al(OH)3 sinh ra bị hòa tan hết.


Quy đổi hỗn hợp thành RCOOH
nRCOOH= 2nH2=0,5 mol => nOtrong axit=2nRCOOH=1 mol
m axit=mC+mH+mO=> mC=29,6-2.14,4/18-1.16=12 g => nCO2=nC=1 mol
CO2 + Ba(OH)2---> BaCO3+ H2O
nBa(OH)2=0,7 mol < nCO2 => Ba(OH)2 hết và CO2 dư
=> m Kết tủa = 0,7*(MBaCO3)=137,9 gam.
nCOOH= nNaHCO3=nCO2=0,5 mol => nOtrong axit=2nCOOH=1 mol
m axit=mC+mH+mO=> mC=29,6-2.14,4/18-1.16=12 g => nCO2=nC=1 => mCO2=44
 với các chất sau:
với các chất sau: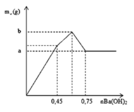


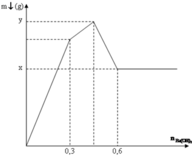
Đáp án cần chọn là: D