Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) nCu=0,2(mol)
PTHH: CuO + H2 -to-> Cu + H2O
b) nH2=nCuO=nCu=0,2(mol)
=>V(H2,đktc)=0,2.22,4=4,48(l)
c) mCuO=0,2.80=16(g)

\(HgO\left(0,1\right)+H_2\left(0,1\right)\rightarrow Hg\left(0,1\right)+H_2O\)
Ta có: \(n_{HgO}=\dfrac{21,7}{217}=0,1\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}m_{Hg}=0,1.201=20,1\left(g\right)\\m_{H_2}=0,1.2=0,2\left(g\right)\end{matrix}\right.\)
a. Số mol thủy ngân (II) oxit là: n = =
= 0,1 (mol)
phương trình phản ứng:
HgO + H2 → H2O + Hg
1 mol 1 mol 1mol 1 mol
0,1 0,1 0,1 0,1
Khối lượng thủy ngân thu được: m = 0,1.201 = 20,1 (g)
b. Số mol khí hi đro: n = 0,1 mol
Thể tích khí hiđro cần dùng ở đktc là:
V = 22,4.0,1 = 2,24 (lít)

n hh khí = 0.5 mol
nCO: x mol
nCO2: y mol
=> x + y = 0.5
28x + 44y = 17.2 g
=> x = 0.3 mol
y = 0.2 mol
Khối lượng oxi tham gia pứ oxh khử oxit KL: 0.2 * 16 = 3.2g => m KL = 11.6 - 3.2 = 8.4g
TH: KL hóa trị I => nKL = 2*nH2 = 0.3 mol => KL: 28!!
KL hóa trị III => nKL = 2/3 *nH2 = 0.1 mol => KL: 84!!
KL hóa trị II => nKL = nH2 = 0.15 mol => KL: 56 => Fe.
nFe / Oxit = 0.15 mol
nO/Oxit = 0.2 mol
=> nFe/nO = 3/4 => Fe3O4
Fe3O4 + 4CO = 3Fe + 4CO2
Fe + H2SO4 = FeSO4 + H2
0.15.....0.15.......0.15.....0.15
=> mH2SO4 pứ = 14.7 g => mdd = 147 g
m dd sau khi cho KL vào = m KL + m dd - mH2 thoát ra = 0.15 * 56 + 147 - 0.15*2 = 155.1g
=> C% FeSO4 = 14.7%

Câu 1: PTHH: Fe2O3 + 3CO ===>Fe + 3CO2
Áp dụng định luật bảo toàn khối lượng
=> mFe = mFe2O3 + mCO - mCO2
= 32 + 16,8 - 26,4 = 22,4 kg
Câu 2/
a/ PTHH: CuCO3 ==( nhiệt)==> CuO + CO2
Cu(OH)2 ==(nhiệt)==> CuO + H2O
Áp dụng định luật bảo toàn khối lượng
=> mCO2 = mmalachite - mCuO - mH2O
= 2,22 - 1,60 - 0,18 = 0,44 gam
b/ Áp dụng định luật bảo toàn khối lượng
=> mquặng = mCuO + mCO2 + mH2O
= 6 + 0,9 + 2,2 = 9,1 gam

Bài 1:
Gọi CTTQ: AO, BO
........x là số mol của hai oxit
nHCl = \(\dfrac{14,6}{36,5}=0,4\) mol
Pt: AO + 2HCl --> ACl2 + H2O
.......x..........2x
.....BO + 2HCl --> BCl2 + H2O
......x..........2x
Ta có hệ pt: \(\left\{{}\begin{matrix}x\left(M_A+16\right)+x\left(M_B+16\right)=9,6\left(1\right)\\2x+2x=0,4\left(2\right)\end{matrix}\right.\)
Từ (2) giải ra x = 0,1
Thế x = 0,1 vào (1), ta được:
\(0,1\left(M_A+16\right)+0,1\left(M_B+16\right)=9,6\)
\(\Leftrightarrow0,1M_A+1,6+0,1M_B+1,6=9,6\)
\(\Leftrightarrow0,1M_A+0,1M_B=9,6-1,6-1,6=6,4\)
\(\Leftrightarrow M_A+M_B=6,4:0,1=64\left(3\right)\)
Thế các nguyên tố đầu bài vào (3), ta tìm được A là Mg, B là Ca (hoặc ngược lại)
Vậy CTTH của hai oxit: MgO, CaO
Bài 2:
Gọi x,y lần lượt là số mol của Fe2O3, FeO
nH2O = \(\dfrac{2,88}{18}=0,16\) mol
Pt: Fe2O3 + 3H2 --to--> 2Fe + 3H2O
........x............3x.........................3x
.......FeO + H2 --to--> Fe + H2O
........y.........y.........................y
Ta có hệ pt: \(\left\{{}\begin{matrix}160x+72y=9,6\\3x+y=0,16\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,034\\y=0,06\end{matrix}\right.\)
P/s: bn bấm máy tính rồi tự làm tròn nha
=> %
nH2 = 3x + y = 3 . 0,034 + 0,06 = 0,162 mol
=> VH2 = 0,162 . 22,4 = 3,63 (lít)

1)
\(C+H_2O\underrightarrow{t^O}CO+H_2\) (1)
\(C+2H_2O\underrightarrow{t^o}CO_2+2H_2\) (2)
2)
Gọi số mol CO, CO2 là a, b (mol)
\(n_{H_2\left(1\right)}=n_{CO}=a\left(mol\right)\)
\(n_{H_2\left(2\right)}=2b\left(mol\right)\)
=> \(n_{H_2}=a+2b\left(mol\right)\)
=> a + b + (a+2b) = \(\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
=> 2a + 3b = 0,5
PTHH: \(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
\(CuO+CO\underrightarrow{t^o}Cu+CO_2\)
=> \(n_{H_2}+n_{CO}=n_{Cu}=\dfrac{25,6}{64}=0,4\)
=> (a + 2b) + a = 0,4
=> 2a + 2b = 0,4
=> a = 0,1 ; b = 0,1
=> X chứa \(\left\{{}\begin{matrix}CO:0,1\left(mol\right)\\CO_2:0,1\left(mol\right)\\H_2:0,3\left(mol\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}\%V_{CO}=\dfrac{0,1}{0,5}.100\%=20\%\\\%V_{CO_2}=\dfrac{0,1}{0,5}.100\%=20\%\\\%V_{H_2}=\dfrac{0,3}{0,5}.100\%=60\%\end{matrix}\right.\)
\(\overline{M}_X=\dfrac{0,1.28+0,1.44+0,3.2}{0,5}=15,6\left(g/mol\right)\)
=> \(d_{X/O_2}=\dfrac{15,6}{32}=0,4875\)

1. C + H2O \(\underrightarrow{t^o}\) CO + H2
C + 2H2O \(\underrightarrow{t^o}\) CO2 + 2H2.
2. Lượng Cu thu được là 0,4 mol, suy ra lượng đồng (II) oxit phản ứng là 0,4 mol. Lượng nguyên tử oxi phản ứng là 0,4 mol.
Suy ra, tổng lượng CO và H2 trong X là 0,4 mol. Lượng khí X là 0,5 mol. Suy ra, số mol CO2 là 0,1 mol.
Gọi a mol và b mol lần lượt là số mol của CO và H2 có trong X.
Lượng C và H2O ban đầu lần lượt là (0,1+a) mol và b mol.
BTKL: 12(0,1+a)+18b=28a+2b+44.0,1 (1)
a+b=0,4 (2).
Từ (1) và (2), suy ra a=0,1 và b=0,3.
Tỉ lệ phần trăm thể tích các khí có trong X:
%VCO=0,1/0,5=20%, %\(V_{H_2}\)=0,3/0,5=60%, %\(V_{CO_2}\)=20%.
Phân tử khối trung bình của X là (28.0,1+2.0,3+44.0,1)/0,5=7,6.
Tỉ khối của X so với oxi là dX/O=7,6/16=0,475.
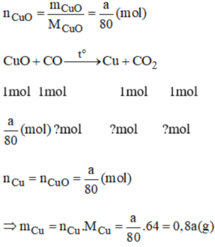
a = 150g
⇒ m C u = 0,8a = 0,8.150 = 120(g)