Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

- Một số tính chất hoá học của muối:
+ Dung dịch muối tác dụng với kim loại;
+ Muối tác dụng với dung dịch acid;
+ Dung dịch muối tác dụng với dung dịch base;
+ Dung dịch muối tác dụng với dung dịch muối.
+ Một số muối có thể bị nhiệt phân
- Muối có thể được điều chế bằng một số phương pháp như:
+ Dung dịch acid tác dụng với base;
+ Dung dịch acid tác dụng với oxide base;
+ Dung dịch acid tác dụng với muối;
+ Oxide acid tác dụng với dung dịch base;
+ Dung dịch muối tác dụng với dung dịch muối.

Oxit là hợp chất của oxi và một nguyên tố khác
TCHH:
+Oxide base tác dụng với dung dịch acid tạo thành muối và nước.
+Oxide acid tác dụng với dung dịch base tạo thành muối và nước.

b, Acid là:
+ HCL: hydrochloric acid
+ H2SO4: sulfuric acid
+ HNO3: nitric acid
c, Base là:
+ KOH: potassium hydroxide
+ Ba(OH)2: barium hydroxide
+ Cu(OH)2 : copper (II) hydroxide
d, Muối là:
+ Na2CO3: sodium cacbonat
+ CaSO3 : calcium sunfit
+ NH4Cl : ammonium chloride
+ NaHCO3: sodium hydrogen carbonate
+ CH3COONa: sodium acetat

Hòa tan muối ăn vào nước, được dung dịch trong suốt.
Cô cạn dung dịch, những hạt muối ăn lại xuất hiện.
- Khi cô cạn dung dịch muối ăn ở thể rắn còn khi hóa tan muối ăn ở thể dung dịch

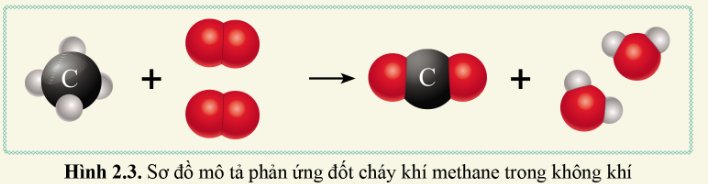
a. Trước phản ứng, có các chất là C, H, O.
- Những nguyên tử H đã liên kết với nguyên tử C, nguyên tử O liên kết với nguyên tử O.
b. Sau phản ứng, có các chất được tào thành là CO2, H2O.
- Những nguyên tử O đã liên kết với nguyên tử C, những nguyên tử H đã liên kết với những nguyên tử O.
c. Số nguyên tử C, H, O trước phản ứng và sau phản ứng đều bằng nhau

Tham khảo
- Khái niệm enzyme: Enzyme là chất xúc tác sinh học đặc hiệu làm tăng tốc độ phản ứng, không bị biến đổi khi kết thúc phản ứng.
- Vai trò của enzyme tiêu hóa: Enzyme tiêu hóa có vai trò xúc tác cho các phản ứng phân giải các chất trong thức ăn (tinh bột, chất đạm, chất béo,...) thành các chất dinh dưỡng mà cơ thể có thể hấp thu được. Như vậy, nhờ sự hoạt động của enzyme tiêu hóa, quá trình tiêu hóa thức ăn được diễn ra với tốc độ nhanh chóng, đáp ứng kịp thời nhu cầu dinh dưỡng của cơ thể.

- muối tác dụng với kim loại tạo ra muối mới và kim loại mới (với kim loại tham gia phản ứng mạnh hơn kim loại có trong muối)
- muối tác dụng với aicd tạo thành muối mới và acid mới (với sản phẩm là chất khí, chất kết tủa hoặc nước)
- muối tác dụng với base tạo thành muối mới và base mới (với sản phảm là chất khí, chất kết tủa hoặc nước)
- muối tác dụng với muối tạo thành 2 muối mới (với sản phẩm là chất khí, chất kết tủa hoặc nước)

1. Định nghĩa về muối
Muối là hợp chất hóa học được tạo thành từ sự kết hợp giữa cation (ion mang điện dương) và anion (ion mang điện âm). Cation có thể là ion kim loại (như Na⁺, Ca²⁺) hoặc ion amoni (NH₄⁺), trong khi anion có thể là ion gốc axit (ví dụ: Cl⁻, SO₄²⁻, NO₃⁻).
- Muối được hình thành khi:
- Ion H⁺ của acid (ví dụ: HCl, H₂SO₄) được thay thế bằng một ion kim loại (ví dụ: Na⁺, Mg²⁺) hoặc ion amoni (NH₄⁺).
- Ví dụ: khi HCl phản ứng với NaOH, ta thu được NaCl (muối clorua natri) và nước.
2. Khả năng tan trong nước của muối
Muối có khả năng hòa tan trong nước khác nhau, phụ thuộc vào các yếu tố như:
- Loại muối: Một số muối tan tốt trong nước, một số muối chỉ tan ít hoặc không tan.
- Nhiệt độ nước: Một số muối có thể tan tốt hơn ở nhiệt độ cao hơn.
- Sự hiện diện của các ion khác trong dung dịch: Các ion có thể ảnh hưởng đến độ tan của muối, ví dụ trong dung dịch bão hòa.
Các nhóm muối có thể phân loại theo khả năng tan:
- Muối tan nhiều: Các muối này có thể hòa tan dễ dàng trong nước, ví dụ NaCl (muối ăn), KNO₃ (muối kali nitrat).
- Muối tan ít: Các muối này hòa tan một lượng nhỏ trong nước, ví dụ AgCl (muối bạc clorua), BaSO₄ (muối bari sulfat).
- Muối không tan: Một số muối gần như không tan trong nước, ví dụ PbSO₄ (muối chì(II) sulfat).
3. Tên muối (chứa cation kim loại)
Khi gọi tên các muối, ta dựa vào hai yếu tố chính: tên của cation (ion mang điện dương) và tên của anion (ion mang điện âm). Quy tắc đặt tên muối chứa cation kim loại được thực hiện như sau:
- Tên kim loại: Nếu kim loại có nhiều hóa trị (như Fe, Cu, Pb, Sn), ta phải chỉ rõ hóa trị của nó bằng cách ghi số hóa trị trong dấu ngoặc đơn sau tên kim loại. Nếu kim loại chỉ có một hóa trị (như Na, K, Ca), ta không cần chỉ hóa trị.
- Tên gốc axit: Đối với gốc axit, ta lấy tên gốc của axit, thay thế "-ic" bằng "-at" đối với axit có gốc axit "-ic" (ví dụ: H₂SO₄ → SO₄²⁻), và thay "-ous" bằng "-it" đối với axit có gốc "-ous" (ví dụ: H₂SO₃ → SO₃²⁻).
Ví dụ:
- FeCl₂: Tên là sắt(II) clorua. Kim loại sắt có hóa trị II, và anion là clorua (Cl⁻).
- FeCl₃: Tên là sắt(III) clorua. Kim loại sắt có hóa trị III, và anion là clorua.
- CuSO₄: Tên là đồng(II) sulfat. Kim loại đồng có hóa trị II, và anion là sulfat (SO₄²⁻).
- NaCl: Tên là natri clorua. Kim loại natri chỉ có hóa trị I, và anion là clorua.
Tóm tắt lại các điểm quan trọng:
- Muối là hợp chất tạo thành từ sự thay thế ion H⁺ của axit bởi ion kim loại hoặc ion amoni (NH₄⁺).
- Khả năng tan trong nước của muối có sự khác biệt rõ rệt, có muối tan tốt, muối tan ít và muối không tan.
- Cách gọi tên muối: Tên muối bao gồm tên cation (kèm hóa trị nếu cần) và tên gốc của axit.


Tham khảo :
- Muối là những hợp chất được tạo ra khi thay thế ion H+ trong acid bằng ion kim loại hoặc ion ammonium (NH4+).
- Tính chất hoá học của muối:
+ Dung dịch muối có thể tác dụng với kim loại tạo thành muối mới và kim loại mới.
+ Muối có thể tác dụng với dung dịch acid tạo thành muối mới và acid mới.
+ Muối có thể tác dụng với dung dịch base tạo thành muối mới và base mới.
+ Hai dung dịch muối có thể tác dụng với nhau tạo thành hai muối mới.
- Mối liên hệ giữa muối và các hợp chất khác được thể hiện bằng sơ đồ sau: