Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Khi đốt cháy Y: nCO2 = 0,3 mol < nH2O = 0,4 mol => ancol no
Có nC : nH = 3 : 8 => C3H8Ox.
Vì Este mạch hở hủy phân tạo 1 ancol + hỗn hợp muối
=> ancol 2 chức, este đơn chức.
Vì Y không hòa tan được Cu(OH)2 nên 2 nhóm Oh không kề nhau.
=> HOCH2-CH2-CH2-OH là CTCT của Y.
=> nY = 0,1 mol => nKOH = 2nY = 0,2 mol
Bảo toàn khối lượng: m + mKOH = mmuối + mancol
=> m = 14,6g
Đáp án cần chọn là: D

Khi đốt cháy Y: nCO2 = 0,4 mol < nH2O = 0,5 mol => ancol no
Có nC : nH = 4 : 10 => Y có CT: C4H10Ox.
Mà Y không có khả năng phản ứng với Cu(OH)2 => x<3
Vì Este mạch hở hủy phân tạo 1 ancol + hỗn hợp muối
=> ancol 2 chức, este đơn chức và Y có 2 nhóm OH.
=> CT của Y là C4H10O2
=> nY = 0,1 mol => nNaOH = 2nY = 0,2 mol
Bảo toàn khối lượng: m + mNaOH = mmuối + mancol
=> m = 16g
Đáp án cần chọn là: C

Coi như hỗn hợp X chỉ gồm Na, K, Ba, O
Cho X vào nước thì 3 kim loại phản ứng sinh ra khí H2, còn O tác dụng với H2 để tạo ra nước theo tỷ lệ 1Oxi+1H2
\(\Rightarrow\) \(n_{H_2}=\frac{1}{2}n_{Na}+\frac{1}{2}n_K+n_{Ba}-n_O=0,14\left(mol\right)\)
Có \(n_{Na}=n_{NaOH}=0,18\left(mol\right)\)
\(n_K=n_{KOH}=\frac{0,044m}{56};n_{Ba}=n_{Ba\left(OH\right)_2}=\frac{0,93m}{171}\left(mol\right)\)
\(\Rightarrow n_O=\frac{1}{2}n_{Na}+\frac{1}{2}n_K+n_{Ba}-n_{H_2}=0,09+\frac{0,022m}{56}+\frac{0,465m}{171}\)
Lại có phương trình tổng khối lượng hỗn hợp X:
\(m_X=m=m_{Na}+m_K+m_{Ba}+m_O\\ =0,18.23+\frac{0,044m}{56}.39+\frac{0,93m}{171}.137+m_O\)
Thay số mol Oxi tính được (theo m) ở trên vào ta được phương trình 1 ẩn m
giải ra được \(m\approx25,5\)
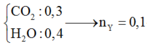
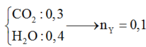

Giải thích:
nCO2 = 0,3 (mol); nH2O = 0,4 (mol)
=> nY = nH2O – nCO2 = 0,1 (mol)
=> Số C trong Y = nCO2/ nH2O = 0,3/0,1 = 3 (mol)
=> CTPT của Y: C3H8O2
Y không có khả năng phản ứng với dd Cu(OH)2 => CTCT của Y: CH2OH- CH2-CH2OH : 0,1 (mol)
X + KOH → muối + ancol
=> nKOH = 2nancol = 0,2 (mol)
BTKL: mX = mmuối + mancol – mKOH = 18,2 + 0,1.76 – 0,2.56 = 14,6 (g)
Đáp án D