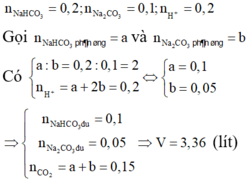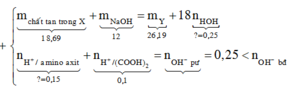Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Hoà tan hoàn toàn hỗn hợp Na2O, Al2O3 vào nước được dung dịch trong suốt X (NaOH dư,NaAlO2)
Chú ý thứ tự các phản ứng khi thêm dung dịch HCl vào dung dịch X
HCl + NaOH → NaCl + H2O (1)
NaAlO2+ HCl+ H2O → NaCl + Al(OH)3 (2)
Al(OH)3 + 3HCl → AlCl3 + 3H2O (3)
Khi thêm 0,1 mol HCl thì bắt đầu xuất hiện kết tủa → nNaOH dư = 0,1 mol (xảy ra (1))
Khi thêm 0,2 mol HCl thì xảy ra (1), (2) ( lượng AlO2- trong pt (2)dư )
→ nkết tủa = nH+ phản ứng (2) = 0,2 - 0,1 = 0,1 mol → a = 7,8 gam. Loại B,D
Khi thêm 0,6 mol HCl xảy ra hiện tượng hòa tan kết tủa (xảy ra cả 3 phương trình)
→ 4×nAlO2- = 3nkết tủa + (nH+ -0,1) → nAlO2- = 0,2 mol
Vậy NaAlO2 0,2 mol, NaOH dư 0,1 mol → m= mAl2O3 + mNa2O = 0,1×102 + 0,15×62 = 19,5 gam
Đáp án A

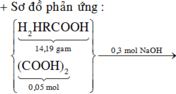
Đặt nP= x mol, nOH- =0,15 mol
TH1: Axit dư, x > 0,15
Dễ thấy chất rắn gồm
(x-0,15)/2 mol P2O5, 0,1 mol NaH2PO4, 0,05 mol KH2PO4
→mrắn= 142. (x-0,15)/2+ 99.0,1+ 136.0,05 > 8,56 gam (Vô lí)
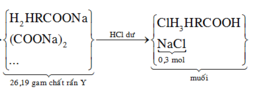
TH2: Kiềm dư, x < 0,15/3= 0,05
Chất rắn gồm: x mol PO43-, 0,15-3x mol OH-, 0,1 mol Na+, 0,05 mol K+
→ mrắn= 95x+ 17. (0,15-3x)+ 23.0,1+ 39.0,05= 8,56 gam
→ x= 0,04
Vậy nP2O5= 0,02 mol→m= 2,84 gam
TH3: Tạo hỗn hợp muối, 0,05 < x< 0,15
Chất rắn gồm:
H2PO4-, HPO42-, PO43- (hai trong 3 gốc này): x mol; K+: 0,05 mol, Na+: 0,1 mol
→mrắn= M.x+ 23.0,1+ 39.0,05
Vì x> 0,05 và M> 95 nên mrắn > 95.0,05+ 2,3+1,95=9 >8,56
→Không thỏa mãn
Đáp án D

Đáp án D
Giả sử kiềm có công thức chung là MOH (M=(0,1.23+0,05.39)/0,15=85/3)
Nếu phản ứng chỉ tạo 1 muối:
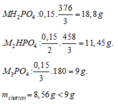
=> MOH dư, phản ứng tạo muối M3PO4.
Đặt nM3PO4=x mol, nMOH=y mol;
180x+136y/3=8,56
3x+y=nMOH=0,15
=> x=0,04, y=0,03.
=> nP2O5=0,04/2=0,02 mol
=> mP2O5=2,84 gam.

Đáp án B
Giả sử dung dịch kiềm có công thức chung là: MOH: 0,15 (mol) với
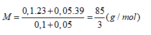
+ Nếu phản ứng chỉ tạo 1 muối:
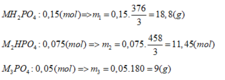
Ta thấy 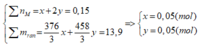
BTNT: P => nP = nMH2PO4 + nM2PO4 = 0,05 + 0,05 = 0,1 (mol)
=> nP2O5 = ½ nP = 0,05 (mol)
=> mP2O5 = 0,05. 142 = 7,1 (g)