Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

nếu học lớp 9 thì vào tìm câu trả lời tương tự ấy
tick nha
Chúc bạn học tốt![]()

1 mol A tác dụng với lượng dư Cu(OH)2/NaOH thu được 2 mol kết tủa đỏ gạch ⇒ A là andehit 2 chức và anđehit fomic.
CTHH của A : CnH2n-2k(CHO)2
Xét đáp án A:\(\%C = \dfrac{12}{30}.100\% = 40\%\)(Không thỏa mãn)
Xét đáp án B :\(\%C = \dfrac{12.3}{72}.100\% = 50\% > 40\%\)(Thỏa mãn)
Xét đáp án C :\(\%C = \dfrac{12.4}{86}.100\% = 55,81\%>40\%\)(Thỏa mãn)
Xét đáp án D :\(\%C = \dfrac{12.2}{58}.100\% = 41,37\% > 40\%\)(Thỏa mãn)
Vậy,đáp án : B,C,D đúng

Số mol ankin trong mỗi phần 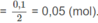
Khi đốt cháy hoàn toàn phần (1):
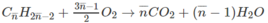
Cứ 1 mol C n H 2 n - 2 tạo ra ( n −1) mol H 2 O
Cứ 0,5. 10 - 1 mol C n H 2 n - 2 tạo ra 0,13 mol H 2 O
Như vậy trong hỗn hợp A phải có ankin có số nguyên tử cacbon nhỏ hơn 3,6 tức là phải có C 2 H 2 hoặc C 3 H 4 .
Nếu có C 2 H 2 thì số mol chất này ở phần 2 là:
n = 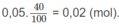
Khi chất này tác dụng với dung dịch A g N O 3 trong N H 3 :
C 2 H 2 + 2 A g N O 3 + 2 N H 3 → C 2 A g 2 ↓ + 2 N H 4 N O 3
0,02 mol 0,02 mol
Khối lượng 0,02 mol C 2 A g 2 là: 0,02. 240 = 4,8 (g) > 4,55 g.
Vậy hỗn hợp A không thể có C 2 H 2 mà phải có C 3 H 4 .
Khi chất này tác dụng với dung dịch A g N O 3 trong N H 3 :
C 3 H 4 + A g N O 3 + N H 3 → C 3 H 3 A g ↓ + N H 4 N O 3
0,02 mol 0,02 mol 0,02 mol
Khối lượng C 3 H 3 A g là 0,02.147 = 2,94 (g).
Số mol A g N O 3 đã phản ứng với các ankin là: 0,25.0,12 = 0,03 (mol): trong đó lượng A g N O 3 tác dụng với C 3 H 4 là 0,02 mol, vậy lượng A g N O 3 tác dụng với ankin khác là 0,01 mol.
Trong phần 2, ngoài 0,02 mol C 3 H 4 còn 0,03 mol 2 ankin khác. Vậy mà lượng A g N O 3 phản ứng chỉ là 0,01 mol, do đó trong 2 ankin còn lại, chỉ có 1 chất có phản ứng với A g N O 3 , 1 chất không có phản ứng:
C n H 2 n - 2 + A g N O 3 + N H 3 → C n H 2 n - 3 A g ↓ + N H 4 N O 3
0,01 mol 0,01 mol 0,01 mol
Khối lượng 0,010 mol C n H 2 n - 3 A g là: 4,55 - 2,94 = 1,61(g).
Khối lượng 1 mol C n H 2 n - 3 A g là 161 g.
14n + 105 = 161 ⇒ n = 4.
Công thức phân tử là C 4 H 6 và CTCT: C H 3 - C H 2 - C ≡ C H (but-1-in)
Đặt công thức chất ankin chưa biết là C n ' H 2 n ' - 2 :
C 3 H 4 + 4 O 2 → 3 C O 2 + 2 H 2 O
0,02 mol 0,04 mol
C 4 H 6 + 5,5 O 2 → 4 C O 2 + 3 H 2 O
0,01 mol 0,03 mol
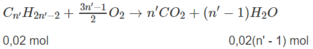
Tổng số mol H 2 O : 0,04 + 0,03 + 0,02(n' - 1) = 0,13 ⇒ n' = 4.
Chất ankin thứ ba có CTPT C 4 H 6 nhưng không tác dụng với A g N O 3 nên CTCT là C H 3 - C ≡ C - C H 3 (but-2-in).
Thành phần về khối lượng:
Propin chiếm: 33,1%; but-1-in : 22,3%; but-2-in: 44,6%.

Câu 1:
a ,\(C_2H_2+2AgNO_3+2NH_3\rightarrow Ag_2C_2+NH_4NO_3\)
0,04__________________________________0,04
\(n_{kt}=0,04\left(mol\right)\)
\(\Rightarrow n_{C3H6}=0,05\left(mol\right)\)
% m(C2H2) = 0,04.26/3,14 . 100% =33,12 %
=> % m(C3H6) = 66 ,88%
b, 9,42 g sẽ có 0,12 mol C2H2 và 0,15 mol C3H6
Tổng số lk pi = 0,12.2+0,15=0,39 (mol)
V = 0,39 (l) = 390 (ml)

Gọi CT: CxHyOz
Bảo toàn khối lượng: m(A)= 59,49 +1.48- 1,2.50=0.97 suy ra M=0.97/0.005=194
Bảo toàn Na: n NaOH =2 n Na2CO3=0.015
suy ra: m NaOH= 0.6 gam suy ra mH2O=59,4 suy ra nH2O=3.3
Bảo toàn C: nC(trong A)=0.05
Bảo toàn H: nH(trong A)=0.05
suy ra m O(trong A)=0.97-12.0,05-0,05=0.32gam suy ra n O(trong A)=0.01
Suy ra : x:y:z= 0.05:0.05:0.01= 5:5;1
Suy ra (C5H5O)n= 194 suy ra n=2
vậy CTPT: C10H10O2