Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi oxit kim loại là R2On Kim loại này phải có số oxh thay đổi
nCO=1,792/22,4=0,08 mol
R2On + nCO =>2 R + nCO2
0,08/n mol<=0,08 mol=>0,16/n mol
nH2=1,344/22,4=0,06 mol
2R +2mHCl =>2RClm +m H2
0,12/m mol<= 0,06 mol
=>m/n=4/3
Có 0,08/n(2R+16n)=4,64=>R=21n chọn n=8/3=>R=56 Fe
Oxit kim loại là Fe3O4
Gọi công thức oxit kim loại là :MxOy
_Tác dụng với CO:
nCO=1.792/22.4=0.08(mol)
MxOy+yCO=>xM+yCO2
0.08/y->0.08(mol)
=>nMxOy=0.08/y(1)
=>nO=0.08mol
=>mO=0.08*16=1.28(g)
=>mM=4.64-1.28=3.36(g)
nH2=1.344/22.4=0.06(mol)
2M+2nHCl=>2MCln+nH2
0.12/n----------------->0.06(mol)
=>M=3.36/0.12/n=28n
_Xét hóa trị của M từ 1->3:
+n=1=>M=28(loại)
+n=2=>M=56(nhận)
+n=3=>M=84(loại)
=>M là sắt (Fe)
=>nFe=0.12/2=0.06(mol)
=>nFexOy=0.06/x (2)
Từ(1)(2)=>
0.08/y=0.06/x
<=>0.08x=0.06y
<=>x/y=3/4
Vậy công thức oxit đầy đủ là Fe3O4

Gọi CT oxit là M2Om
Mol H2 TN1=0,06 mol
Mol H2 TN2=0,045 mol
M2Om + mH2→ 2M + mH2O
0,06/m mol<=0,06 mol. =>0,12/m mol
=>0,06(2M+16m)/m=3,48
2M + 2nHCl→ 2MCln + nH2
0,12/m mol. 0,045 mol
⇒⇒0,045.2/n=0,12/m⇒⇒m=8/3; n=2 tm
Thay m=8/3 vào công thức tính m có M=56 FeFe
Oxit là Fe3O4 vì n=8/3

\(n_{H_2thuđược}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
\(n_{H_2cầndùng}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
Ta có : Số mol Oxi/Oxit = n H2 dùng = 0,6 ( mol )
\(m_{\dfrac{O}{Oxit}}=0,6.16=9,6\left(g\right)\)
\(m_{\dfrac{M}{Oxit}}=32-9,6=22,4\left(g\right)\)
Gọi hóa trị M là n
PTHH :
\(2M+2nHCl\rightarrow2MCl_2+nH_2\uparrow\)
\(\dfrac{2}{n}.0,4\) 0,4
\(M_M=\dfrac{22,4}{\dfrac{2}{n}.0,4}=28.n\)
| n | 1 | 2 | 3 |
| M | 28 | 56 | 84 |
| Dk | (L) | T/M (Fe) | (L) |
Vậy kim loại M là Fe
\(\rightarrow\dfrac{n_{Fe}}{n_O}=\dfrac{\dfrac{22,4}{56}}{0,6}=\dfrac{2}{3}\)
Vậy CTPT của Oxit kim loại M là Fe2O3 .
Gọi hoá trị M là x nhưng mình làm lộn thành n , bạn đổi lại x thành n nha

1/Gọi công thức oxit kim loại:MxOy
_Khi cho tác dụng với khí CO tạo thành khí CO2.
MxOy+yCO=>xM+yCO2
_Cho CO2 tác dụng với dd Ca(OH)2 tạo thành CaCO3:
nCaCO3=7/100=0.07(mol)=nCO2
CO2+Ca(OH)2=>CaCO3+H2O
0.07------------------>0.07(mol)
=>nO=0.07(mol)
=>mO=0.07*16=1.12(g)
=>mM=4.06-1.12=2.94(g)
_Lượng kim loại sinh ra tác dụng với dd HCl,(n là hóa trị của M)
nH2=1.176/22.4=0.0525(mol)
2M+2nHCl=>2MCln+nH2
=>nM=0.0525*2/n=0.105/n
=>M=28n
_Xét hóa trị n của M từ 1->3:
+n=1=>M=28(loại)
+n=2=>M=56(nhận)
+n=3=>M=84(loại)
Vậy M là sắt(Fe)
=>nFe=0.105/2=0.0525(mol)
=>nFe:nO=0.0525:0.07=3:4
Vậy công thức oxit kim loại là Fe3O4.

PTHH: CuO + CO → Cu + CO2 ↑
FexOy + yCO → xFe + yCO2 ↑
Cu + HCl → Không phản ứng
Fe + 2HCl → FeCl2 + H2 ↑
Số mol của H2 là: 1,792 : 22,4 = 0,08 mol
Số mol của Fe là: 0,08 . 1 = 0,08 mol
Khối lượng của Fe là: 0,08 . 56 = 4,48 gam
Khối lượng của Cu là: 7,04 - 4,48 = 2,56 gam
Số mol của Cu là: 2,56 : 64 = 0,04 mol
Khối lượng của CuO là: 0,04 . 80 = 3,2 gam
Khối lượng của ôxit sắt là: 9,6 - 3,2 = 6,4 gam
Số mol của Ôxit sắt tính theo khối lượng là:
\(\frac{6,4}{56x+16y}\) (mol)
Số mol của ôxit sắt tính theo pt là: 0,08 : x
<=> \(\frac{6,4}{56x+16y}=\frac{0,08}{x}\) => x : y = 2 : 3
=> CTHH của ôxit sắt là: Fe2O3


Ta có bảng sau:
n |
1 |
2 |
3 |
4 |
M |
21 (loại) |
42 (loại) |
63 (loại) |
84 (loại) |
=> loại trường hợp này


B1:
Gọi số mol của CuO và FexOy là a (mol)
\(\text{=> 80a + (56x+16y)a= 2,4 (1)}\)
Khối lượng kim loại thu được là Cu và Fe. Bảo toàn nguyên tố ta có nCu = a mol; nFe = ax mol => 64a + 56ax = 1,76 (2)
Cho Cu và Fe tác dụng với HCl chỉ có Fe tác dụng,\(\text{nFe = nH2 => ax = 0,02 mol (3)}\)
Từ (1)(2)(3) => a = 0,01 ; x = 2, y = 3
Vậy công thức oxit sắt là Fe2O3
B3:
Gọi oxit là RxOn
\(\text{RxOy + yCO -> xR +yCO2}\)
\(\text{CO2 + Ca(OH)2 -> CaCO3 + H2O}\)
Ta có kết tủa là CaCO3 -> nCaCO3=22/100=0,22 mol
Theo ptpu: nCO2=nCaCO3=0,22 mol -> nO trong oxit =nCO2=0,22 mol
\(\text{-> mR=12,76-mO=12,76-0,22.16=9,24 gam}\)
Gọi n là hóa trị của R
Cho 9,24 gam R tác dụng với H2SO4 đặc nóng dư thu được 0,2475 mol SO2 (bạn ghi sai đề, 5,544 mới đúng)
\(\text{2R + 2nH2SO4 -> R2(SO4)n + n SO2 + H2O}\)
-> nR=2nSO2/n=0,2475.2/n=0,495/n -> MR=9,24/(0,495/n)=56/3 .n
Thỏa mãn n=3 -> MR=56 -> R là Fe
\(\text{-> nFe=0,165 mol -> oxit là FexOy với x:y=0,165;0,22=3:4 -> Fe3O4}\)
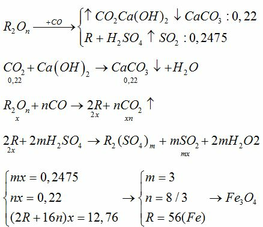
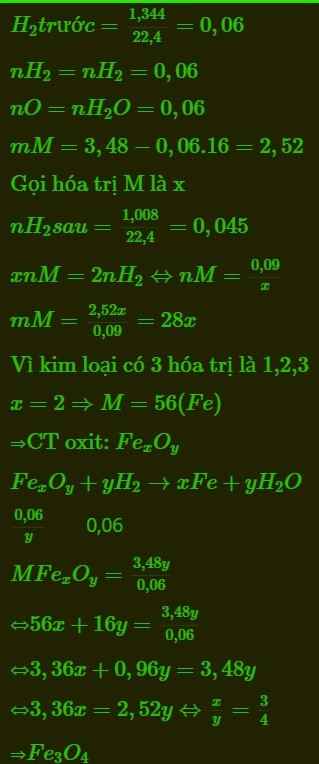
Gọi CTTQ của Oxit kim loại R là \(R_xO_y\).
PTPƯ 1 : \(R_xO_y+yH_2\underrightarrow{t^o}xR+yH_2O\)
\(n_{H_2}=\dfrac{V}{22,4}=\dfrac{3,136}{22,4}=0,14\left(mol\right)\)
=> \(n_{H_2O}=0,14\left(mol\right)\)
- Áp dụng định luật bảo toàn khối lượng :
\(m_R=8,12+0,14\times2-0,14\times18=5,88\left(g\right)\)
PTPƯ 2 : \(2R+2nHCl\rightarrow2RCl+nH_2\uparrow\)
\(\Rightarrow n_{H_2}=\dfrac{2,352}{22,4}=0,105\left(mol\right)\)
\(\Rightarrow n_R=\dfrac{2}{n}.n_{H_2}=\dfrac{2.0,105}{n}=\dfrac{0,21}{n}\left(mol\right)\)
\(\Rightarrow M_R=\dfrac{m}{n}=\dfrac{5,88}{\dfrac{0,21}{n}}=28n\)
\(\rightarrow n=2\rightarrow R=2.28=56\)
\(\rightarrow R=Fe\)
\(\Rightarrow n_{Fe}=\dfrac{m}{M}=\dfrac{0,21}{2}=0,105\left(mol\right)\)
\(m_O=8,12-0,105\times56=2,24\left(g\right)\)
\(\Rightarrow n_O=\dfrac{m}{M}=\dfrac{2,24}{16}=0,14\left(mol\right)\)
\(\dfrac{x}{y}=\dfrac{n_{Fe}}{n_O}=\dfrac{0,105}{0,14}=\dfrac{3}{4}\)
Vậy công thức của Oxit kim loại R (Fe) là \(Fe_3O_4\).