Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

sao chị ko đáp lại câu trả lời của em ở câu trước , chị ko biết hả ?

a)
Giả sử lấy lượng mỗi chất là a gam.
MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O (1)
2KMnO4 + 14 HCl → 2MnCl2 + 2KCl + 5Cl2 + 8H2O (2)
K2Cr2O7 + 14 HCl → 2CrCl2 + 2KCl + 3Cl2 + 7H2O (3)
Vậy dùng : KMnO4 điều chế được nhiều Cl2 hơn
b) Nếu số mol các chất bằng n mol
Theo (1) nmol MnO2 → nmol Cl2
Theo (2) nmol KMnO4 → 2,5 nmol Cl2
Theo (3) nmol K2Cr2O7 → 3nmol Cl2
Ta có: 3n > 2,5n > n
Vậy dùng K2Cr2O7 được nhiều hơn Cl2 hơn
a) Giả sử lấy lượng mỗi chất là a gam.
MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O (1)
2KMnO4 + 14 HCl → 2MnCl2 + 2KCl + 5Cl2 + 8H2O (2)
K2Cr2O7 + 14 HCl → 2CrCl2 + 2KCl + 3Cl2 + 7H2O (3)
Vậy dùng : KMnO4 điều chế được nhiều Cl2 hơn
b) Nếu số mol các chất bằng n mol
Theo (1) nmol MnO2 → nmol Cl2
Theo (2) nmol KMnO4 → 2,5 nmol Cl2
Theo (3) nmol K2Cr2O7 → 3nmol Cl2
Ta có: 3n > 2,5n > n
Vậy dùng K2Cr2O7 được nhiều Cl2 hơn

a) Hỗn hợp A gồm FeS (x mol), Fe dư (y mol) và S dư (0,8 gam)
FeS + 2HCl -------> FeCl2 + H2S
x………………..………x…….x (mol)
Fe + 2HCl -------> FeCl2 + H2
y…………………..…y……..y (mol)
=> Khí D gồm H2S và H2
\(M_D=\dfrac{34x+2y}{x+y}=9.2=18\) (*)
Khí D sục rất từ từ qua dung dịch CuCl2
H2S + CuCl2 -------> CuS + 2HCl
x………………………...x (mol)
=>\(n_{CuS}=x=\dfrac{9,6}{96}=0,1\left(mol\right)\)
Từ (*) => y = 0,1 (mol)
nFe = x+ y = 0,1 + 0,1= 0,2 (mol)
=> m = 0,2 .56 = 11,2 (g)
nS pư = x = 0,1 (mol)
=> p = 0,1.32 + 0,8 = 4 (g)
b) Dung dịch C chứa FeCl2
nFeCl2 = x + y = 0,2 (mol)
FeCl2 + 2NaOH -------> Fe(OH)2 + 2NaCl
0,2................................,.0,2 (mol)
4Fe(OH)2 + O2 + 2H2O -------> 4Fe(OH)3
0,2..............................................0,2 (mol)
2Fe(OH)3 ------> Fe2O3 + 3H2O
0,2........................0,1 (mol)
Chất rắn là Fe2O3
Theo PT => nFe2O3 = 0,1 mol
=> mFe2O3 = 0,1.160 = 16 gam

Gọi x,y là số mol Fe phản ứng, Fe dư
Fe+S\(\rightarrow\)FeS
.x.....x.........x
FeS+2HCl−−−>FeCl2+H2S
.....x....................................x
Fe+2HCl−−−>FeCl2+H2
...y................................y
H2S+Pb(NO3)2−−−>PbS\(\downarrow\)+2HNO3
0,1..............................0,1........
Ta có: \(\dfrac{34x+2y}{x+y}\)=18
=> x=y=0,1
m\(_{Fe}\)bđ=m\(_{Fe}\) pứ + m\(_{Fe}\) dư =0,1.2.56=11,2(g)
m\(_S\)bđ=m\(_S\) pứ + m\(_S\) dư =0,1.32+0,8=4(g)

a) Giả sử lấy lượng mỗi chất là a gam
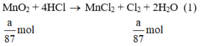
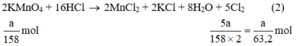
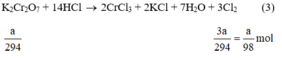
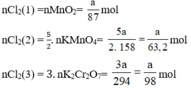
Ta có: 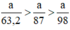
Lượng Cl2 điều chế được từ pt (2) nhiều nhất.
Vậy dùng KMnO4 điều chế được nhiều Cl2 hơn.
b) Nếu lấy số mol các chất bằng a mol
Theo (1) nCl2(1) = nMnO2 = a mol
Theo (2) nCl2(2) = 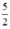 . nKMnO4 = 2,5a mol
. nKMnO4 = 2,5a mol
Theo (3) nCl2(3) = 3. nK2Cr2O7 = 3a mol
Ta có: 3a > 2,5a > a.
⇒ lượng Cl2 điều chế được từ pt (3) nhiều nhất.
Vậy dùng K2Cr2O7 được nhiều Cl2 hơn.

Trong 4 chất trên, H2SO4 đặc hút nước mạnh nhất nên là chất tốt nhất để tách hơi nước ra khỏi khí oxi

Ta có pthh:
\(Fe+S\underrightarrow{t^o}FeS\left(1\right)\)
x1 x1 x1 (mol)
Sau khi nung trong hỗn hợp A có :
\(\left(x-x_1\right)molS\)
\(\left(2x-x_1\right)molFe\)
và x1 mol FeS
- hòa tan A trong axit HCl dư :
\(Fe+2HCl\rightarrow FeCL_2+H_2\uparrow\left(2\right)\)
\(FeS+2HCl\rightarrow FeCl_2+H_2S\uparrow\left(3\right)\)
Còn lại 0,4 g chất rắn B là lưu huỳnh dư
\(nS=x-x_1=\dfrac{0,4}{32}=0,0125\left(mol\right)\left(I\right)\)
Dung dịch C gồm HCl dư và FeCl2 với số mol là 2x .
Khí D gồm H2 và H2S .
Sục khí D từ từ vào dung dịch CuCl2 dư , chỉ có H2S phản ứng.
\(CuCl_2+H_2S\rightarrow CuS\downarrow+2HCl\left(4\right)\)
Kết tủa đen tạo thành là CuS
theo (1) (2) , (4) :
\(nCuS=x_1=\dfrac{4,8}{96}=0,05\left(mol\right)\left(II\right)\)
Kết hợp (I) ; và (II) ta có : x - x1= 0,0125
x = 0,0125 + 0,05 = 0,0625
Hiệu suất pứ tạo thành hh A:
Theo S: \(h\%=\dfrac{0,05}{0,0625}.100\%=80\%\)


Dẫn khí oxi ẩm đi qua CaO để được khí oxi khô.
Chọn đáp án B.