Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Giải thích:
Quy đổi hỗn hợp X thành:
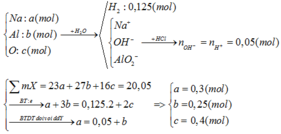
Khi thêm tiếp 310 ml HCl tức 0,31 mol HCl => ta thấy: nH+ > nAlO2- => kết tủa bị hòa tan một phần
Áp dụng công thức nhanh ta có:
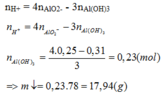
Đáp án D

Đáp án A
Y + 0,05 mol HCl → bắt đầu có ↓
⇒ Y gồm NaOH và NaAlO2.
⇒ nNaOH = nHCl = 0,05 mol.
► Quy X về Na, Al và O. Đặt nAl = x; nO = y.
⇒ nNaAlO2 = x ⇒ nNa/X = (x + 0,05) mol.
Bảo toàn electron:
(x + 0,05) + 3x = 2y + 2 × 0,125
|| mX = 23.(x + 0,05) + 27x + 16y = 20,05(g).
► Giải hệ có: x = 0,25 mol; y = 0,4 mol.
"Thêm tiếp" 0,31 mol HCl thì:
1 < nH+ ÷ nAlO2– = 0,31 ÷ 0,25 = 1,24 < 3
⇒ nH+ = 4nAlO2– - 3nAl(OH)3
⇒ nAl(OH)3 = (4 × 0,25 - 0,31) ÷ 3 = 0,23 mol
⇒ m = 17,94(g)

Giải thích:
Đặt x, y, z là số mol Na, Al, O
Phương trình 1 theo khối lượng đi: 23x + 27y + 16z = 20,05
Phương trình 2 bảo toàn điện tích: x + 2y = 0,125.2 + 2z
Phương trình 3 tính theo số mol OH-: nOH- = nNa= nAl + nH+ => x + y = 0,05
Giải hệ được : x= 0,3 ; y = 0,25 ; z = 0,4
n kết tủa = (4.nAlO2- - nH+)/3 = (4.0,25 – 0,31)/3 = 0,23 mol
=> m = 17,94g
Đáp án A

Coi như hỗn hợp X chỉ gồm Na, K, Ba, O
Cho X vào nước thì 3 kim loại phản ứng sinh ra khí H2, còn O tác dụng với H2 để tạo ra nước theo tỷ lệ 1Oxi+1H2
\(\Rightarrow\) \(n_{H_2}=\frac{1}{2}n_{Na}+\frac{1}{2}n_K+n_{Ba}-n_O=0,14\left(mol\right)\)
Có \(n_{Na}=n_{NaOH}=0,18\left(mol\right)\)
\(n_K=n_{KOH}=\frac{0,044m}{56};n_{Ba}=n_{Ba\left(OH\right)_2}=\frac{0,93m}{171}\left(mol\right)\)
\(\Rightarrow n_O=\frac{1}{2}n_{Na}+\frac{1}{2}n_K+n_{Ba}-n_{H_2}=0,09+\frac{0,022m}{56}+\frac{0,465m}{171}\)
Lại có phương trình tổng khối lượng hỗn hợp X:
\(m_X=m=m_{Na}+m_K+m_{Ba}+m_O\\ =0,18.23+\frac{0,044m}{56}.39+\frac{0,93m}{171}.137+m_O\)
Thay số mol Oxi tính được (theo m) ở trên vào ta được phương trình 1 ẩn m
giải ra được \(m\approx25,5\)

Đáp án D
Có n(NaOH) = 0,15 mol; n(H2) = 0,08 mol.
Dd X gồm Na+; ZnO2-, OH‑.
OH- + H+ → H2O
ZnO2- + 2H+ → Zn(OH)2 ↓
Zn(OH)2 + 2H+ → Zn2+ + H2O.
Dùng hết 0,08 mol HCl thì bắt đầu có kết tủa → n(OH-) = 0,08 mol.
Khi cho 0,32 mol HCl hay 0,48 mol HCl vào dd X đều thu được a gam kết tủa.
Có:
n(H+ trước) = 2.n↓ + n(OH-) → n↓ = (0,32 – 0,08) : 2 = 0,12 mol.
n(H+ sau) = 4.n(ZnO2-) – 2n↓ + n(OH-) → n(ZnO2-) = 0,16 mol.
BTĐT trong dd X → n(Na+) = 0,4 mol.
BTNT (H): n(NaOH) + 2n(H2O) = 2.n(H2) + n(OH-)
→ n(H2O) = (2.0,08 + 0,08) : 2 = 0,045 mol.
BTKL: m(hh) + m(NaOH) + m(H2O) = m(H2) + m(Na+) + m(ZnO2-) + m(OH-)
→ m = (0,08.2 + 23.0,4 + 0,16.97 + 0,08.17) – (0,15.40 + 0,045.18) = 19,43 gam.

Đáp án B
Cho từ từ 0,1 mol HCl vào dung dịch X thì bắt đầu xuất hiện kết tủa, chứng tỏ trong X có 0,1 mol OH - , các ion còn lại là Na+, Al OH 4 - .
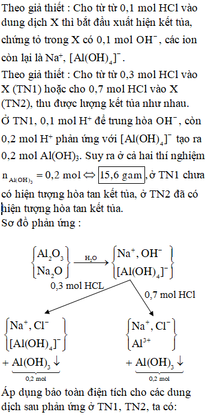
Cho từ từ 0,3 mol HCl vào X (TN1) hoặc cho 0,7 mol HCl vào X (TN2), thu được lượng kết tủa như nhau. Ở TN1, 0,1 mol H+ để trung hòa OH - , còn 0,2 mol H+ phản ứng với Al OH 4 - tạo ra 0,2 mol Al(OH)3. Suy ra ở cả hai thí nghiệm
![]()
ở TN1 chưa có hiện tượng hòa tan kết tủa, ở TN2 đã có hiện tượng hòa tan kết tủa.
Sơ đồ phản ứng :
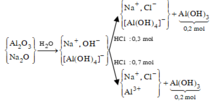
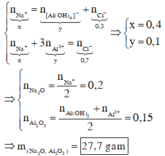
Áp dụng bảo toàn điện tích cho các dung dịch sau phản ứng ở TN1, TN2, ta có :
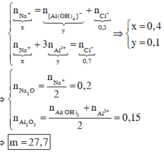

Giải thích:
Đặt x, y, z là số mol Na, Al, O
BTKL: 23x + 27y + 16z = 20.05
BTĐT: 1x + 2y = 0.125.2 + 2z
nOH- = nNa= nAl + nH+ => x + y = 0.05
Giải hệ 3 pt đc: x = 0,3, y = 0,25, z = 0,4
n kết tủa = (4 . nAlO2- - nH+)/3 = (4 . 0,25 – 0,31)/3 = 0,23
=> m = 17,94
Đáp án A