Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi công thức của ankan là CnH2n+2 x (mol) và anken CmH2m y (mol)
Ta có :
Số mol CO2 = 0,3 (mol)
Số mol H2O = 0,45 (mol)
\(\Rightarrow\) số mol ankan = 0,45 – 0,3 = 0,15 (mol)
\(\Rightarrow\) 0,15.n + ym = 0,3
\(\Rightarrow\) n <2
\(\Rightarrow\) 2 ankan là CH4 và C2H6
Trong A có 2 chất cùng số nguyên tử cacbon => anken C2H4

nCO2 = 0,2
nH2O = 0,3
nH2O > nCO2 ⇒ 2 Hidrocacbon đó là ankan
Gọi công thức chung của 2 chất đó là CnH2n+2 (n>1)
Ta có n CO2 : n H2O = n : (n+1) = 0,2 : 0,3 ⇒ n = 2
⇒ 2 chất đó là CH4 và C3H8
Đáp án D.

Đáp án : D
Ta có nCuO = 0,2 mol, nH2O = 0,3 mol
Ta có nH2O > nCO2 => ankan
Viết pt đốt cháy dễ dàng tìm được n trung bình = 2
=> CH4 và C3H8.

Gọi \(\left\{{}\begin{matrix}n_{CO_2}=a\left(mol\right)\\n_{H_2O}=b\left(mol\right)\end{matrix}\right.\)
\(m_{giảm}=m_{BaCO_3}-m_{CO_2}-m_{H_2O}\)
=> 44a + 18b = 29,5 (1)
Bảo toàn C; nC = a (mol)
Bảo toàn H: nH = 2b (mol)
=> 12a + 2b = 6,3 (2)
(1)(2) => a = 0,425 (mol); b = 0,6 (mol)
Do \(n_{CO_2}< n_{H_2O}\)
=> 2 hidrocacbon là ankan
nankan = 0,6 - 0,425 = 0,175 (mol)
=> \(\overline{C}=\dfrac{0,425}{0,175}=2,43\)
Mà 2 ankan liên tiếp nhau
=> 2 ankan là C2H6 và C3H8

Đáp án B
Có C ¯ = n C O 2 n X = 2 , 4 ⇒ 1 axit có 2 nguyên tử C, 1 axit có 3 nguyên tử C trong phân tử.
Vì 2 axit đơn chức n O t r o n g X = 2 n X = 0 , 2 ( m o l )
Bảo toàn nguyên tố O ta có:
![]()
=> Trong hai axit có một axit không no.
Vậy 2 axit là CH3COOH và C2H3COOH

Số mol 2 chất trong 6,55 g M là: 
Số mol 2 chất trong 2,62 g M là: 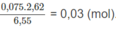
Giả sử trong 2,62 g M có a mol C x H y và b mol C x + 1 H y + 2
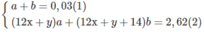
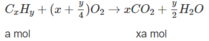
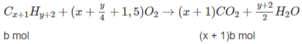
xa + (x + 1)b = 0,2 (3)
Từ (3), ta có x(a + b) + b = 0,2
b = 0,2 - 0,03x
Vì 0 < b < 0,03 nên 0 < 0,2 - 0,03x < 0,03.
⇒ 5,67 < x < 6,67 ⇒ x = 6 .
b = 0,2 - 0,03.6 = 0,02; a = 0,03 - 0,02 = 0,01
Thay giá trị của a và b vào (2), tìm được y = 6.
Khối lương
C
6
H
6
chiếm 
Khối lương C 7 H 8 chiếm 100 - 29,8% = 70,2%.

Số mol 2 chất trong 7,28g M: 
Số mol 2 chất trong 5,2g M: 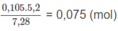
Theo định luật bảo toàn khối lượng:
m C O 2 + m H 2 O = m M + m O 2 = 12.4(g)
Theo đầu bài, số mol C O 2 = số mol H 2 O = n.
44n + 18n = 12,4 ⇒ n = 0,2 (mol)
Các chất trong hỗn hợp có chứa C, H và có thể có O. Chất thứ nhất là C X H Y O Z (a mol) và chất thứ 2 là C X + 2 H Y + 4 O Z (b mol).
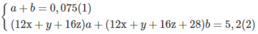
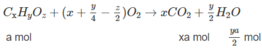
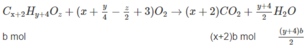
xa + (x + 2)b = 0,2 (3)
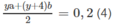
Giải hệ phương trình :
Từ (3) ta có x(a + b) + 2b = 0,200
2b = 0,200 - 0,0750x
b = 0,100 - 0,0375x
0 < b < 0,075 ⇒ 0 < 0,100 - 0,0375x < 0,0750
⇒ 0,660 < X < 2,66
Trong khoảng này có 2 số nguyên là 1 và 2.
Nếu x = 1.
b = 0,100 - 3.75. 10 - 2 = 0,0625
a = 0,0750 - 0,0625 = 0,0125.
Thay giá trị của a và b vào (4) ta có :
0125y + 0,0625(y + 4) = 0,400
⇒ y = 2.
Thay x = 1, y = 2; a = 0,0125, b = 0,0625 vào (2):
(14 + 16z).0,0125 + (42 + 16z).0,0625 = 5,20
⇒ z = 2.
C
H
2
O
2
chiếm: 
C 3 H 6 O 2 chiếm: 100% - 11,1% = 88,9%.
Nếu x = 2 .
b = 0,100 - 0,0375 X 2 = 0,0250
a = 0,0750 - 0,0250 = 0,05
từ đó tìm tiếp, ta được y = 4 và z = 2.
% khối lượng của
C
2
H
4
O
2
: 
% khối lương của C 4 H 8 O 2 : 100% - 57,7% = 42,3%.
Ta có:
\(n_{CO2}=\frac{8,36}{44}=0,19\left(mol\right)\)
\(\Rightarrow n_{C\left(X\right)}=n_{CO2}=0,19\left(mol\right)\)
\(\Rightarrow m_H=m_X-m_C=2,72-0,19.22=0,44\left(g\right)\Rightarrow n_H=0,44\left(mol\right)\)
Do vậy 2 hidrocacbon thuộc dãy đồng đẳng ankan.
\(\Rightarrow n_X=n_{H2O}-n_{CO2}=0,22-0,19=0,03\left(mol\right)\)
\(\Rightarrow\overline{C_X}=\frac{0,19}{0,03}=6,333\)
Vì 2 hidrocacbon hơn kém nhau 2 C nên có 2 trường hợp xảy ra
TH1: 2 hidrocacbon là C5H12; C7H14 với số mol lần lượt là x, y.
\(\Rightarrow\left\{{}\begin{matrix}x+y=0,03\\5x+7y=0,19\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,01\\y=0,02\end{matrix}\right.\)
\(\Rightarrow m_{C5H12}=0,01.\left(12.5+12\right)=0,72\left(g\right)\)
\(\Rightarrow\%m_{C5H12}=\frac{0,72}{2,72}=26,5\%\)
\(\Rightarrow\%m_{C7H16}=100\%-26,5\%=73,5\%\)
TH2: 2 hidrocacbon là C6H14; C8H18 với số mol lần lượt là x, y
\(\Rightarrow\left\{{}\begin{matrix}x+y=0,03\\6x+8y=0,19\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,025\\y=0,005\end{matrix}\right.\)
\(\Rightarrow m_{C6H14}=0,025.\left(12.6+14\right)=2,15\left(g\right)\)
\(\Rightarrow\%m_{C6H14}=\frac{2,15}{2,72}=79\%\)
\(\Rightarrow\%m_{C8H18}=100\%-79\%=21\%\)