

Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



– Xác định các chất:
A là NaOH; B là Na2CO3; D là NaHCO3; M là NaAlO2; N là Al(OH)3;
P là Ba(HCO3)2; R là BaSO4; Q là BaCO3; Y là NaHSO4; X là CO2
– Các phương trình phản ứng:
2NaOH + CO2 → Na2CO3 + H2O
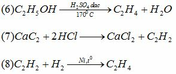
Na2CO3 + CO2 + H2O →2NaHCO3
2NaHCO3 →Na2CO3 + CO2 + H2O
NaOH + Al + H2O → NaAlO2 + 3/2H2
NaAlO2 + CO2 + 2H2O → NaHCO3 + Al(OH)3
3Na2CO3 + 2AlCl3 + 3H2O →6NaCl + 3CO2 + Al(OH)3
2NaHCO3 + Ba(OH)2 → Na2CO3 + BaCO3 + 2H2O
BaCO3 + 2NaHSO4 →BaSO4 + CO2 + Na2SO4 + H2O
Ba(HCO3)2 + 2NaHSO4 →BaSO4 + 2CO2 + Na2SO4 + 2H2O
Ba(HCO3)2 + Na2SO4 →BaSO4 + 2NaHCO3

%Na = 39,316% => MZ = 58,5
=> Z là NaCl
=> X là H2 và Y là HCl
Pt: Cl2 + H2 → 2HCl
HCl + NaOH → NaCl + H2O
2NaCl + H2SO4đặc → Na2SO4 + 2HCl
4HCl + MnO2 → MnCl2 + Cl2↑ + 2H2O

H2SO4+2NaOh=Na2SO4+2H2O(1)
Dung dịch sau phản ứng làm đổi màu quỳ tím thành đỏ =>axit H2SO4 dư
2KOH+H2SO4=K2SO4+2H2O(2)
nH2SO4=0,05.1=0,05 mol
nKOH=0,02.0,5=0,01 mol
Theo PTHH nH2SO4 (2)=0,01/2=0,005 mol (đây là lượng h2so4 dư )
nH2SO4 tham gia phản ứng ở PT (1)=0,05-0,005=0,045 mol
---->nNaOH=0,045 mol
CM=0,045/0,06=0,75 M

Để biết chất khí đó nặng hơn hay nhẹ hơn không khí thì dùng tỉ khối:
\(\frac{d_{\text{chất}}}{d_{kk}}\)
a/Từ đó tìm được các chất nặng hơn không khí là : CO2 , O2 , SO2
b/ Các chất nhẹ hơn không khí là H2 , N2
c/ Các chất cháy được trong không khí là H2 , SO2
d/ Tác dụng với nước tạo thành dung dịch Axit : CO2 , SO2
e/ Làm đục nước vôi trong : CO2 , SO2
g/ Đổi màu giấy quỳ tím ẩm thành đỏ : CO2 , SO2
khoan sao O2 ko cháy đc trong kk. chẳng phải đk để có sự cháy là O2 ak?

\(n_{MgCO3}=\dfrac{8,4}{84}=0,1\left(mol\right)\)
a) Pt : \(2CH_3COOH+MgCO_3\rightarrow\left(CH_3COO\right)_2Mg+CO_2+H_2O|\)
2 1 1 1 1
0,2 0,1 0,1 0,1
b) \(n_{CH3COOH}=\dfrac{0,1.2}{1}=0,2\left(mol\right)\)
⇒ \(m_{CH3COOH}=0,2.60=12\left(g\right)\)
\(C_{ddCH3COOH}=\dfrac{12.100}{200}=6\)0/0
\(n_{\left(CH3COO\right)2Mg}=\dfrac{0,1.1}{1}=0,1\left(mol\right)\)
⇒ \(m_{\left(CH3COO\right)2Mg}=0,1.142=14,2\left(g\right)\)
\(m_{ddspu}=8,4+200-\left(0,1.44\right)=204\left(g\right)\)
\(C_{dd\left(CH3COO\right)2Mg}=\dfrac{14,2.100}{204}=6,96\)0/0
Chúc bạn học tốt

a) X là Cl2
Z là hợp chất 2 nguyên tố, Z là muối của Kali trong đó chiếm 52,35% về khối lượng => Z là KCl
Y là hợp chất 2 nguyên tố, trong đó có chứa Clo, dd Y làm quỳ tím chuyển sang màu đỏ => Y là axit => Y là HCl
Đất đèn +HCl → F => F là C2H2
Ta có sơ đồ sau:
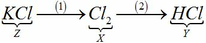

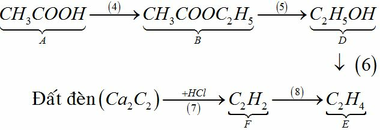
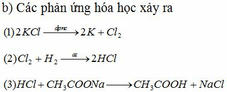
4 C H 3 C O O N a + C 2 H 5 O H ↔ H 2 S O 4 , t ∘ C H 3 C O O C 2 H 5 + H 2 O 5 C H 3 C O O C 2 H 5 + N a O H → C H 3 C O O N a + C 2 H 5 O H

\(H_2SO_4+2NaOH\rightarrow Na_2SO_4+H_2O\)
\(a\) \(2a\)
\(H_2SO_4+2KOH\rightarrow K_2SO_4+H_2O\)
\(b\) \(2b\)
Sau pư (1) đổi màu quỳ tìm \(\Rightarrow H_2SO_4\) dư \(n_{KON}=0,02.0,5=0,01\left(mol\right)\)
\(\rightarrow n_{H_2SO_4dư}=\frac{1}{2}n_{KOU}=5.10^{-3}\left(MOL\right)\)
\(\rightarrow n_{H_2O_4\text{ban đầu }}=0,05.1=0,05\left(mol\right)\)
\(\rightarrow n_{H_2SO_4\left(\text{pư 1 }\right)}=0,05-5.10^{-3}=0,045\left(mol\right)\)
\(\rightarrow n_{NaOH}=0,045.2=0,09\left(mol\right)\)
\(\rightarrow CM_{NaOH}=\frac{0,09}{0,05}=1,8\left(M\right)\)

- Trích mẫu thử.
- Nhỏ vài giọt từng mẫu thử vào quỳ tím.
+ Quỳ hóa xanh: Ba(OH)2, NaOH. (1)
+ Quỳ không đổi màu: NaCl, Na2SO4. (2)
- Cho mẫu thử nhóm (1) và (2) pư với nhau.
+ Có tủa trắng: nhóm (1) là Ba(OH)2, nhóm (2) là Na2SO4.
+ Không hiện tượng: còn lại.
- Dán nhãn.