Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

khi cho Fe vào HCl tạo Fe2+
áp dụng định luật bảo toàn e ta có:
Fe => Fe2+ + 2e 2H+ +2e => H2
nFe = 0,05 mol => mFe=2,8 g => mFe2O3 =7,2g => nFe2O3=0,045 mol
nói chung khi nung kết tủa trong không khí đều tạo Fe2O3 => m (chất rắn)= 7,6 g

Đáp án C
quan sát 4 đáp án: a ≤ 0,029 mol → nếu Cu bị đẩy ra hết thì mCu ≤ 0,029 × 64 = 1,856 < 3,72
||→ chứng tỏ Z chứa Cu và Fe (Cu trong dung dịch bị đẩy ra hết). Rõ hơn, quan sát sơ đồ quá trình sau:
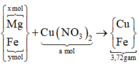
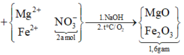
Gọi nMg = x mol và nFe ban đầu = y mol → có ngay 24x + 56y = 3,28 gam.
Trong dung dịch Y bảo toàn điện tích có nFe2+ = (a – x) mol ||→ 1,6 = 40x + 80 × (a – x) ⇄ 80a – 40x = 1,6.
Bảo toàn nguyên tố Fe có trong 3,72 gam gồm a mol Cu và nFe = (x + y – a) mol.
||→ 56 × (x + y – a) + 64a = 3,72 ⇄ 56x + 56y + 8a = 3,72.
Giải hệ 3 ẩn 3 phương trình trên được x ≈ 0,008 mol; y = 0,055 mol và a = 0,024 mol.
||→ theo yêu cầu, đáp án cần chọn là C.

Đáp án C
quan sát 4 đáp án: a ≤ 0,029 mol → nếu Cu bị đẩy ra hết thì mCu ≤ 0,029 × 64 = 1,856 < 3,72
||→ chứng tỏ Z chứa Cu và Fe (Cu trong dung dịch bị đẩy ra hết). Rõ hơn, quan sát sơ đồ quá trình sau:
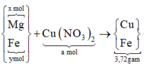
Gọi nMg = x mol và nFe ban đầu = y mol → có ngay 24x + 56y = 3,28 gam.
Trong dung dịch Y bảo toàn điện tích có nFe2+ = (a – x) mol ||→ 1,6 = 40x + 80 × (a – x) ⇄ 80a – 40x = 1,6.
Bảo toàn nguyên tố Fe có trong 3,72 gam gồm a mol Cu và nFe = (x + y – a) mol.
||→ 56 × (x + y – a) + 64a = 3,72 ⇄ 56x + 56y + 8a = 3,72.
Giải hệ 3 ẩn 3 phương trình trên được x ≈ 0,008 mol; y = 0,055 mol và a = 0,024 mol.
||→ theo yêu cầu, đáp án cần chọn là C.

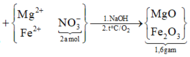
Cách 1: Trước hết ta tóm tắt sơ đồ phản ứng để dễ dàng nắm bắt nội dung của bài toán:
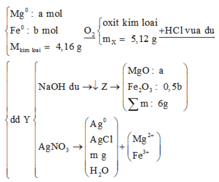
+ Bảo toàn nguyên tố Mg: nMgO = nMg = a mol
+ Bảo toàn nguyên tố Fe:
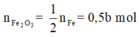
Bây giờ ta đi tìm a, b.
+ Từ đó ta có hệ:
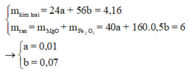
+ Bảo toàn khối lượng: mO(X) = 5,92 - 4,16 = 1,76 g
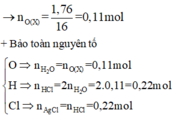
+ Như vậy ta có: mkết tủa =mAg + mAgCl , mà đã có được nAgCl, nên công việc của ta là đi tính khối lượng Ag.
Để tính được Ag, ta cần phải xác định được các trạng thái số oxi hóa của các nguyên tố có sự thay đổi số oxi hóa là Mg, Fe, O và Ag, dựa vào sơ đồ phản ứng ở trên ta dễ dàng tính được mAg.
+ Bảo toàn electron ta có các quá trình
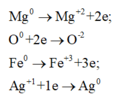
+ Do đó 2nMg + 3nFe = 2nO(X) + nAg
⇒2.0,01+ 3.0,07 = 2.0,11+nAg ⟹nAg =0,01 mol
Suy ra mkết tủa = mAg +mAgCl =0,01.108 + 0,22.143,5 = 32,65 g
Cách 2: Ta sẽ không cần tìm a, b như trên, thay vào đó ta sẽ sử dụng giả thiết “hỗn hợp X chỉ gồm các oxit” :
+ Nung Z trong không khí được 6 gam chất rắn là Fe2O3.
+ Bảo toàn khối lượng: mO(X) = 5,92 - 4,16 = 1,76 g
+ Bảo toàn nguyên tố:
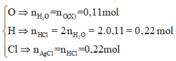
+ Tương tự như trên ta cần phải tính được nAg, dễ thấy 6 g rắn khi nung Z > mX(5,92)
⇒ Trong X phải có FeO, vì “hỗn hợp X chỉ gồm các oxit” nên ta coi X chỉ gồm 2 oxit là FeO và Fe2O3.
Do đó khối lượng O dùng để oxi hóa Fe2+ trong X thành Fe3+ là:
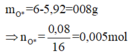
+ Như vậy bảo toàn electron, thì số mol:
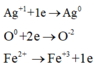
+ Nên nAg = nFe2+ = 2nO = 2.0,005 = 0,01 mol
⇒ m↓ = mAg +mAgCl =0,01.108 + 0,22.143,5 = 32,65 g
Đáp án A

nO/X = (5,92 – 4,16) ÷ 16 = 0,11 mol
[O] + 2HCl → 2Cl + H2O ⇒ nCl– = 2nO = 0,22 mol.
Đặt nMg = x; nFe = y ⇒ 24x + 56y = 4,16(g).
Rắn gồm x mol MgO và 0,5y mol Fe2O3
⇒ 40x + 160.0,5y = 6(g)
⇒ giải hệ có: x = 0,01 mol; y = 0,07 mol.
Bảo toàn electron cả quá trình:
2nMg + 3nFe = 2nO + nAg ⇒ nAg = 2 × 0,01 + 3 × 0,07 - 2 × 0,11 = 0,01 mol.
► Kết tủa gồm 0,01 mol Ag và 0,22 mol AgCl
⇒ m = 0,01 × 108 + 0,22 × 143,5 = 32,65(g).
Đáp án C