Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi số mol của Cu là a => nAl= 2a, nMg= 3a
mCu+mAl+mMg = 19 => a=0,1 =>nCu=0,1(mol);nAl=0,2(mol);nMg=0,3(mol)
dY/H2 =18,5 => M(Y)= 37 (dùng pp đường chéo) => nNO=nN2O
n(Y)= \(\dfrac{4,48}{22,4}\) =0,2 (mol)
Suy ra: nNO=nN2O= 0,1 (mol)
nNH4NO3 =\(\dfrac{\text{0,1.2+0,2.3+0,3.2−0,1.3−0,1.8 }}{8}\)=0,0375 (mol) bảo toàn e nhe
mm′ = mCu(NO3)2+ mAl(NO3)3 +mMg(NO3)2+mNH4NO3 = 108,8(g) ( khúc này bảo toàn nguyên tố Cu,Al,Mg => số mol của muối Cu2+,Al3+,Mg2+ )

Đáp án A
Fe+6 HNO3 đặc → Fe(NO3)3+ 3NO2+3 H2O
Cu+ 4HNO3→ Cu(NO3)2+ 2NO2+2 H2O
Đặt nFe= xmol; nCu= y mol
Ta có mhhX= 56x+ 64y= 12,0
Số mol khí NO2 là nNO2= 3x+ 2y= 0,5 mol
Giải hệ có x= 0,1; y=0,1 → %mFe=46,67%

Gọi \(\left\{{}\begin{matrix}n_{NO}=a\left(mol\right)\\n_{NO_2}=b\left(mol\right)\end{matrix}\right.\) \(\Rightarrow a+b=\dfrac{4,928}{22,4}=0,22\left(mol\right)\) (1)
Ta có: \(n_{Cu}=\dfrac{8,32}{64}=0,13\left(mol\right)\)
Bảo toàn electron: \(2n_{Cu}=n_{NO_2}+3n_{NO}\) \(\Rightarrow3a+b=0,26\) (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}a=0,02\\b=0,2\end{matrix}\right.\) \(\Rightarrow n_{HNO_3}=4n_{NO}+2n_{NO_2}=0,48\left(mol\right)\)
\(\Rightarrow C_{M_{HNO_3}}=\dfrac{0,48}{3}=0,16\left(M\right)\)
Ta thấy trong 4,928 lít hh có 0,02 mol NO và 0,2 mol NO2
\(\Rightarrow\) Trong 1 lít hh sẽ có 0,1 lít NO và 0,9 lít NO2
\(\Rightarrow m_{hh.khí}=\dfrac{0,1}{22,4}\cdot30+\dfrac{0,9}{22,4}\cdot46\approx1,98\left(g\right)\)

Ta đặt: nNO= x mol; nNO2= y mol
Ta có : nY= x+y= 6,72/22,4= 0,3 mol
mY= 30x+ 46y= nY.MY= 0,3.19.2
Giải hệ có x= 0,15 và y= 0,15
Đặt nFe= a mol ; nCu= b mol
QT cho e:
Fe → Fe3++ 3e
a 3a mol
Cu → Cu2++ 2e
b 2b mol
QT nhận e:
N+5+ 3e→ NO
0,45 0,15
N+5+ 1e→ NO2
0,15 0,15
Theo ĐL bảo toàn e có: ne cho= ne nhận nên 3a+2b= 0,45+ 0,15= 0,60
Mặt khác mkim loại= 56a+ 64b= 15,2
Giải hệ trên có a= 0,1, b= 0,15 →%mFe=36,84%
Đáp án C

Gọi \(\left\{{}\begin{matrix}n_{NO_2}=x\left(mol\right)\\n_{NO}=y\left(mol\right)\end{matrix}\right.\)
\(n_{hhkhí}=\dfrac{4,48}{22,4}=0,2mol\) \(\Rightarrow x+y=0,2\left(1\right)\)
\(d_{\dfrac{khí}{H_2}}=18,2\Rightarrow M_{khí}=18,2\cdot2=36,4\)
Sơ đồ chéo: \(NO_2:46\) 6,4
36,4
\(NO:30\) 9,6
\(\Rightarrow\dfrac{x}{y}=\dfrac{6,4}{9,6}=\dfrac{2}{3}\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{NO_2}=x=0,08mol\\n_{NO}=y=0,12mol\end{matrix}\right.\)
\(\underrightarrow{BTe:}\) \(3n_{Fe}=n_{NO_2}+3n_{NO}=0,08+3\cdot0,12=0,44mol\)
\(\Rightarrow n_{Fe}=\dfrac{11}{75}mol\Rightarrow m_{Fe}=\dfrac{616}{75}\left(g\right)\)
\(m_{muối}=m_{Fe}+62n\left(e\right)=\dfrac{616}{75}+62\cdot\left(0,08+0,12\cdot3\right)=35,5\left(g\right)\)
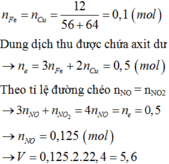
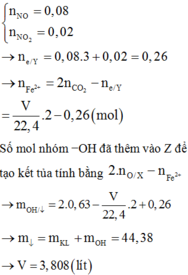

n khí = 0,6 mol
nNO 30 5,34
40,66
nNO2 46 10,66
=> nNO / nNO2 = 1/2
=> nNO = 0,2 nNO2 = 0,4
5Cu + 16HNO3 => 5Cu(NO3)2 + 2 NO + 4NO2 + 8H2O
0,5 <= 0,2
=> m = 0,5.64 = 32 g