Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

=
= 0,5 (mol) =>
= 1 mol
mmuối = mkim loại + mgốc axit = 20 + 35,5 = 55,5 (gam)
Chọn B

\(n_{H_2}=\dfrac{1}{2}=0,5\left(mol\right)\)
Bảo toàn H: nHCl = 1(mol)
Theo ĐLBTKL: mhh KL + mHCl = mhh muối + mH2
=> mhh muối = 20 + 36,5.1 - 1 = 55,5 (g)
=> B

Hoà tan hoàn toàn 20 gam hỗn hợp Fe và Mg trong dung dịch HCI thu được 1 gam khí H2. Khi cô cạn dung dịch thu được bao nhiêu gam muối khan?
A. 54,5 gam. B. 55,5 gam. C. 56,5 gam. D. 57,5 gam.

Áp dụng định luật bảo toàn khối lượng ta có:
\(m=m_{ACl_n}+m_{BCl_m}=m_{A+B}+m_{HCl}-m_{H_2}\)
Áp dụng bảo toàn nguyên tố:
nHCl phản ứng = 2nH2 = 0,2 mol
Ta có m = 10 + 0,2 x 36,5 - 0,2 = 17,1 (g)
Chọn đáp án B

Đáp án C
Bảo toàn nguyên tố Hidro và Clo: nCl– = nHCl = 2nH2 = 1 mol.
⇒ mmuối khan = mkim loại + mCl– = 20 + 1 × 35,5 = 55,5(g)

Bảo toàn nguyên tố Hidro và Clo: nCl– = nHCl = 2nH2 = 1 mol.
⇒ mmuối khan = mkim loại + mCl– = 20 + 1 × 35,5 = 55,5(g)
Đáp án C

A. 184,1 gam và 91,8 gam.
B. 84,9 gam và 91,8 gam.
C. 184,1 gam và 177,9 gam.
D. 84,9 gam và 86,1 gam.

Giải thích: Đáp án C
nH2=0,5 mol=>nHCl pư=nCl-=1 mol
=> m muối=mKL+mCl-=20+35,5=55,5 gam
Đáp án B.
• Cách 1:
gọi x, y lần lượt là số mol của Fe và Mg trong hỗn hợp
số mol H2 là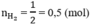
theo bài ra ta có hệ phương trình
khối lượng muối khan là :
m = mFeCl2 + mMgCl2 = x(56 + 71) + y(24 + 71)
m = 56x + 24y + 71(x + y)
m = 20 + 71.0,5 = 55,5(g)
• Cách 2:
nmuối =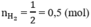
Khối lượng muối = m(kim loại) + m(gốc clorua) = 20,0 + 71. 0,5 = 55,5 (g)