Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Số mol H2 là nH2 = 0,6/2 = 0,3(mol)
PTHH : Mg + 2HCl → MgCl2 + H2 ↑ (1)
Zn + 2HCl → ZnCl2 + H2 ↑ (2)
Gọi x, y lần lượt là số mol của Mg và Zn trong dung dịch x, y > 0
nH2 = x + y = 0,3 mol.
mhh = 24x + 65y = 15,4.
Khối lượng muối là m = x(24 + 71) + y(65 + 71)
m = 24x + 65y + 71(x + y) = 15,4 + 71.0,3 = 36,7 (g)

\(Đặt:n_{Mg}=a\left(mol\right),n_{Zn}=b\left(mol\right)\left(a,b>0\right)\\ Mg+2HCl\rightarrow MgCl_2+H_2\\ Zn+2HCl\rightarrow ZnCl_2+H_2\\ \Rightarrow\left\{{}\begin{matrix}24a+65b=15,4\\2a+2b=0,6\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,1\\b=0,2\end{matrix}\right.\\ m_{muối}=m_{MgCl_2}+m_{ZnCl_2}=95a+136b=36,7\left(g\right)\\ \Rightarrow A\)

Đáp án D
nCl- = 2nH2 = 2.0,3= 0,6 mol
mMuối = mKL = mCl- = 15,4 + 0,3.96 =36,7 g

=
= 0,5 (mol) =>
= 1 mol
mmuối = mkim loại + mgốc axit = 20 + 35,5 = 55,5 (gam)
Chọn B

3.NO2 nhé
nNO2= 0,06 mol
PTHH:
Cu + 4HNO3→ Cu(NO3)2 + 2NO2+ 2H2O
x__________________________2x
Al+ 6HNO3→ Al(NO3)3+3NO2+3H2O
y______________________3y
Giải HPT:
\(\left\{{}\begin{matrix}64x+27y=1,23\\2x+3y=0,06\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=,015\\y=0,01\end{matrix}\right.\)
%Cu=\(\frac{0,015.64}{1,23}\text{.100%=78,048 %}\)
1.
Gọi số mol Mg và Al là a và b
nH2=0,4
Mg+2HCl\(\rightarrow\)MgCl2+H2
2Al+6HCl\(\rightarrow\)2AlCl3+3H2
Giải HPT:\(\left\{{}\begin{matrix}\text{ 24a+27b=7,8}\\\text{a+1,5b=0,4}\end{matrix}\right.\rightarrow\left\{{}\begin{matrix}a=0,1\\b=0,2\end{matrix}\right.\)
\(\rightarrow\)%mMg=\(\frac{0,1.24}{7,8}\)=30,77%
2.
Gọi số mol Zn, Al là a và b
3Zn+8HNO3\(\rightarrow\)3Zn(NO3)2+2NO+4H2O
Al+4HNO3\(\rightarrow\)Al(NO3)3+NO+2H2O
nNO=0,4
Giải HPT:
\(\left\{{}\begin{matrix}\text{65a+27b=11,9}\\\frac{2a}{3}\text{+b=0,4}\end{matrix}\right.\rightarrow\left\{{}\begin{matrix}a=\frac{11}{470}\\\frac{271}{705}\end{matrix}\right.\)
\(\rightarrow\)%mZn=\(\frac{65.\frac{11}{470}}{11,9}\)=12,78%

a) nH2= 0,45(mol)
PTHH: Mg +2 HCl -> MgCl2+ H2
Fe +2 HCl -> FeCl2 + H2
-> nHCl=nCl- = 2.nH2=0,9(mol)
=> m(muối)= mCl- + m(Mg,Fe)= 0,9.35,5+ 23,1=55,05(g)

Áp dụng định luật bảo toàn khối lượng ta có:
\(m=m_{ACl_n}+m_{BCl_m}=m_{A+B}+m_{HCl}-m_{H_2}\)
Áp dụng bảo toàn nguyên tố:
nHCl phản ứng = 2nH2 = 0,2 mol
Ta có m = 10 + 0,2 x 36,5 - 0,2 = 17,1 (g)
Chọn đáp án B
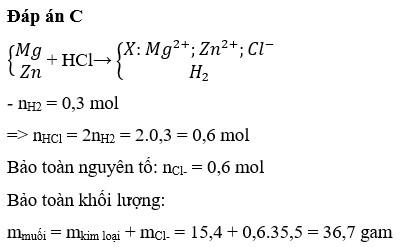
Chọn A
Gọi công thức chung của Mg và Zn là M
M + 2HCl → MCl2 +H2
Áp dụng định luật bảo toàn khối lượng ta có:
mkim loại + mHCl = mmuối +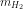
=> mmuối = 15,4 + 0,6.36,5 - 0,6 = 36,7 (gam)
Hòa tan hoàn toàn 15,4 gam hỗn hợp Mg và Zn trong dung dịch HCl dư thấy có 0,6 gam khí H2 bay ra. Khối lượng muối tạo ra trong dung dịch là
A. 36,7 gam
B. 35,7 gam
C. 63,7 gam
D. 53,7 gam