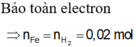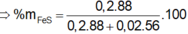Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Bài này ta phải nhìn kỹ vào PTHH và biết vận dụng ĐLBTKL :)
\(n_{CO_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH:
\(MgCO_3+2HCl\rightarrow MgCl_2+CO_2\uparrow+H_2O\left(1\right)\\ CaCO_3+2HCl\rightarrow CaCl_2+CO_2\uparrow+H_2O\left(2\right)\\ Na_2CO_3+2HCl\rightarrow2NaCl+CO_2\uparrow+H_2O\left(3\right)\)
Theo pthh (1, 2, 3): \(\left\{{}\begin{matrix}n_{H_2O}=n_{CO_2}=0,2\left(mol\right)\\n_{HCl}=2n_{CO_2}=2.0,2=0,4\left(mol\right)\end{matrix}\right.\)
Áp dụng ĐLBTKL:
\(m_{muối.cacbonat}+m_{HCl}=m_{muối.clorua}+m_{CO_2}+m_{H_2O}\)
=> x = mmuối clorua = 18,7 + 0,4.36,5 - 0,2.44 - 0,2.18 = 20,9 (g)

Câu 1 :\(n_{CO_2} = \dfrac{2,688}{22,4} = 0,12(mol)\)
MgCO3 + 2HCl \(\to\) MgCl2 + CO2 + H2O
..................................0,12........0,12..................(mol)
Suy ra: a = 0,12.95 = 11,4(gam)
Câu 2 :
\(Fe + 2HCl \to FeCl_2 + H_2\\ n_{Fe} = n_{H_2} = \dfrac{3,36}{22,4} = 0,15(mol)\\ \Rightarrow n_{Cu} = 2n_{Fe} = 0,15.2 = 0,3(mol)\\ 2Fe+3Cl_2\xrightarrow{t^o} 2FeCl_3\\ Cu+Cl_2 \xrightarrow{t^o} CuCl_2\\ n_{Cl_2} = \dfrac{3}{2}n_{Fe} + n_{Cu} = 0,525\\ \Rightarrow V = 0,525.22,4 =11,76(lít)\)

\(n_{HCl} = \dfrac{448.1,12.3,65\%}{36,5} = 0,50176(mol)\\ Zn + 2HCl \to ZnCl_2 + H_2\\ ZnO + 2HCl \to ZnCl_2 + H_2O\\ n_{Zn} = n_{H_2} = \dfrac{2,24}{22,4} = 0,1(mol)\\ n_{ZnO} = \dfrac{n_{HCl} - 2n_{Zn}}{2} = \dfrac{0,50176-0,1.2}{2} = 0,15088(mol)\\ \%m_{Zn} = \dfrac{0,1.65}{0,1.65 + 0,15088.81}.100\% = 34,72\%\\ \%m_{ZnO} = 65,28\%\)

\(Đặt:nMg=a\left(mol\right),n_{MgCO_3}=b\left(mol\right)\)
\(n_{khí}=\dfrac{6.72}{22.4}=0.3\left(mol\right)\)
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
\(a................a.......a\)
\(MgCO_3+2HCl\rightarrow MgCl_2+CO_2+H_2O\)
\(b....................b........b\)
\(m_X=24a+84b=13.2\left(g\right)\left(1\right)\)
\(n_{khí}=a+b=0.3\left(mol\right)\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.2,b=0.1\)
\(m_{Mg}=0.2\cdot24=4.8\left(g\right),m_{MgCO_3}=0.1\cdot84=8.4\left(g\right)\)
\(m_{ddB}=13.2+200-0.2\cdot2-0.1\cdot44=208.4\left(g\right)\)
\(m_{MgCl_2}=0.3\cdot95=28.5\left(g\right)\)
\(C\%MgCl_2=\dfrac{28.5}{208.4}\cdot100\%=13.67\%\)

Câu 1.1 :
$Ca(OH)_2 + CO_2 \to CaCO_3 + H_2O$
n CO2 = n CaCO3 = 7/100 = 0,07(mol)
$CO + O_{oxit} \to CO_2$
n O(oxit) = n CO2 = 0,07(mol)
=> m kim loại = 4,06 -0,07.16 = 2,94(gam)
Gọi kim loại là R ; n H2 = 1,176/22,4 = 0,0525(mol)
$2R + 2n HCl \to 2RCl_n + nH_2$
n R = 2/n n H2 = 0,105/n(mol)
=> R.0,105/n = 2,94
=> R = 28n
Với n = 2 thì R = 56(Fe)
n Fe = 2,94/56 = 0,0525(mol)
Ta có :
n Fe / n O = 0,0525 / 0,07 = 3/4
Vậy CT oxit là Fe3O4
Ta có :
n Al2(SO4)3 = 273,75.21,863%/342 = 0,175(mol)
Bảo toàn nguyên tố S :
n H2SO4 = 3n Al2(SO4)3 = 0,525(mol)
n H2 = 5,04/22,4 = 0,225(mol)
Bảo toàn nguyên tố H :
n H2SO4 = n H2 + n H2O
=> n H2O = 0,525 - 0,225 = 0,3(mol)
Bảo toàn khối lượng :
m + 0,525.98 = 273,75.21,863% + 0,225.2 + 0,3.18
=> m =14,25(gam)

\(n_{H_2}=\dfrac{3.36}{22.4}=0.15\left(mol\right)\)
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
\(0.15.....0.3.......................0.15\)
\(m_{Mg}=0.15\cdot24=3.6\left(g\right)\)
\(m_{Cu}=10-3.6=6.4\left(g\right)\)
\(\%Mg=\dfrac{3.6}{10}\cdot100\%36\%\)
\(\%Cu=64\%\)
\(V_{dd_{HCl}}=\dfrac{0.3}{2}=0.15\left(l\right)\)

a.
Do E gồm hai oxit nên Mg, CuCl2 hết, Fe đã phản ứng
Phương trình
Mg + CuCl2 \(\rightarrow\) MgCl2 + Cu (1)
Fe + CuCl2 \(\rightarrow\) FeCl2 + Cu (2)
Khi cho NaOH dư vào
2NaOH + MgCl2 \(\rightarrow\) Mg(OH)2 + 2NaCl (3)
2NaOH + FeCl2 \(\rightarrow\) Fe(OH)2 + 2NaCl (4)
Khi nung
Mg(OH)2 \(\underrightarrow{t^o}\) MgO + H2O (5)
4Fe(OH)2 +O2 \(\underrightarrow{t^o}\) 4Fe2O3 + 4H2O (6)
b.
Đặt số mol của Fe, Mg có ban đầu lần lượt là x, y, số mol Fe dư là t (x, y>0, t\(\ge\)0)
Có hệ \(\begin{cases}24x+56y+0t=3,16\\40x+64y-8t=3,84\\40x+80y-80t=1,4\end{cases}\)\(\Rightarrow\)\(\begin{cases}x=0,015mol\\y=0,05mol\\t=0,04mol\end{cases}\)
Vậy trong hỗn hợp đầu %mMg = \(\frac{0,015.24}{3,16}.100\)=11,392%
%mFe=100%-11,392% = 88,608%
Nồng độ của CuCl2: z =0,025:0,25=0,1M

\(n_{H_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\\ PTHH:2Al+6HCl\rightarrow2AlCl_3+3H_2\\ Fe+2HCl\rightarrow FeCl_2+3H_2\\ Đặt:n_{Al}=a\left(mol\right);n_{Fe}=b\left(mol\right)\left(a,b>0\right)\\ \Rightarrow\left\{{}\begin{matrix}27a+56b=11\\1,5a+b=0,4\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,2\\b=0,1\end{matrix}\right.\\ a,n_{HCl}=2.n_{H_2}=2.0,4=0,8\left(mol\right)\\ \Rightarrow V_{ddHCl}=\dfrac{0,8}{8}=0,1\left(l\right)\\ b,FeCl_2+2AgNO_3\rightarrow Fe\left(NO_3\right)_2+2AgCl\downarrow\\ AlCl_3+3AgNO_3\rightarrow Al\left(NO_3\right)_3+3AgCl\downarrow\\ n_{AgCl}=n_{AgNO_3}=3.n_{AlCl_3}+2.n_{FeCl_2}=3.a+2.b=3.0,2+2.0,1=0,8\left(mol\right)\\ \Rightarrow a=\dfrac{170.0,8}{250}.100=54,4\%\\ b=m_{\downarrow}=m_{AgCl}=0,8.143,5=114,8\left(g\right)\)