Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

MgCO3 + 2HCl → MgCl2 + CO2 + H2O (1)
BaCO3 + 2HCl → BaCl2 + CO2 + H2O (2)
CO2 + Ca(OH)2 → CaCO3↓ + H2O. (3)
Theo (1), (2) và (3), để lượng kết tủa B thu được là lớn nhất thì:
nCO2 = nMgCO3 + nBaCO3 = 0,2 mol
Ta có:  = 0,2
= 0,2
=> a = 29,89.

Số mol H3PO4: 0,050 x 0,50 = 0,025 (mol).
H3PO4 + 3NaOH → Na3PO4 + 3H2O
1 mol 3 mol
0,025 mol 3 x 0,025 mol
Thể tích dung dịch NaOH: 0,075 lít hay 75 ml

b)
= 10 (gam)
=> phản ứng =
= 0,01 (mol)
Cu + 2AgNO3 → Cu(NO3)2 + 2Ag
0,005 0,01 0,01 (mol)
Khối lượng của vật sau phản ứng là:
10 + 108.0,01 - 64.0,005 = 10,76 (gam)

Bạn chú ý, gửi từng câu hỏi một, không nên gửi nhiều câu hỏi một lúc
Câu 1.
Bài này có thể gọi M là kim loại chung của 3 kim loại trên:
M + HNO3 ---> M(NO3)n + NO + N2O + H2O (chú ý với bài tính toán kiểu này ko cần cân bằng pt).
Ta có số mol HNO3 = 1,5.0,95 = 1,425 mol.
Ta có khối lượng của hh khí (NO và N2O) = 16,4.2.số mol = 16,4.2.0,25 = 8,2 gam.
Áp dụng ĐLBTKL ta có: 29 + 63.1,425 = m + 8,2 + 18.0,7125 (chú ý số mol H2O luôn bằng 1/2 số mol HNO3).
Tính ra m = 97,75 g

Chọn D
Gọi số mol của CuSO4 và NaCl lần lượt là x và 3x (mol)
Thứ tự điện phân các chất tại catot và anot
Tại catot:
Cu2+ +2e → Cu↓
2H2O + 2e → 2OH- + H2
Tại anot:
2Cl- → Cl2 + 2e
2H2O → 4H+ + O2↑ + 4e
Vì nCl- = 3nCu2+ và chất tan thu được hòa tan được Al2O3 => Cl- điện phân hết.
2 chất tan thu được là Na2SO4 : x ( mol) ; NaOH: (3x – 2x) = x (mol)
2NaOH + Al2O3 → 2NaAlO2 + H2O
0,06 ← 0,03 (mol)
=> x = nNaOH = 0,06 (mol)
Tại catot: Cu: 0,06 mol; nH2 = a (mol)
Tại anot: Cl2: 0,09 mol; nO2 = b (mol)
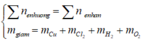
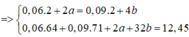
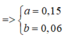
=> ∑ ne = 0,06.2 + 2.0,15 = 0,42 (mol)
Áp dung CT ta có: ne = It/F => t = 0,42.96500/2 = 20265 (s) = 5,63 (giờ)
Gần nhất với 5,6 giờ

Đáp án D
Khí gồm SO2 ; CO2 có n = 0,25 mol và M = 55,2g
=> nSO2 = 0,14 ; nCO2 = 0,11 mol
=> nNa2SO3 = 0,14 ; nCuCO3 = 0,11
Gọi thể tích dung dịch axit là V => nHCl = V ; nH2SO4 = 0,5V mol
=> nH2O =1/2 nH+ = V mol
Bảo toàn khối lượng : mX + maxit = mchất tan + mkhí + mH2O
=> V = 0,33 lit
=> nHCl = 0,33 ; nH2SO4 = 0,165 mol
Bảo toàn điện tích : nNa+ + 2nCu2+ = nCl- + 2nSO4 => nCu2+ = 0,19 mol
=> nCuO = 0,19 – 0,11 = 0,08 mol => m = 37,68g
, nCu2+ đp = 0,19.0,94 = 0,1786 mol
Catot : Cu2+ + 2e -> Cu
Anot : 2Cl- -> Cl2 + 2e
2H2O -> 4H+ + O2 + 4e
=> 2nCu2+ đp = nCl- + nH+ => nH+ = 0,0272 mol
Lấy nFe = 0,0942 mol phản ứng với Z( 0,0272 mol H+ và 0,0114 mol Cu2+)
=> sau phản ứng có : 0,0114 mol Cu và 0,0692 mol Fe dư
=> m1 = 4,6048g
=>D

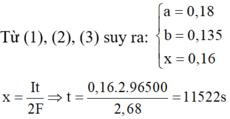

Trong X có : nFe3O4 = 0,03 mol ; nCuO = 0,02 mol
Khi phản ứng với HCl vừa đủ thì trong dung dịch có :
0,02 mol Cu2+ ; 0,03 mol Fe2+ ; 0,06 mol Fe3+ ; 0,28 mol Cl- .
Khi điện phân :
+/ Anot : 2Cl- → Cl2 + 2e
+/ Catot : Fe3+ + 1e → Fe2+ (1)
Cu2+ + 2e → Cu (2)
Fe2+ + 2e → Fe (3)
Nếu dung dịch chỉ giảm khối lượng vì Cl2 bay ra , chỉ xảy ra (1) ở Catot
=> ne trao đổi = 0,06 mol => mCl2 = 2.13g < 11,18g =>Loại
Nếu (10 và (20 xảy ra vừa đủ => ne trao đổi = 0,1 mol
=> mgiảm = mCl2 + mCu = 4,83g < 11,18 =>Loại
Vậy xảy ra cả (1) ; (2) ; (3)
Đặt nFe2+ phản ứng = a mol
=> ne trao đổi = (0,1 + 2a) mol => nCl2 = (0,05 + a) mol
=>mGiảm = 0,02.64 + 56a + 71.(0,05 + a) = 11,18
=> a = 0,05 mol
=>nFe2+ dư = 0,03 + 0,06 – 0,05 = 0,04 mol
Khi phản ứng với KMnO4 tạo MnSO4 ; Fe2+ bị OXH thành Fe3+
Bảo toàn e : nFe2+ = 5nKMnO4 => 0,04 = 5.0,1V
=>V = 0,08 l = 80 ml
=>B