Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Khi hoà tan hợp kim gồm 3 kim loại Fe, Cu và Al trong dung dịch HCl dư thì Cu không tác dụng, khối lượng 1,86 gam là khối ỉượng Cu. Gọi số mol Fe là x mol, Al là y mol.
n Fe = x mol
n Al = y mol
n H 2 = 3,024/22,4 = 0,135
Ta có hệ phương trình
56x + 27y = 6 - 1,86 = 4,14
x + 3/2y = 0,135
=> x = 0,045; y = 0,06
m Fe = 0,045 x 56 = 2,52g; n Al = 0,06 x 27 = 1,62g
Từ đó ta tính được thành phần phần trăm khối lượng các kim loại.

a. Fe + 2HCl => FeCl2 + H2
2Al + 6HCl => 2AlCl3 + 3H2
b. mCu= m kim loại ko tan =1,86
=> mFe + m Al = 6-1,86 =4,14
giải hệ 56x + 27y = 4,14
x + 3y/2 = 0,135
=> x= 0,045 y= 0,06
=> mFe = 2,52 m Al = 1,62
=> %Fe = 42%
%Al= 27%
%Cu = 31%

So sánh các phản ứng của hỗn hợp X với oxi và hỗn hợp Y với dung dịch HCl, ta thấy :
n HCl = 2 n trong oxit ; m O 2 = 8,7 - 6,7 = 2g
n O trong oxit = 0,125 mol; n HCl = 0,25 mol
V HCl = 0,25/2 = 0,125l

\(n_{CuO}=n_{Cu}=\dfrac{4}{80}=0,05mol\\ n_{H_2}=0,4mol\\ n_{Al}=a;n_{Zn}=b\\ 27a+65b=15,1-0,05\cdot64\\ BTe^-:3a+2b=2\cdot0,4\\ a=0,2;b=0,1\\ m_{ddHCl}=\dfrac{\left(0,6+0,2\right)\cdot36,5}{0,2}=146g\)

Phương trình hoá học của phản ứng :
Ag không tác dụng với oxi, không tác dụng với dung dịch HCl nên 2,7 garn chất rắn không tan là Ag.
Hỗn hợp kim loại với oxi.
4Al + 3 O 2 → 2 Al 2 O 3
3Fe + 2 O 2 → Fe 3 O 4
2Cu + O 2 → 2CuO
Hỗn hợp chất rắn Y với dung dịch HCl
Al 2 O 3 + 6HCl → 2Al Cl 3 + 3 H 2 O
Fe 3 O 4 + 8HCl → Fe Cl 2 + 2Fe Cl 3 + 4 H 2 O
CuO + 2HCl → Cu Cl 2 + H 2 O

\(n_{H_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
PTHH: Fe + H2SO4 → FeSO4 + H2
Mol: 0,4 0,4
\(m_{Fe}=0,4.56=22,4\left(g\right)\)
\(m_{hh}=22,4+5=27,4\left(g\right)\)
\(\%m_{Fe}=\dfrac{22,4.100\%}{27,4}=81,75\%;\%m_{Cu}=100-81,75=18,25\%\)

Cu không tác dụng với axit HCl , do đó chất không tan là Cu và m Cu = 2,5 (gam).
Khối lượng Al và Mg bằng : 12,7 - 2,5 = 10,2 (gam)
Phương trình hoá học của phản ứng :
2Al + 6HCl → 2 AlCl 3 + 3 H 2
Mg + 2HCl → MgCl 2 + H 2
Theo phương trình hoá học trên và dữ kiện đề bài cho, ta có :
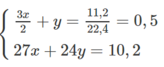
Giải ra, ta có : x = y = 0,2 mol
m Al = 0,2 x 27 = 5,4g
m Mg = 0,2 x 24 = 4,8g
% m Al = 5,4/12,7 .100% = 42,52%
% m Mg = 4,8/12,7 .100% = 37,8%
% m Cu = 100% - 42,52% - 37,8% = 19,68%

\(n_{H_2}=\dfrac{4,928}{22,4}=0,22mol\)
\(n_{CuSO_4}=0,66.0,5=0,33mol\)
- Gọi số mol trong phần I là :Fe(x mol), Al(y mol), Ag(z Mol)
- Sỗ mol mỗi kim loại trong phần II: Fe(tx mol), Al(ty mol), Ag(tz Mol)
56(x+tx)+27(y+ty)+108(z+tz)=24,5(*)
- Phần I: Fe+2HCl\(\rightarrow\)FeCl2+H2(1)
2Al+6HCl\(\rightarrow\)2AlCl3+3H2(2)
x+1,5y=0,22(**)
- Phần II: Fe+CuSO4\(\rightarrow\)FeSO4+Cu(3)
2Al+3CuSO4\(\rightarrow\)Al2(SO4)3+3Cu(4)
tx+1,5ty=0,33(***)
152tx+171ty=39,9(****)
- Kết hợp(***) và(****) : tx=0,06, ty=0,18
\(y=3x\)(*****)
- kết hợp (**) và (*****) ta có: x=0,04, y=0,12
\(\rightarrow t=\dfrac{0,06}{0,04}=1,5\)
- Thay x=0,04 ,y=0,12 , t=1,5 vào (*) ta có z=0,04
mI=56x+27y+108z=56.0,04+27.0,12+108.0,04=9,8 gam
số mol Cu=tx+1,5ty=0,33 mol
chất rắn Z gồm 0,33 mol Cu và tz=0,04.1,5=0,06 mol Ag
mZ=0,33.64+0,06.108=27,6 gam