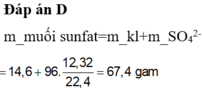Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D.
nSO2 = 0,55 => ne = 0,55.2 = 1,1 (mol)
mmuối = mKL + Mgốc axit. ne/2
= 14,6 + 96. 1,1/2 = 67,4 g

ta có : \(n_{Fe}=\dfrac{m}{M}=\dfrac{8,4}{56}=0,15\left(mol\right)\)
PTHH :
2Fe + 6H2SO4 ( đặc nóng) ----> Fe2(SO4)3 + 6H2O + 3SO2
lại có : theo PT 3nFe= nH2SO4
Theo GT 3nFe > nH2SO4 ( 0,15 . 3 > 0,4 )
=> Fe dư => nFe dư = 0,15 . 3 - 0,4 = 0.05 (mol)
PTHH (2)
Fe + Fe2(SO4)3 ----> 3FeSO4
.0,05.....0,05...................0,15...(mol)
=> \(m_{Fe_2\left(SO_4\right)_3}=n\cdot M=\left(0,4-0,05\right)\cdot400=140\left(g\right)\)
=> \(m_{FeSO_4}=n\cdot M=0,15\cdot152=22,8\left(g\right)\)
=> m gam muối khan = 22,8 + 140 = 162,8 (g)
Đây là hóa 9 mà ( sao ghi 10 ) -.-

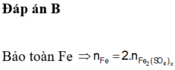
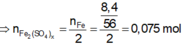
![]()
![]()
![]()
![]()
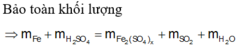
=> 8,4+0,4.98=0,075(56.2+96x)+(0,4-0,075x).64+0,4.18
=> x=8/3
m_muối=0,075(56.2+96.8/3)=27,6 gam
![]()

Câu 1. cho 7,36 gam hỗn hợp X gồm Fe và MgO tác dụng với dung dịch H2SO4 đặc nóng, dư. Sau phản ứng thu được dd Y và 2,016 lít khí SO2 (đktc, sản phẩm khử duy nhất). Tính phần trăm khối lượng từng chất trong hỗn hợp X?
Giải
2Fe + 6H2SO4 đ,n => Fe2(SO4)3 + 3SO2 + 6H2O
MgO + H2SO4 đ,n => MgSO4 + H2O
nSO2 = V/22.4 = 2.016/22.4 = 0.09 (mol)
Theo pt => nFe = n.M = 0.06 (mol)
mFe = n.M = 0.06 x 56 = 3.36 (g)
% m Fe = 3.36x100/7.36 = 45.65 %
% m MgO = 100 - 45.65 = 54.35 %
Câu 2. cho m gam hỗn hợp X gồm Cu và Fe2O3 tác dụng với dd H2SO4 đặc nóng, vừa đủ. Sau phản ứng thu được dd Y và 1,12 lít khí SO2 (đktc, sản phẩm khử duy nhất). Cô cạn dd Y được 20 gam muối khan. Tính giá trị m?
Giải
Cu + 2H2SO4 đ,n => CuSO4 + SO2 + 2H2O
Fe2O3 + 3H2SO4 đ,n = >Fe2(SO4)3 +3H2O
nSO2 = V/22.4 = 1.12/22.4 = 0.05 (mol)
Theo pt => nCuSO4 = 0.05 (mol)
mCuSO4 = 0.05x160 = 8 (g)
=> mFe2(SO4)3 = 20 - 8 = 12 (g)
=> nFe2(SO4)3 = 12/400= 0.03 (mol) = nFe2O3
==> mCu = n.M = 0.05 x 64 = 3.2 (g)
==> mFe2O3 = n.M = 0.03x160 = 4.8 (g)
Vậy m = 3.2 + 4.8 = 8 (g)