Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Độ tan của NaCl :
\(S=\dfrac{90.100}{250}=36\left(g\right)\)

Chọn C.
Dung dịch Y chứa H+ với n H + = 2 n H 2 = 0 , 12 mol ⇒ H + ban đầu: 0 , 12 + 2 n H 2 ⇒ n O 2 = 0 , 03 + 0 , 5 n H 2
Khối lượng dung dịch giảm:
m Cu + m khí = 300 - 283 , 32 = 16 , 68 ⇒ 64 n Cu + 71 n Cl 2 + 18 n H 2 = 15 , 72 (1)
→ BT : e 2 n Cu = 0 , 12 + 2 n Cl 2 (2) và
160 n Cu + 117 n Cl 2 = 31 , 76 (3)
Từ (1), (2), (3) suy ra:
n Cu = 0 , 14 mol ; n Cl 2 = 0 , 08 mol ; n H 2 = 0 , 06 mol ⇒ n O 2 = 0 , 06 mol
Vậy V = 3,136 lít.

Đáp án A
Do chứa muối trung hòa nên dung dịch Y chứa Al3+ a mol, Zn2+ b mol, NH4+ c mol và SO42- 0,585 mol.
Bảo toàn điện tích:3a+2bc=0,585 .2
![]()
![]()
![]()
Hỗn hợp khí Z chứa CO2 x mol, N2 y mol và H2 z mol
![]()
![]()
Bảo toàn nguyên tố N:
n N O 3 - ( x ) 2 y + 0 , 03 - 0 , 09 = 2 y - 0 , 06
Trong X
m N O 3 - + m C O 3 2 - = m x - m k i m l o a i = 8 , 52
![]()
![]()
![]()

Đáp án A
Do chứa muối trung hòa nên dung dịch Y chứa Al3+ a mol, Zn2+ b mol, NH4+ c mol và SO42- 0,585 mol.
Bảo toàn điện tích: 3a + 2b + c = 0,585.2
m m u ố i = 27a + 65b + 18c + 96.0,585 = 79,65
n N a O H = 4a + 4b + c = 1,91
=> a = 0,2; b = 0,27; c = 0,03
Hỗn hợp khí Z chứa CO2 x mol, N2 y mol và H2 z mol
→ n Z = x + y + z = 0,18
n H + = 2x + 12y + 2z + 0,03.10 = 0,585.2 + 0,09
Bảo toàn nguyên tố N: n N O - 3 ( X ) = 2y + 0,03 - 0,09 = 2y - 0,06
Trong X:
![]()
=>62(2y - 0,06) + 60x = 8,52
=> x = 0,08; y = 0,06; z = 0,04 → n Z n = b - x = 0,19
=> %Zn = 39,24%

pV = nRT với p = 1atm; V = 3,813 lít;
R = 0,082; T = 273 + 27 = 300K.
khí hóa nâu ngoài không khí là NO
⇒ thay số có nNO = 0,155 mol.
phản ứng xảy ra hoàn toàn nên Fe sẽ lên Fe3+ trong muối Fe(NO3)3.
Bảo toàn electron có: 3nFe + nFeO = 3nNO = 0,465 mol.
Lại có: mFe + mFeO = 9,48 gam
⇒ giải nFe = 0,15 mol; nFeO = 0,015 mol.
⇒ ∑nFe(NO3)3 = 0,165 mol
⇒ bảo toàn N có ∑nHNO3 cần = 0,65 mol.
⇒ VHNO3 = 0,65 ÷ 0,5 = 1,3 lít = 1300 mL
Đáp án D

Đáp án B
nNaCl = 1mol
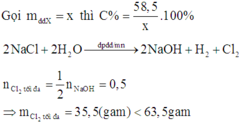
Do đó sau khi NaCl bị điện phân hết thì tiếp tục có sự điện phân nước:
![]()
Khi đó khí thoát ra ở anot gồm có Cl2 và O2
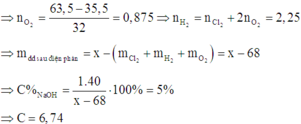

Đáp án C
TH1: Cl- bị đp hết trước Cu2+, H2O ở anot bị điện phân
Al2O3+6H+→2Al3++3H2O
0,2.…1,2
Catot:
Cu2+ + 2e → Cu
Anot:
Cl- -1e → 0,5Cl2
H2O - 2e→0,5O2 + 2H+
0,3 1,2
Ta thấy nO2=0,3 => nCl2 = 0 (vô lí)
TH2: Cu2+ bị điện phân hết trước Cl-, H2O ở catot bị điện phân sinh ra OH-
Al2O3+2OH-→2AlO2-+H2O
0,2…….0,4
Catot:
Cu2+ +2e→Cu
x 2x
H2O+1e→OH-+0,5H2
0,4 0,4
Anot:
Cl- -1e → 0,5Cl2
0,6...0,3
=>2x+0,4=0,6=>x=0,1 mol
=>nCuSO4=0,1 mol; nNaCl=0,6 mol
=>m=0,1.160+0,6.58,5=51,1 gam

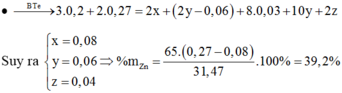

\(n_{NaCl} = \dfrac{0,585}{58,5}=0,01(mol)\\ C_{M_{NaCl}} = \dfrac{0,01}{1}=0,01M\)
Áp suất thẩm thấu : \(P = RTC = 0,082.(273 + 25).0,01 = 0,24436(atm)\)