Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Khối lượng mol của những khí cho:
a) dX/O2 = 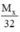 = 1,375 ⇒ MX = 1,375 x 32 = 44 g/mol;
= 1,375 ⇒ MX = 1,375 x 32 = 44 g/mol;
dY/O2 = 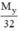 = 0,0625 ⇒ MY = 0,0625 x 32 = 2 g/mol.
= 0,0625 ⇒ MY = 0,0625 x 32 = 2 g/mol.
b) dX/kk = 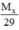 = 2,207 ⇒ MX = 29 x 2,207 = 64 g/mol;
= 2,207 ⇒ MX = 29 x 2,207 = 64 g/mol;
dY/kk = 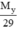 = 1,172 ⇒ MY = 29 x 1,172 = 34 g/mol.
= 1,172 ⇒ MY = 29 x 1,172 = 34 g/mol.

nA = \(\dfrac{11,2}{22,4}\) = 0,5 mol
d \(\dfrac{A}{kk}\) = \(\dfrac{MA}{29}\) = 0,552 \(\Rightarrow\) MA = 29 . 0,552 = 16 (g/mol)
- nC = \(\dfrac{75.16}{100.12}\) = 1 mol
- nH = \(\dfrac{25.16}{100.1}\) = 4 mol
A là CH4
PT : CH4 + O2 -> CO2 + 2H2O
nO2 = 2nCH4 = 2.0,5 = 1 mol
VO2 = 1. 22,4 = 22,4 l
Khối lượng mol khí A tham gia phản ứng là:
dA/kk = 0,552 => MA = 29 . 0,552 = 16 g
mC = = 12; mH =
= 4
Đặt công thức hóa học của khí A là CxHy, ta có:
12 . x = 12 => x = 1
1 . y = 4 => y = 4
Công thức hóa học của khí A là CH4
Phương trình phản ứng
CH4 + 2O2 → CO2 + 2H2O
Theo phương trình phản ứng, thể tích oxi bằng hai lần thể tích khí CH4 nên thể tích khí oxi đủ để đốt cháy hết 11,2 lít khí A là:
= 2 .
= 11,2 . 2 = 22,4 lít

a) Hợp chất A có khối lượng mol phân tử là 58,5 g/mol, thành phần các nguyên tố theo khối lượng: 60,68% Cl và còn lại là Na.
b) Hợp chất B có khối lượng mol phân tử là 106 g/mol, thành phần các nguyên tố theo khối lượng: 43,4% Na; 11,3% C; 45,3% O
Bài giải:
a) Ta có:
MA = 58,5 g
%Cl = 60,68% => %Na = 39,32%
=> MCl = = 35,5 đvC => nCl = 1 mol
=> MNa = = 23 đvC => nNa = 1 mol
Vì Na hóa trị I và Cl hóa trị 1 nên CTHH: NaCl
b) Ta có:
MB =106 g
MNa = = 46 => nNa =
= 2 mol
MC = = 12 => nC = 1 mol
MO = = 48 => nO =
= 3 mol
Suy ra trong một phân tử hợp chất B có 2 nguyên tử Na, 1 nguyên tử C và 3 nguyên tử O
Do đó công thức hòa học của hợp chất B là Na2CO3
a) Ta có:
MA = 58,5 g
%Cl = 60,68% => %Na = 39,32%
=> MCl = = 35,5 đvC => nCl = 1 mol
=> MNa = = 23 đvC => nNa = 1 mol
Vì Na hóa trị I và Cl hóa trị 1 nên CTHH: NaCl
b) Ta có:
MB =106 g
MNa = = 46 => nNa =
= 2 mol
MC = = 12 => nC = 1 mol
MO = = 48 => nO =
= 3 mol
Suy ra trong một phân tử hợp chất B có 2 nguyên tử Na, 1 nguyên tử C và 3 nguyên tử O
Do đó công thức hòa học của hợp chất B là Na2CO3

Ta có: = 17 => MA = 17 . 2 = 34
Khối lượng của mỗi nguyên tố có trong 1 mol khí A
=> mH = = 2 (g) => mS =
= 32 (g)
hoặc mS = 34 - 2 = 32 (g)
Số mol nguyên tử của mỗi nguyên tố trong 1 mol khí A:
nH = = 2 mol nS =
= 1 mol
Suy ra trong 1 phân tử hợp chất A có 2 nguyên tử H và 1 nguyên tử S. Do đó công thức hóa học của khí A là H2S
Ta có: = 17 => MA = 17 . 2 = 34
Khối lượng của mỗi nguyên tố có trong 1 mol khí A
=> mH = = 2 (g) => mS =
= 32 (g)
hoặc mS = 34 - 2 = 32 (g)
Số mol nguyên tử của mỗi nguyên tố trong 1 mol khí A:
nH = = 2 mol nS =
= 1 mol
Suy ra trong 1 phân tử hợp chất A có 2 nguyên tử H và 1 nguyên tử S. Do đó công thức hóa học của khí A là H2S

2. Kết luận nào sau đây đúng ?
Thế tích mol của chất khí phụ thuộc vào:
a) Nhiệt độ của chất khí;
b) Khối lượng mol của chất khí;
c) Bản chất của chất khí;
d) Áp suất của chất khí.
Bài giải:
Câu a và d diễn tả đúng.

mdd muối = 86,26 - 60,26 = 26g
--> m muối KT = 66,26 - 60,26 = 6 g
=> m H20 = 26 - 6 = 20 g
- Có 6g muối tan trong 20 g H20
- Có ? g muối tan trong 100g H20
( dùng tăng suất để tính tức là lấy 100g nhân 6g chia 20 g H20, kiểu nhân chéo chia ngang ây)
=> có 30 g muối tan trong 100g H20
S= 30g
Ta có: mdd = 86,26 – 60,26 = 26 (gam)
mct = 66,26 – 60,26 = 6 (gam)
Ở 20℃, cứ 20 gam nước hòa tan 6 gam muối tạo dung dịch bão hòa. Vậy ở 20℃, 100 gam nước hòa tan khối lượng muối là:
S=100×620=30(gam)
Vậy độ tan của muối ở 20℃ là 30 gam

Số mol sắt tham gia phản ứng:
nFe = 0,05 mol
a) Thể tích khí hiđro thu được ở đktc:
Fe + 2HCl → FeCl2 + H2.
Theo phương trình hóa học, ta có: = nFe = 0,05 mol
Thể tích khí thu được ở đktc là: = 22,4 . n = 22,4 . 0,05 = 1,12 lít
b) Khối lượng axit clohiđric cần dùng
Theo phương trình hóa học, ta có:
nHCl = 2nFe = 2 . 0,05 = 0,1 mol
Khối lượng HCl cần dùng là: mHCl = M . n = 0,1 . 36,5 = 3,65 g
Bài giải:
Số mol sắt tham gia phản ứng:
nFe = 0,05 mol
a) Thể tích khí hiđro thu được ở đktc:
Fe + 2HCl → FeCl2 + H2.
Theo phương trình hóa học, ta có: = nFe = 0,05 mol
Thể tích khí thu được ở đktc là: = 22,4 . n = 22,4 . 0,05 = 1,12 lít
b) Khối lượng axit clohiđric cần dùng
Theo phương trình hóa học, ta có:
nHCl = 2nFe = 2 . 0,05 = 0,1 mol
Khối lượng HCl cần dùng là: mHCl = M . n = 0,1 . 36,5 = 3,65 g

Nếu hai chất khí khác nhau mà có thể tích bằng nhau (đo cùng nhiệt độ và áp suất) thì:
a) Chúng có cùng số mol chất.
b) Chúng có cùng khối lượng .
c) Chúng có cùng số phân tử.
d) Không thể kết luận được điều gì cả.

a, nCaCO3=10/100=0,1 mol
PTHH: CaCO3+2HCl---> CaCl2+CO2+H2O
Theo pthh ta có: nCaCl2=nCaCO3=0,1 mol
=> mCaCl2=0,1.111=11,1 (g)
b, nCaCO3=5/100=0,05 mol
Theo pthh ta có : nCO2=nCaCO3=0,05 mol
=> VO2(điều kiện phòng)= 0,05.24= 1,2 l
a) Số mol canxi cacbonat tham gia phản ứng
=
= 0,1 mol
CaCO3 + 2HCl → CaCl2 + CO2 + H2O
Theo phương trình hóa học, ta có:
=
= 0,1 mol
Khối lượng của canxi clotua tham gia phản ứng:
= 0,1 . (40 + 71) = 11,1 g
b) Số mol canxi cacbonat tham gia phản ứng:
=
= 0,05 mol
Theo phương trình hóa học, ta có:
=
= 0,05 mol
Thể tích khí CO2 ở điều kiện phòng là:
= 24 . 0,05 = 1,2 lít
a) Khối lượng mol của các khí có tỉ khối với oxi là:
b) Khối lượng mol của các khí có tỉ khối với không khí là:
dx/kk =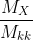 =
= 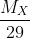 = 2,207 => MX = 29 . 2,207 = 64 g
= 2,207 => MX = 29 . 2,207 = 64 g
dy/kk =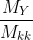 =
=  = 1,172 => MY = 29 . 1,172 = 34 g
= 1,172 => MY = 29 . 1,172 = 34 g
a) Khối lượng mol của các khí có tỉ khối với oxi là:
b) Khối lượng mol của các khí có tỉ khối với không khí là:
dx/kk =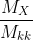 =
= 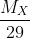 = 2,207 => MX = 29 . 2,207 = 64 g
= 2,207 => MX = 29 . 2,207 = 64 g
dy/kk =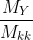 =
=  = 1,172 => MY = 29 . 1,172 = 34 g
= 1,172 => MY = 29 . 1,172 = 34 g