Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

CO2 + Ca(OH)2 → CaCO3 + H2O
0,1 0,1 0,1
2CO2 + CaCO3 + H2O → Ca(HCO3)2
0,16 – 0,1 → 0,06
=> n↓= 0,04 mol
n↓= 0,04 mol => m ↓ = 4g < 0,16 . 44 = 7,04g
=> mdd tăng = 7,04 – 4 = 3,04g
nCa(OH)2 = 2.0,05=0,1(mol)
ta có nCO2/nCa(OH)2 = 0,16/0,1 = 1,6
=> có 2 phản ứng xảy ra
CO2 + Ca(OH)2 ---> CaCO3 + H2O (1)
2CO2 +Ca(OH)2 ---> Ca(HCO3)2 (2)
bảo toàn C ta có x +2y = 0,16(3)
bảo toàn Ca ta có x +y = 0,1 (4)
từ (3) và (4) => x= 0,04(mol) y= 0,06(mol)
mCa(HCO3) = 0,06.145= 8,7(g)
m Ca(OH)2 = 0,1.57 = 5,7g
vậy khối lượng của Ca(HCO3)2 tăng 3g so với Ca(OH)2 ban đầu

Dẫn sản phẩm cháy vào bình đựng Ca(OH)2 thì CO2 và H2O bị hấp thụ
Vì đun nước lọc thu được thêm kết tủa\(\rightarrow\) Tạo ra Ca(HCO3)2
Ca(OH)2 + CO2 \(\rightarrow\)CaCO3 + H2O
Ca(OH)2 + 2CO2\(\rightarrow\) Ca(HCO3)2
Ca(HCO3)2\(\rightarrow\)CaCO3 + CO2 + H2O
nCaCO3=\(\frac{40}{100}\)=0,4 mol
nCa(HCO3)2=nCaCO3 tạo thêm=\(\frac{25}{100}\)=0,25 mol
\(\rightarrow\)nCO2=nCaCO3 +2nCa(HCO3)2=0,9 mol
m bình tăng=mCO2 + mH2O -mCaCO3 (1) =7,7 \(\rightarrow\) mCO2 + mH2O=40+7,7
\(\rightarrow\)nH2O=8,1 gam \(\rightarrow\) nH2O=0,45 mol
\(\rightarrow\) X chứa 0,9 mol C và 0,9 mol H
Vì 0,9.12 +0,9=11,7 nên không X không chứa O
\(\rightarrow\)X có dạng (CH)n
Ta có: 70 < MX <80\(\rightarrow\) n=6\(\rightarrow\) X là C6H6
nX=\(\frac{11}{78}\)=0,15 mol
Cho X tác dụng với AgNO3 /NH3 được 43,8 gam kết tủa
\(\rightarrow\)nX=n kết tủa \(\rightarrow\) M kết tủa=292
\(\rightarrow\)Số nguyên tử Ag thế vào\(\frac{\text{292-78}}{108-1}\)=2
X có 2 liên nhóm -C≡CH
CTCT của X có thể là HC≡C-CH2-CH2-C≡CH
hoặc HC≡C-CH(CH3)-C≡CH

1. nCa(OH)2=15*0,01=0,15 mol
Khi sục khí CO2 vào thì kết tủa xuất hiện:
CO2 + Ca(OH)2 -> CaCO3 + H20
Ta có: nCO2 : nCa(OH)2 = 1:1
Mà: 0,02 <= n CO2 <= 0,17 nên CO2 dư,kết tủa bị hòa tan
CaCO3 +H20 + CO2 -> Ca(HCO3)2 (tan)
Tỉ lệ là 1:1 nên kết tủa thu được nhiều nhất khi nCO2=nCa(OH)2=0,15 mol => mCaCO3=15g
* Xét khoảng 0,02 <= n CO2 <= 0,15, lúc này số mol CO2 càng tăng thì khối lượng kết tủa càng lớn => Khối lượng kết tủa nhỏ nhất khi nCO2 = 0,02 mol => mCaCO3=0,02* 100 = 2g
* Xét khoảng 0,15 < n CO2 <= 0,17, lúc này số mol CO2 càng tăng thì khối lượng kết tủa càng giảm=> nCO2 có thể dư nhiều nhất là 0,17 - 0,15=0,02 mol => nCaCO3 bị hòa tan = nCO2 =0,02
=> mCaCO3 thu được khi nCO2= 0,17 mol là: 0,15 - 0,02*100 = 13g
Vậy khối lượng kết tủa thu được trong khoảng [2;15]g
Chúc bạn học tốt!

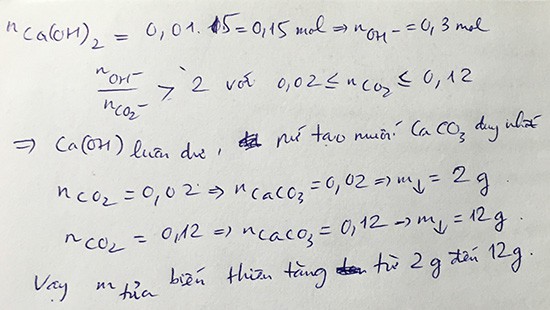
Đáp án A
Ta có: n C a C O 3 = 2/100 = 0,02 mol
mdung dịch tăng= m C O 2 - m C a C O 3
→ m C O 2 = 4,16 + 2 = 6,16 gam
→ n C O 2 = 0,14 mol
→ V C O 2 = 0,14.22,4 = 3,136 lít