Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn C
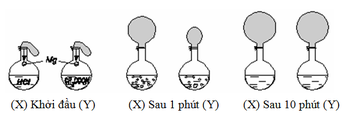
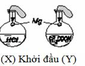
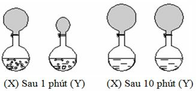
(1) Sau 1 phút, khí H2 thoát ra ở bình X nhiều hơn ở bình Y
(4) Sau 10 phút, khí H2 thoát ra ở 2 bình X và Y bằng nhau

Đáp án B
Do hai bình mắc nối tiếp điện tích qua chúng không đổi, dẫn tới số mol e trao đổi của chúng bằng nhau:
![]()

Đáp án B
Vì hai bình điện phân mắc nối tiếp nên số mol electron trao đổi ở hai bình điện phân là như nhau.
Ở hai bình đều không thấy khí ở catot thoát ra nên ở catot của hai bình chưa có sự điện phân nước.
Áp dụng định luật bảo toàn mol electron, ta có:
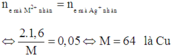

Đáp án A
- 2 bình mắc nối tiếp nên dòng điện chạy qua có cùng cường độ
Đổi 3 phút 13 giây = 193 giây; 9 phút 39 giây = 579 giây
- Phương trình điện phân
Bình 1:
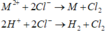
Bình 2: ![]()
+ Bình 2:
![]()
=> Chứng tỏ Ag+ còn dư sau khi điện phân 193s, có thể còn dư sau điện phân 579s
Điện phân 193s :
![]()
+ Bình 1:
![]()
=> Chứng tỏ M2+ ở bình 1 bị điện phân trước, sau khi điện phân 193s thì M2+ còn dư; sau khi điện phân 579s thì M2+ hết; H+ đã bị điện phân
Điện phân 193s:
![]()
=> M là Cu => 0,8 a = 3 , 2 64 => a = 0,0625(M)
![]()

nZn=\(\dfrac{m}{M}=\dfrac{12,8}{65}=0,197\left(mol\right)\)
pthh:
Zn + 2HCl \(\rightarrow\) ZnCl2 + H2
0,197..0,394.....0,197...0,197(mol)
2H2 + O2 \(\rightarrow\) 2H2O
0,197................0,197
mH2O=n.M=0,197.18=3,546(g)

Đáp án A
· Có n FeCO 3 = n CO 2 = n CaCO 3 = 24 100 = 0 , 24 mol
· Phần 1: n Al = 2 3 n H 2 = 2 3 . 0 , 06 = 0 , 04 mol
Þ Al dư, hỗn hợp rắn sau phản ứng gồm Fe, Al2O3.
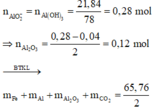 ⇒
m
Fe
=
32
,
86
-
44
.
0
,
24
2
-
102
.
0
,
12
-
27
.
0
,
04
=
14
,
28
g
⇒
n
Fe
=
0
,
255
mol
⇒
m
Fe
=
32
,
86
-
44
.
0
,
24
2
-
102
.
0
,
12
-
27
.
0
,
04
=
14
,
28
g
⇒
n
Fe
=
0
,
255
mol
· Phần 2: Đặt số mol muối Fe2(SO4)3 và FeSO4 lần lượt là x, y.
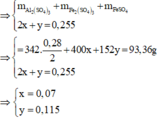
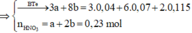
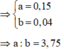

Chọn đáp án A
nCO2 = 0,24 mol. Bảo toàn khối lượng: mB = 65,76 - 0,24 × 44 = 55,2(g).
► Xét 1 phần ⇒ mB = 27,6(g). Có H2 ⇒ Al dư ⇒ B gồm Al dư, Al2O3 và Fe.
⇒ nAl = 0,06 ÷ 1,5 = 0,04 mol || nAl(OH)3 = 0,28 mol ⇒ nAl2O3 = 0,12 mol.
→ m B nFe = 0,255 mol ⇒ nSO42– = (93,36 - 0,28 × 27 - 0,255 × 56) ÷ 96 = 0,745 mol.
⇒ nH2SO4 = 0,745 mol ⇒ ∑nH+ = 0,745 × 2 + 0,23 = 1,72 mol.
● ∑nH+ = 4nNO + 10nN2O + 2nO ⇒ 4a + 10b = 1. Bảo toàn nguyên tố Nitơ:
a + 2b = 0,23 mol ||⇒ giải hệ có: a = 0,15 mol; b = 0,04 mol.
⇒ a : b = 3,75 ⇒ chọn A.

Ta gọi nC=x ;nH=y ta được 12x+y=4,64
Ta có: m dd giảm=mkếttủa - (mCO2 + mH2O) => mCO2+mH2O
=mkettua- mdd giảm=39,4-19,912=19,488g
=> 44x+18.0,5y=10,688
Giải hpt: x=0,348; y=0,464 => x:y=3:4
=> CTĐGN của X là C3H4 => CTPT là C3H4.
Chọn đáp án C.