
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


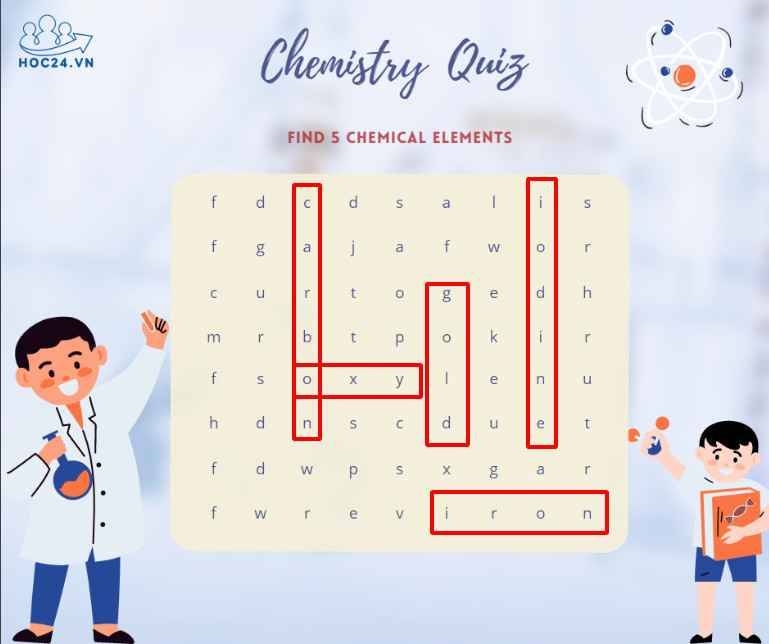
*cái oxy em k chắc á cô:<< em tìm được mấy nguyên tố này th ạ:<.


Đề bài cho hỗn hợp X gồm hai khí là methane (CH4) và ethylene (C2H4). Hỗn hợp này có tỉ khối so với hydrogen (H2) bằng 10.
- Bước 1: Tính khối lượng mol trung bình của hỗn hợp X (MX)
Tỉ khối của hỗn hợp X so với hydrogen được tính bằng công thức: dX/H2=MH2MX.
Trong đó, MH2=2 g/mol.
Ta có: 10=2MX⇒MX=10×2=20 g/mol.
- Bước 2: Gọi thành phần phần trăm thể tích của từng khí trong hỗn hợp
Giả sử trong 1 mol hỗn hợp X, số mol của CH4 là x và số mol của C2H4 là y.
Ta có: x+y=1 (1)
Khối lượng mol trung bình của hỗn hợp X được tính bằng công thức: MX=nCH4+nC2H4nCH4⋅MCH4+nC2H4⋅MC2H4.
MCH4=12+4=16 g/mol.
MC2H4=12×2+4=28 g/mol.
Thay vào công thức ta có: 20=x+yx⋅16+y⋅28=116x+28y (2)
Từ (1) và (2) ta có hệ phương trình:
x+y=1
16x+28y=20
Giải hệ phương trình này, ta được: x=32 và y=31.
Điều này có nghĩa là trong hỗn hợp X, số mol của CH4 chiếm 32 và số mol của C2H4 chiếm 31.
- Bước 3: Tính tổng số mol của hỗn hợp X
Thể tích của hỗn hợp X ở điều kiện tiêu chuẩn (đktc) là 3,7185 lít.
Số mol của hỗn hợp X là: nX=24.79V=24.793.7185=0.15 mol.
(Lưu ý: Nếu đề bài cho ở điều kiện tiêu chuẩn cũ (0 độ C, 1 atm) thì V = 22.4, nhưng theo quy ước quốc tế mới, 1 bar và 25 độ C thì V = 24.79. Đề bài không nói rõ nên ta chọn chuẩn mới là 24.79).
- Bước 4: Tính số mol C2H4 trong hỗn hợp X
Từ kết quả ở bước 2, ta biết số mol C2H4 chiếm 31 tổng số mol.
nC2H4=nX×y=0.15×31=0.05 mol.
- Bước 5: Tính số mol Br2 đã phản ứng
Khi hỗn hợp X cho qua dung dịch Br2 dư, chỉ có ethylene (C2H4) phản ứng vì nó có liên kết đôi (C=C). Methane (CH4) là ankan nên không phản ứng với Br2.
Phương trình phản ứng:
C2H4+Br2→C2H4Br2
Theo phương trình, tỉ lệ mol là 1:1, vậy:
nBr2=nC2H4=0.05 mol.
Kết luận
Số mol Br2 đã tham gia phản ứng là 0,05 mol.

Câu 3:
N2+O2\(\overset{t^0}{\rightarrow}\)2NO
4NO+3O2+2H2O\(\rightarrow\)4HNO3
NO3- : làm tăng lượng phân đạm cho cây!


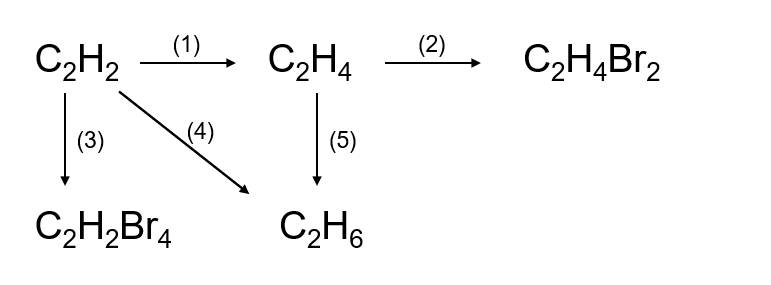
(1) \(2CH_4\xrightarrow[lln]{1500^oC}C_2H_2+3H_2\)
(2) \(C_2H_2+H_2\underrightarrow{t^o,Pd}C_2H_4\)
(3) \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
(4) \(CH_4+Cl_2\underrightarrow{as}CH_3Cl+HCl\)
(5) \(C_2H_2+2Br_2\rightarrow C_2H_2Br_4\)
(6) \(C_2H_2+2H_2\underrightarrow{t^o,Ni}C_2H_6\)
(7) \(C_2H_4+H_2\underrightarrow{t^o,Ni}C_2H_6\)
(1) 2��4→���1500���2�2+3�22CH41500oCllnC2H2+3H2
(2) �2�2+�2��,��→�2�4C2H2+H2to,PdC2H4
(3) �2�4+��2→�2�4��2C2H4+Br2→C2H4Br2
(4) ��4+��2��→��3��+���CH

Câu 1:
Khi đẫn hỗn hợp gồm C2H4 và CH4 qua bình đựng dung dịch Br2 dư thì C2H4 bị giữ lại trong bình
=> m bình tăng = mC2H4 = 1,4(g)
\(nC_2H_4=\dfrac{1,4}{28}=0,05(mol)\)
\(=> VC_2H_4(đktc)=0,05.22,4=1,12(l)\)
Phần trăm thể tích của mỗi hidrocacbon trong hon hợp ban đầu là:
\(=>\%VC_2H_4=\dfrac{1,12.100}{2,8}=40\%\)
\(=>\%VCH_4=100\%-40\%=60\%\)
Câu 2:
\(a) \) \(PTHH:\)
\(2C_2H_6+7O_2-t^o-> 4CO_2+6H_2O\) \((1)\)
\(C_3H_8+5O_2-t^o-> 3CO_2+4H_2O\) \((2)\)
\(2C_4H_{10}+13O_2-t^o->8CO_2+10H_2O\) \((3)\)
\(b)\) (thiếu số liệu)

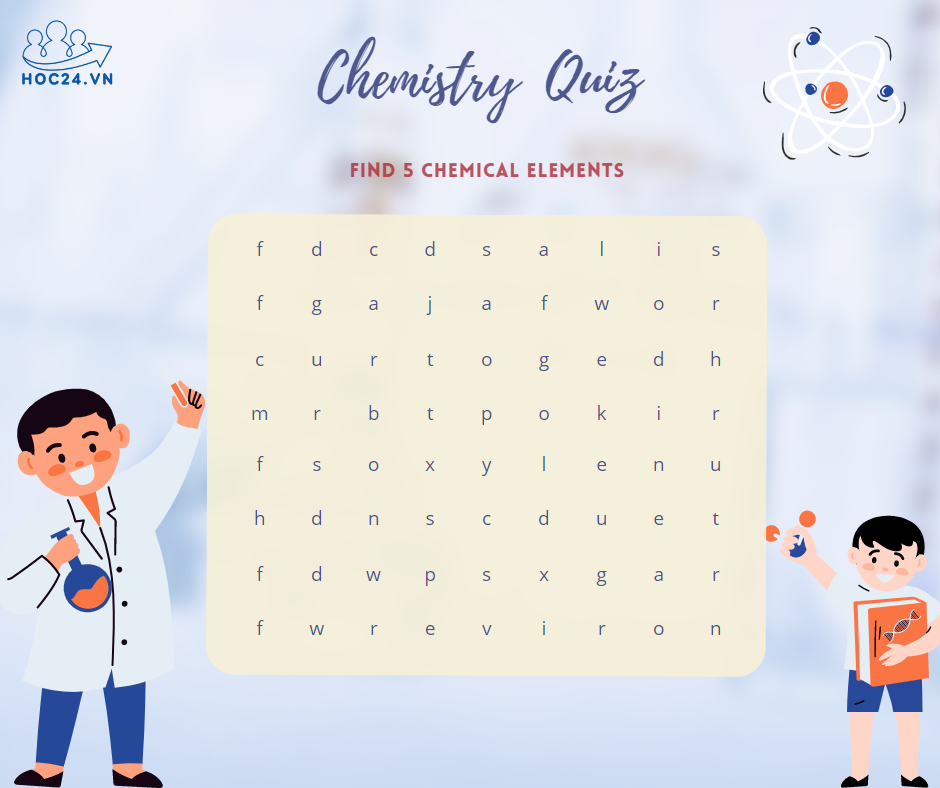
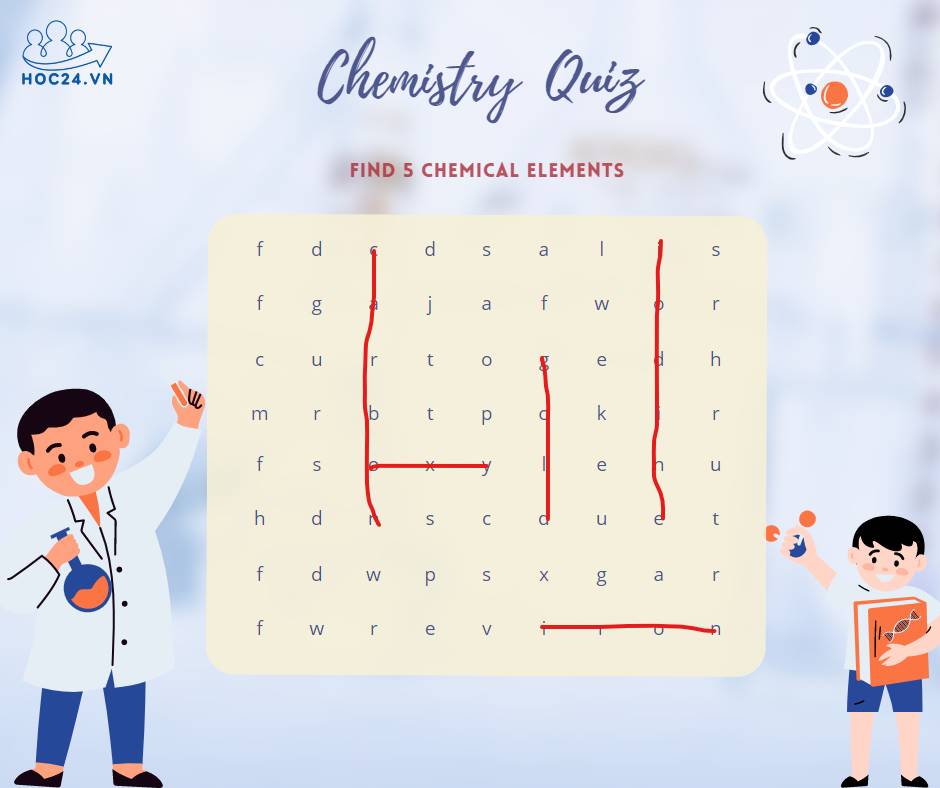














 Giúp mình giải vài câu thực tế Hoá nha..
Giúp mình giải vài câu thực tế Hoá nha..









 mơ
mơ
a)
$n_{NaHCO_3} = \dfrac{42}{84} = 0,5(mol)$
$NaHCO_3 + CH_3COOH \to CH_3COONa + CO_2 + H_2O$
Theo PTHH :
$n_{CH_3COOH} = n_{NaHCO_3} = 0,5(mol)$
$m_{dd\ CH_3COOH} = \dfrac{0,5.60}{12\%} = 250(gam)$
b) $n_{CO_2} = n_{NaHCO_3} = 0,5(mol)$
$V_{CO_2} = 0,5.22,4 = 11,2(lít)$
c) $CH_3COOH + NaOH \to CH_3COONa + H_2O$
$n_{NaOH} = n_{CH_3COOH} = 0,5(mol)$
$V_{dd\ NaOH} = \dfrac{0,5}{0,2} = 2,5(lít)$