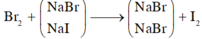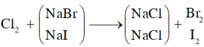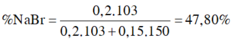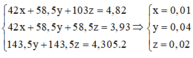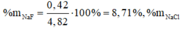Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án C
Gọi số mol của NaBr là x mol; NaI là y mol.
Cho B r 2 vào dung dịch A, chỉ NaI phản ứng.
NaI + 1 2 Br2 → NaBr + 1 2 I2
1 mol NaI → 1 mol NaBr khối lượng giảm 47g
→ n N a I = 7 , 05 47 = 0,15 mol = y
Khi sục khí Clo vào dung dịch A, cả NaBr và NaI phản ứng.
m m u ố i g i ả m = x.(80 – 35,5) + y (127-35,5) = 22,625 g
→ x = 0,2 mol
ð % m N a B r = 0 , 2 . 103 0 , 2 . 103 + 0 , 15 . 150 .100(%) = 47,80(%)

Đáp án B
Đặt
![]()
Khối lượng muối khan giảm là do đã xảy ra phản ứng thay thế các nguyên tử halogen trong muối.
Ta có hệ:
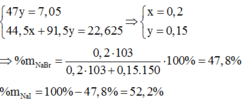

X + AgNO3\(\rightarrow\)kết tủa AgCl + muối Y
Kết tủa là AgCl\(\rightarrow\) nAgCl=\(\frac{22,96}{\text{108+35,5}}\)=0,16 mol
Bảo toàn Ag: nAgCl=nAgNO3=0,16 mol
\(\rightarrow\)mAgNO3=0,16.(108+62)=27,2 gam
BTKL: mX + mAgNO3=mAgCl + mY
\(\rightarrow\)9,3+27,2=22,96+mY\(\rightarrow\)mY=13,54 gam

=
= 0, 025 mol
Phương trình hóa học của phản ứng:
NaBr + AgNO3 → AgBr↓ + NaNO3
X mol x mol x mol
NaCl + AgNO3 → AgCl↓ + NaNO3
Y mol y mol y mol
Biết nồng độ phần trăm của mỗi muối trong dung dịch bằng nhau và khối lượng dung dịch là 50g, do đó khối lượng NaCl bằng khối lượng NaBr.
Ta có hệ phương trình đại số:
Giải ra , ta có x = 0, 009 mol NaBr
→ mNaBr = mNaCl = 103 x 0,009 = 0,927g
C% = x 100% = 1,86%

nNO=3,36/22,4=0,15
Theo định luật bảo toàn mol e
\(Fe^0\rightarrow Fe^{+3}+3e
\)
\(Cu^0\rightarrow Cu^{+2}+2e\)
\(N^{+5}+3e\rightarrow N^{+2}\)
=> 3a+2b=3.0,15=0,45
Ta có hpt:\(\begin{cases}3a+2b=0,45\\56a+64b=12,4\end{cases}\Leftrightarrow\begin{cases}a=0,05\left(mol\right)\\b=0,15\left(mol\right)\end{cases}}\)
\(n_{Fe\left(NO3\right)3}=n_{Fe}=0,05,n_{Cu\left(NO3\right)2}=n_{Cu_{ }_{ }}=0,15\)Từ đó tính m nha bạn