Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

A: MgO, CuO
B: MgCl2, CuCl2
C: Mg(OH)2, Cu(OH)2
PT: \(2Mg+O_2\underrightarrow{t^o}2MgO\)
\(2Cu+O_2\underrightarrow{t^o}2CuO\)
\(MgO+2HCl\rightarrow MgCl_2+H_2O\)
\(CuO+2HCl\rightarrow CuCl_2+H_2O\)
\(MgCl_2+2NaOH\rightarrow2NaCl+Mg\left(OH\right)_{2\downarrow}\)
\(CuCl_2+2NaOH\rightarrow2NaCl+Cu\left(OH\right)_{2\downarrow}\)
\(Mg\left(OH\right)_2\underrightarrow{t^o}MgO+H_2O\)
\(Cu\left(OH\right)_2\underrightarrow{t^o}CuO+H_2O\)

câu 1: nAl=0,4 mol
mHCL=54,75g=> nHCl=1,5 mol
PTHH: 2Al+6HCl=> 2AlCl3+3H2
0,4mol: 1,5mol => nHCl dư theo nAl
0,4mol-->1,2 mol-->0,4mol-->0,6mol
thể tích H2 là V=0,6.22,4=13,44ml
b) theo định luật btoan khối lượng ta có : mAlCl3=200+10,8-0,6.2=209,6g
m AlCl3=0,4.(27+35,5.3)=53,4g
=> C% AlCl3= 25,48%
PTHH: 2Al + 6HCl → 2AlCl3 + 3H2 ↑
Khối lượng chất tan HCl là:
200 . 27,375% = 54,75(gam)
Số mol của HCl là: 54,75 : 36,5 = 1,5 (mol)
Số mol của Al là: 10,8 : 27 = 0,4 (mol)
So sánh: \( {0,4{} \over 2}\) < \({1,5} \over 6\)
=> HCl dư, tính theo Al
Số mol của khí hiđrô sinh ra là: 0,4 . \(3 \ \over 2\) = 0,6 (mol)
V= 0,6 . 22,4 = 13,44 (lít)
Sau đó áp dụng định luật bảo toàn khối lượng để tính khối lượng dung dịch A:
Khối lượng nhôm + Khối lượng dung dịch axit
= Khối lượng dung dịch A + khối lượng khí hiđrô
<=> Khối lượng dung dịch A là:
10,8 + 200 - 0,6 . 2 = 209,6 (gam)
Khối lượng chất tan AlCl3 trong dung dịch A là:
0,4 . 133,5 = 53,4 (gam)
C% chất tan trong dung dịch A là:
( 53,4 : 209,6 ) . 100% = 25,48%

1. Gọi mol của Mg và Al là x, y mol
=> 24x + 27y = 12,6 (1)
nH2 = 0,6 mol => x + 1,5y = 0,6 (2)
Từ (1) (2) => x = 0,3 ; y = 0,2
=> %Mg = 57,14%
=> %Al = 42,86%
nH2=13,44/22,4=0,6(mol)
Đặt: nMg=a(mol); nAl=b(mol) (a,b>0)
1) PTHH: Mg + H2SO4 -> MgSO4 + H2
a__________a________a_____a(mol)
2Al +3 H2SO4 -> Al2(SO4)3 + 3 H2
b___1,5b______0,5b____1,5b(mol)
Ta có hpt:
\(\left\{{}\begin{matrix}24a+27b=12,6\\a+1,5b=0,6\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,3\\b=0,2\end{matrix}\right.\)
=> mMg=0,3.24=7,2(g)
=>%mMg= (7,2/12,6).100=57,143%
=>%mAl=42,857%
2) mMgSO4=120.a=120.0,3=36(g)
mAl2(SO4)3=342.0,5b=342.0,5.0,2= 34,2(g)
mH2SO4= (0,3+0,2.1,5).98=58,8(g)
=>mddH2SO4=58,8: 14,7%=400(g)
=>mddsau= 12,6+400 - 2.0,6= 411,4(g)
=>C%ddAl2(SO4)3= (34,2/411,4).100=8,313%
C%ddMgSO4=(36/411,4).100=8,751%

\(n_{O_2}=\frac{1.68}{22.4}=0.075\left(mol\right)\)
\(4Na+O_2\rightarrow2Na_2O\)
x \(\frac{1}{4}x\) \(\frac{1}{2}x\)
\(4K+O_2\rightarrow2K_2O\)
x \(\frac{1}{4}x\) \(\frac{1}{2}x\)
Theo bài ra ta có \(\begin{cases}23x+39y=10.1\\\frac{1}{4}x+\frac{1}{4}y=0.075\end{cases}\) \(\begin{cases}0.1\\0.2\end{cases}\)
\(m_{Na}=0.1\times23=2.3\left(g\right)\)
\(m_K=0.2\times39=7.8\left(g\right)\)

\(\frac{n_C}{n_S}=\frac{3}{2}=1,5=>n_C=1,5n_S\)
gọi số mol S là x => số mol C là 1,5x
theo đề ra ta có : 32x+12.1,5x=5(g)
=> 32x + 18x = 5
=> x = 0,1(mol)
=> \(m_S=0,1.32=3,2\left(g\right)\)
=> \(m_C=5-3,2=1,8\left(g\right)\)
b , \(S+O_2->SO_2\left(1\right)\)
\(C+O_2->CO_2\left(2\right)\)
\(M_B=21.2=42\left(g\right)\)
\(M_B< M_{CO_2}< M_{SO_2}\)
=> trong B có \(O_2\left(dư\right)\)
theo (1) \(n_{SO_2}=n_S=0,1\left(mol\right)\)
theo (2) \(n_{CO_2}=n_C=\frac{1,8}{12}=0,15\left(mol\right)\)
gọi n là số mol \(O_2\)dư , ta có
\(M_B=\frac{0,1.64+0,15.44+32n}{0,1+0,15+n}=42\)
=> 6,4 + 6,6 + 32n = 4,2+ 6,3 + 42n
=> 2,5 = 10n
=> n = 0,25(mol)
theo (1) \(n_{O_2\left(pư\right)}=n_S=0,1\left(mol\right)\) , theo (2) \(n_{O_2\left(pư\right)}=n_C=0,15\left(mol\right)\)
=> \(V_{O_2}=\left(0,25+0,15+0,1\right).22,4=11,2\left(l\right)\)
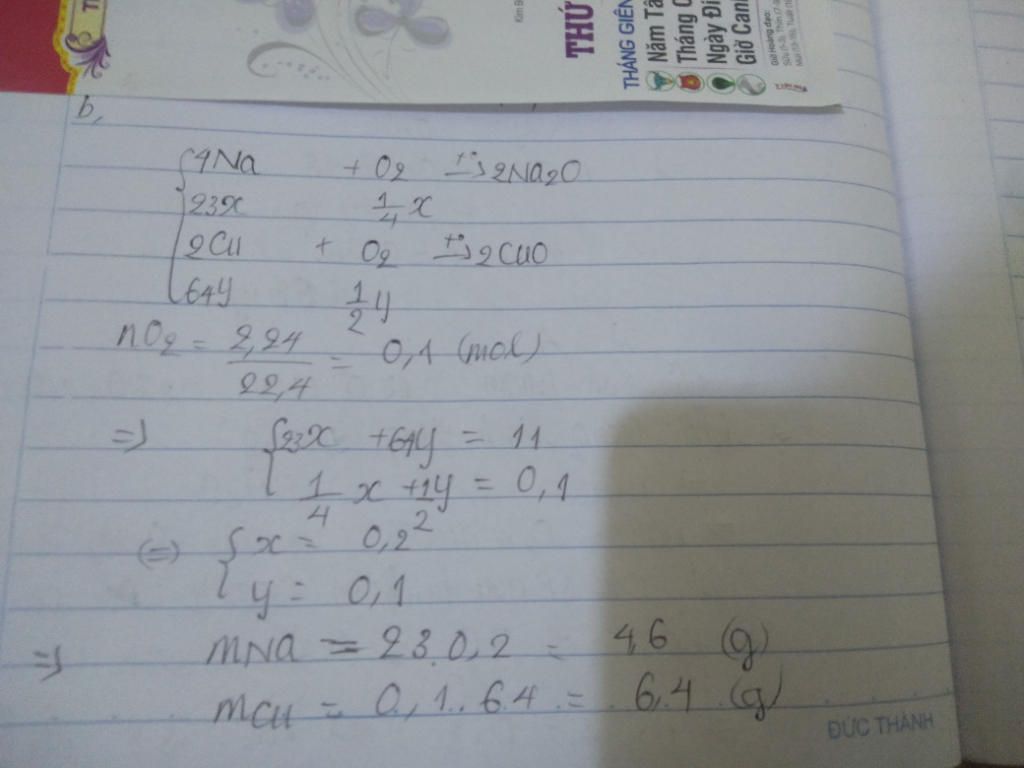
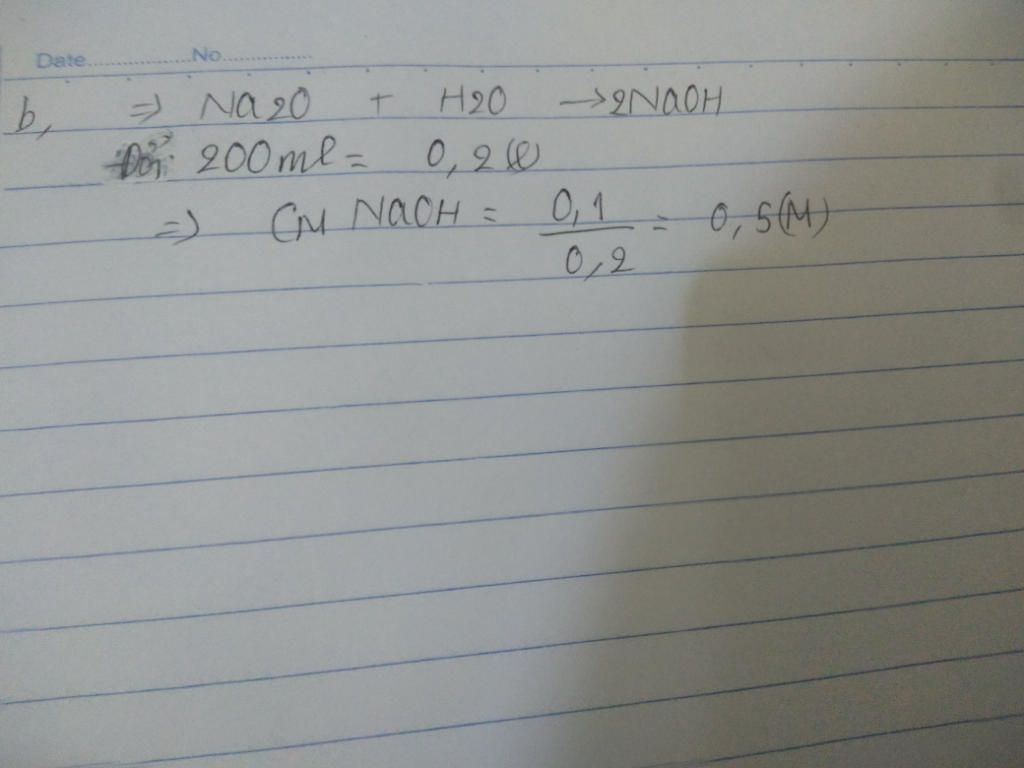
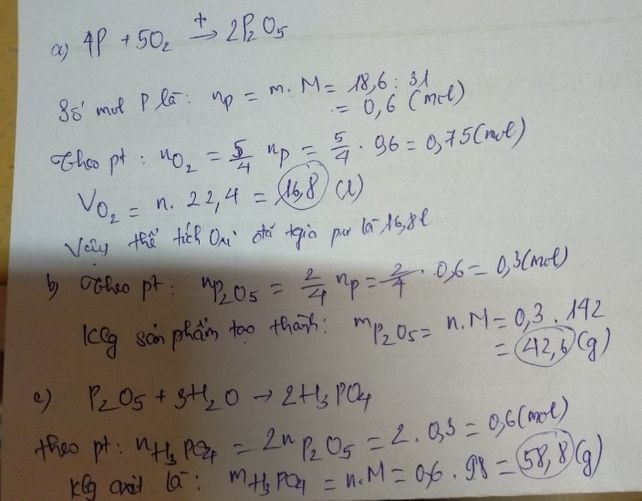
 Bạn tham khảo cách làm nhé! cho mik 1 like nha
Bạn tham khảo cách làm nhé! cho mik 1 like nha
Đặt: nK= x mol
nMg= 2x mol
mhh= 39x + 24x*2= 8.7g
<=> x= 0.1
2K + 1/2O2 -to-> K2O
0.1__0.025______0.05
Mg + 1/2O2 -to-> MgO
0.2____0.1______0.2
VO2= (0.1+0.025)*22.4=2.8l
Rắn A: K2O, MgO
K2O + H2O --> 2KOH
0.05__________0.1
mK2O= 0.05*94=4.7g
dd B: KOH
Rắn C: MgO
CM KOH= 0.1/0.2=0.5M
mKOH= 0.1*56=5.6g
mH2O= 200*1=200g
mdd sau hòa tan= mK2O + mH2O= 4.7+200=204.7g
C% KOH= 5.6/204.7*100%= 2.73%