Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
n N a O H = 0 , 5 . 0 , 1 = 0 , 05 m o l ; n K O H = 0 , 5 . 0 , 2 = 0 , 1 m o l
Gọi công thức chung của 2 bazơ mà MOH
Ta có: n M O H = 0 , 1 + 0 , 05 = 0 , 15 m o l
M M O H = 40 . 0 , 05 + 56 . 0 , 1 0 , 15 = 152 3 → M M = 101 3
TH1: Muối là MH2PO4
→ n M H 2 P O 4 = 0 , 15 m o l → m M H 2 P O 4 = 0 , 15 . 101 3 + 97 = 19 , 6 g a m
TH2: Muối là M2HPO4
→ n M H 2 P O 4 = 0 , 075 m o l → m M H 2 P O 4 = 0 , 075 . 101 3 . 2 + 96 = 12 , 25 g a m
TH3: Muối là M3PO4
→ n M 3 P O 4 = 0 , 05 m o l → m M 3 P O 4 = 9 , 8 g a m
Nhận thấy: m M 3 P O 4 < m c h ấ t r ắ n
Chất rắn có chứa MOH dư (a mol) và M3PO4 (b mol)
Ta có hệ phương trình:
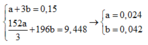
BTNT.P ta có: n P = 0 , 042 m o l → m p = 0 , 042 . 31 = 1 , 302 g a m

Đáp án C
NaOH: 0,05
KOH: 0,1
Gọi công thức chung 2 bazo là MOH (M=101/3) với nMOH=0,15
- Nếu chỉ tạo muối dạng MH2PO4:
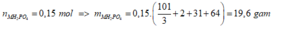
- Nếu chỉ tạo muối dạng M2HPO4:
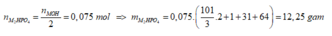
- Nếu chỉ tạo muối M3PO4:
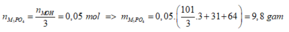
Ta thấy m muối<9,8 gam => MOH dư, H3PO4 hết
Giả sử chất rắn gồm: 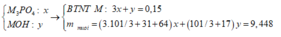
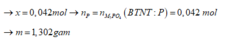

Đáp án C
Phương pháp: Gọi công thức chung 2 bazo là MOH (M = 101/3) với nMOH = 0,15
- Giả sử tạo các muối
+ Nếu chỉ tạo muối dạng MH2PO4
+ Nếu chỉ tạo muối dạng M2HPO4:
+ Nếu chỉ tạo muối M3PO4:
Để biết được hỗn hợp rắn gồm những chất nào, bảo toàn nguyên tố, bảo toàn khối lượng muối => đáp án
Hướng dẫn giải:
NaOH: 0,05
KOH: 0,1
Gọi công thức chung 2 bazo là MOH (M=101/3) với nMOH=0,15
- Nếu chỉ tạo muối dạng MH2PO4:
![]()
![]()
- Nếu chỉ tạo muối dạng M2HPO4:
![]()
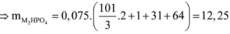
- Nếu chỉ tạo muối dạng M3PO4:
![]()
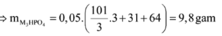
Ta thấy mmuối < 9,8 gam => MOH dư, H3PO4 hết
Giả sử chất rắn gồm:
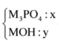
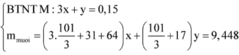
![]()
![]()
![]()

Đáp án C
2P -> P2O5 -> 2H3PO4
=> nH3PO4 = nP = 0,2 mol
,nOH = 0,5 mol => 2 < nOH : nH3PO4 = 2,5 < 3
Các phản ứng :
2MOH + H3PO4 -> M2HPO4 + 2H2O
3MOH + H3PO4 -> M3PO4 + 3H2O
=> Muối gồm : 0,1 mol M2HPO4 và 0,1 mol M3PO4
=> mmuối = mK + mNa + mHPO4 + mPO4 = 35,4g

nH+=0,4+0,1.a
nNO3-=0,1a
bạn viết phương trình Mg+H+ +NO3- dưới dạng pt ion
H++NO3 ttuowng đương với HNO3 loãng
rồi bạn sử dụng phương pháp đường chéo, định luật bảo toàn nguyên tố và electron

a, (1) 4P+5.O2->2.P2O5
(2) P2O5+4.NaOH->2.Na2HPO4+H2O
b, photpho có n=6,2:31=0,2 mol.dựa theo pt (1) thấy nP2O5=0,1mol.theo pt (2) thấy nNaOH=0,4mol vậy mNaOH=0,4.40=16 g vậy m(dd NaOH)=16:32%=50 g
c, theo pt (2) nNa2HPO4 =0,2 mol vậy mNa2HPO4=0,2.142=28,4 g
m(dd sau pư)=mP+m(dd NaOH)=6,2+50=56,2 g
=> C%(dd Na2HPO4)=28,4:56,2=50,53%


Photpho cháy trong không khí lấy dư theo phản ứng :
P 2 O 5 tác dụng với tạo thành H 3 P O 4 theo phản ứng :
Theo phản ứng (1): 4 x 31,0 g P tạo ra 2 x 142,0 g P 2 O 5
a g P tạo ra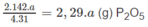
Theo các phản ứng (1) và (2) :
4 x 31,0 (g) P tạo ra 4 x 98,0 (g) H 3 P O 4
a (g) P tạo ra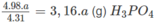
Khối lượng H 3 P O 4 có trong 500,0 ml dung dịch 85,00% :
Khối lượng H 3 P O 4 sau khi đã hoà tan P 2 O 5 : 722,5 g + 3,16 x a g.
Khối lượng của dung dịch H 3 P O 4 sau khi đã hoà tan P 2 O 5 :
500,0 x 1,7 g + 2,29 x a g = 850,0 g + 2,29 x a g
Ta có phương trình về nồng độ phần trăm của dung dịch H 3 P O 4 :
Giải phương trình được a = 62,16 g photpho.