Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

-Theo dữ kiện đề bài ta có
ADCT n=\(\dfrac{m}{M} \)\(\rightarrow\)nAl=\(\dfrac{8,1}{27}\)=0,3(mol)
nO=0,9.10^23/6.10^23=0,15(mol)
-PTHH: 4Al+ 3O2\(\rightarrow\)2Al2O3
Ta có tỉ lệ \(\dfrac{n_{Al}}{4} va \frac{n_{{O}_2}}{3}\)\(\leftrightarrow\)\(\frac{0,3}{4} > \frac{0,15}{3}\)
\(\rightarrow\)nAl du, nO PU het. ta tinh theo nO
a,
-Theo PTHH nAl2O3=2/3.0,15=0,1(mol)
ADCTm=n.M nen mAl2O3=0,1.102=10,2(g)
- Ta có nAl PU het =4/3. nO2=0,2(mol)
nAl du= nAl bd -nAl PU het=0,3-0,2=0,1(mol)
ADCTm=n.M nen mAl du=0,1. 27=2,7(g)
b,
%Al=2. 27/ 102. 100%=53%
%O=3. 16/ 102 .100%=47%
Vay.......

\(n_{Al}=\dfrac{8,1}{27}=0,3\left(mol\right)\)
\(n_{O_2}=\dfrac{0,9\cdot10^{23}}{6\cdot10^{23}}=0,15\left(mol\right)\)
PTHH : 4Al + 3O2 ----> 2Al2O3
ta có tỉ lệ : \(\dfrac{n_{Al}}{n_{O_2}}=\dfrac{4}{3}< \dfrac{0,3}{0,15}\)=> Al dư , O2 hết
Rắn A gồm : Al(dư) , Al2O3
=> mAl phản ứng=\(0,15\cdot\dfrac{4}{3}\cdot27=5,4\left(g\right)\)
=> mAl dư = 8,1 - 5,4 = 2,7(g)
=> \(m_{Al_2O_3}=0,15\cdot\dfrac{2}{3}\cdot102=10,2\left(g\right)\)
b)
\(\%m_{Al\left(A\right)}=\dfrac{2,7}{2,7+10,2}\cdot100\%=20,93\%\)
\(\%m_{Al_2O_3}=100\%-20,93\%=79,07\%\)
\(n_{Al}=\dfrac{8,1}{27}=0,3\left(mol\right)\)
\(n_{O_2}=\dfrac{0,9.10^{23}}{6.10^{23}}=0,15\left(mol\right)\)
- PTHH: \(4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
Theo PT và đề bài ta có tỉ lệ:
\(\dfrac{0,3}{4}=0,075>\dfrac{0,15}{3}=0,05\)
\(\Rightarrow Al_{dư}\). \(O_2\) hết nên ta tính theo \(n_{O_2}\)
a. Chất rắn A gồm Al(dư) và \(Al_2O_3\)
Theo PT ta có: \(n_{Al_2O_3}=\dfrac{2}{3}.n_{O_2}=\dfrac{2}{3}.0,15=0,1\left(mol\right)\)
\(\Rightarrow m_{Al_2O_3}=0,1.102=10,2\left(g\right)\)
Theo PT ta có: \(n_{Al\left(pư\right)}=\dfrac{4}{3}.n_{O_2}=\dfrac{4}{3}.0,15=0,2\left(mol\right)\)
\(n_{Al\left(dư\right)}=0,3-0,2=0,1\left(mol\right)\)
\(\Rightarrow m_{Al\left(dư\right)}=0,1.27=2,7\left(g\right)\)
b. \(m_A=m_{Al\left(dư\right)}+m_{Al_2O_3}=2,7+10,2=12,9\left(g\right)\)
\(\Rightarrow\%Al=\dfrac{2,7}{12,9}.100\%=20,93\%\)
\(\Rightarrow\%Al_2O_3=100\%-20,93\%=79,07\%\)

Đốt cháy 12,15g kim loại nhôm trong bình kín có chứa 0,9.1023 phân tử O2. Phản ứng kết thúc thu được chất rắn A.
a. A gồm những chất nào? m bao nhiêu
b. Tính% theo khối lượng mỗi chất trong A
c. Hòa tan hết A bắng lượng vừa đủ dd H2SO4 9,8% được dd B. Tính C% muối trong dd B.
----
a) nAl = 12,15/27= 0,45(mol)
nO2= \(\frac{0,9.10^{23}}{6.10^{23}}=0,15\left(mol\right)\)
PTHH: 4 Al + 3 O2 -to-> 2 Al2O3
Ta có: 0,45/4 > 0,15/3
=> Al dư, O2 hết, tính theo nO2
Rắn A có Al dư, Al2O3.
nAl(dư)= 0,45 - 4/3 . 0,15= 0,25(mol)
=> mAl(DƯ)= 0,25. 27= 6,75(g)
nAl2O3= 2/3. nAl= 2/3. 0,15= 0,1(mol)
=> mAl2O3= 0,1.102= 10,2(g)
=> mAl= mAl(dư)+mAl2O3= 6,75+10,2= 16,95(g)
b) %mAl= \(\frac{6,75}{16,95}.100\approx39,823\%\)
=> %mAl2O3\(\approx100\%-39,823\%\approx60,177\%\)
c) PTHH: 2 Al + 3 H2SO4 -> Al2(SO4)3 + 3 H2
0,25_____________0,375____0,125_______0,375(mol)
Al2O3 + 3 H2SO4 -> Al2(SO4)3 + 3 H2O
0,1____0,3______0,1_____0,3(mol)
nH2SO4= 0,375+0,3= 0,675(mol)
=> mH2SO4= 0,675.98=66,15(g)
=> mddH2SO4= (66,15. 100)/9,8=675(g)
nAl2(SO4)3= 0,125+0,1= 0,225(mol)
=> mAl2(SO4)3= 0,225.342=76,95(g)
mddsau= mA+ mddH2SO4 - mH2= 16,95+ 675-0,375.2=691,2(g)
=> \(C\%ddAl_2\left(SO_4\right)_3=\frac{76,95}{691,2}.100\approx11,133\%\)

\(n_P=\dfrac{m_P}{M_P}=\dfrac{12,4}{31}=0,4mol\)
\(n_{O_2}=\dfrac{m_{O_2}}{M_{O_2}}=\dfrac{17}{32}=0,53125mol\)
\(4P+5O_2\rightarrow\left(t^o\right)2P_2O_5\)
0,4 < 0,53125 ( mol )
0,4 0,5 0,2 ( mol )
\(n_{O_2\left(du\right)}=0,53125-0,5=0,03125mol\)
Chất được tạo thành là P2O5
\(m_{P_2O_5}=n_{P_2O_5}.M_{P_2O_5}=0,2.142=18,4g\)

Bài 2: (chị Hương Giang làm cho bạn bài 1 rồi)
Áp dụng ĐLBTKL, ta có:
mM + mO2 = mM2On
=> mO2 = 4 - 2,4 = 1,6 (g)
nO2 = 1,6/32 = 0,05 (mol)
PTHH: 4M + nO2 -> (to) 2M2On
Mol: 0,2/n <--- 0,05
M(M) = 2,4/(0,2/n) = 12n (g/mol)
Xét:
n = 1 => Loại
n = 2 => M = 24 => Mg
n = 3 => Loại
Vạya M là Mg
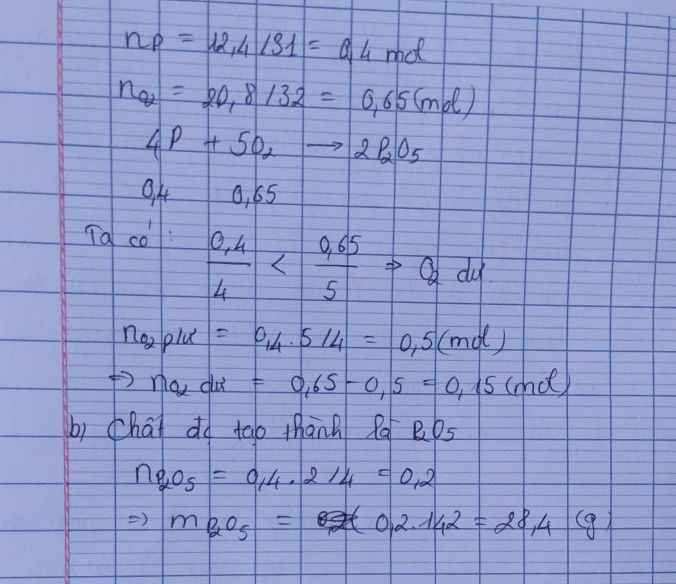

Đốt cháy 8,1 gam nhôm trong bình chứa 0,9.1023 phân tử oxi, được chất rắn A
a. Chất rắn A gồm những chất gì? Khôi lượng từng chất là bao nhiêu.
b. Tính % theo khối lượng mỗi chất trong hỗn hợp A.
------
a) nO2= \(\frac{0,9.10^{23}}{6.10^{23}}=0,15\left(mol\right)\)
nAl= 8,1/27= 0,3(mol)
PTHH: 4 Al + 3 O2 -to-> 2 Al2O3
Ta có: 0,3/4 > 0,15/3
=> O2 hết, Al dư, tính theo nO2
=> Rắn A gồm Al dư, Al2O3
nAl2O3= 2/3 . nO2= 2/3 . 0,15= 0,1(mol)
=> mAl2O3 = 0,1.102= 10,2(g)
nAl(dư)= 0,3 - 4/3 . 0,15= 0,1(mol)
=> mAl(dư)=0,1.27= 2,7(g)
b) %mAl(dư)= \(\frac{2,7}{2,7+10,2}.100\approx20,930\%\)
=> %mAl2O3\(\approx100\%-20,930\%\approx79,070\%\)
a) \(n_{Al}=\frac{8,1}{27}=0,3\left(mol\right)\)
\(n_{O2}=\frac{0,9.10^{23}}{6.10^{23}}=0,15\left(mol\right)\)
\(4Al+3O2-->2Al2O3\)
Lập tỉ lệ
\(n_{Al}\left(\frac{0,3}{4}\right)>n_{O2}\left(\frac{0,15}{3}\right)=>ALdư\)
Chất rắn sau pư là Al2O3 và Al dư
\(n_{Al2O3}=\frac{2}{3}n_{Al}=0,1\left(mol\right)\)
\(m_{Al2O3}=0,1.102=10,2\left(g\right)\)
\(n_{Al}=\frac{4}{3}n_{O2}=0,2\left(mol\right)\)
\(n_{Al}dư=0,3-0,2=0,1\left(mol\right)\)
\(m_{Al}dư=0,1.27=2,7\left(g\right)\)
b)\(\%m_{Al}dư=\frac{2,7}{2,7+10,2}.100\%=20,93\%\)
\(\%m_{Al2O3}=100-20,93=79,07\%\)