Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
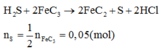
Chú ý: Không tồn tại muối sunfua của Al và Fe(III). H2S không phản ứng với AlCl3 nhưng nếu
![]()
Có sự khác nhau này do Fe3+ có tính oxi hóa mạnh còn Al3+ tính oxi hóa yếu

\(n_{Cu}=a\left(mol\right),n_{Fe}=b\left(mol\right)\)
\(m_X=64a+56b=16.2\left(g\right)\left(1\right)\)
\(n_{SO_2}=\dfrac{8.96}{22.4}=0.4\left(mol\right)\)
Bảo toàn e :
\(2a+3b=0.4\cdot2=0.8\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.0475,b=0.235\)
\(\%Cu=\dfrac{0.0475\cdot64}{16.2}\cdot100\%=18.76\%\)
\(\%Fe=81.24\%\)
\(b.\)
\(\dfrac{a}{b}=\dfrac{0.0475}{0.235}=\dfrac{19}{94}\)
\(\Rightarrow n_{Cu}=19x\left(mol\right),n_{Fe}=94x\left(mol\right)\)
\(m_X=19x\cdot64+94x\cdot56=22\left(g\right)\)
\(\Rightarrow x=\dfrac{11}{3240}\)
\(n_{H_2}=n_{Fe}=\dfrac{11}{3240}\cdot94=\dfrac{517}{1620}\left(mol\right)\)
\(V_{H_2}=7.15\left(l\right)\)

\(m_{tang}=44,6-28,6=16\left(g\right)=m_O\)
\(\Rightarrow n_O=1\left(mol\right)\)
\(2H+O\rightarrow H_2O\)
\(\Rightarrow n_H=2\left(mol\right)=2n_{H2SO4}\)
\(\Rightarrow n_{H2SO4}=1\left(mol\right)=n_{SO4}\)
\(\Rightarrow m_{SO4}=96\left(g\right)\)
m muối= m kim loại+ mSO4
\(=28,6+96=124,6\left(g\right)\)

Gọi số mol của NO2 và NO là a và b
Ta có hệ phương trình :
\(\left\{{}\begin{matrix}a+b=\frac{1,12}{22,4}\\\frac{46a+30b}{a+b}=16,75.2\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}a=0,01\\b=0,04\end{matrix}\right.\)
\(n_{HNO3}=n_{HNO3_{tao.muoi}}+n_{N\left(pu.khử\right)}=2n_{NO2}+4n_{NO}\)
\(=0,18\left(mol\right)\)
\(\Rightarrow CM_{HNO3}=0,65M\)
\(m_{muoi}=m_{pu}+m_{NO3}=\left(6,25-2,516\right)+\left(0,01.1+0,04.3\right).62\)
\(=11,794\left(g\right)\)

- Bảo toàn khối lượng => mO=63.2-0.15*64-x*56=53.6-x*56
=>nO=3.35-3.5*x
- Fe - 3e \(\rightarrow\) Fe3+ (1)
x 3x
O + 2e \(\rightarrow\) O2- (2)
(3.35-3.5*x) 6.7-7*x
Cu - 2e \(\rightarrow\) Cu2+ (3)
0.15 0.3
S6+ + 2e \(\rightarrow\) S4+ (4)
0.6 0.3
=> Bảo toàn mol e=>6.7-7*x+0.6 =3x + 0.3
=> x=0.7