Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
A. C + 4HNO3 đặc nóng → CO2 + 4NO2+ 2H2O
→Số oxi hóa của C tăng từ 0 lên +4 nên C là chất khử
B. C +2 H2SO4 đặc nóng → CO2+ 2SO2+ 2H2O
→Số oxi hóa của C tăng từ 0 lên +4 nên C là chất khử
C. CaO + 3C→CaC2+ CO
→ Số oxi hóa của C tăng từ 0 lên +2 (trong CO) và giảm từ 0 xuống -1 (trong CaC2) nên C vừa là chất khử vừa là chất oxi hóa.
D. C + O2 → CO2
→Số oxi hóa của C tăng từ 0 lên +4 nên C là chất khử

A. C + 2HNO3 → CO2 + 4NO2 + 2H2O.
B. C + 2H2SO4 (đặc, nóng) → CO2 + 2SO2 + 2H2O.
C. CaO + 3C → CaC2 + CO. Trong phản ứng, C từ số oxi hóa là O lên số oxi hóa +2 và xuống số oxi hóa -1 → C vừa thể hiện tính khử, vừa thể hiện tính oxi hóa.
Đáp án C

Từ tỉ khối hơi của Y và Z so với metan dễ dàng suy ra MY = 50,5;MZ = 85 => Y là CH3Cl và Z là CH2C12
Đề bài cho 2 số liệu tuyệt đối là khối lượng hỗn hợp X và số mol NaOH, ta cần tìm số mol của CH3C1 và CH2C12. Do đó có thể dùng phương pháp đại số lập 2 phương trình 2 ẩn giải bình thường. Gọi số mol CH3C1 là a, số mol CH2C12 là b
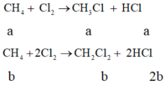
![]()
![]()
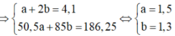
![]()
![]()
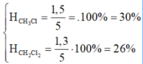
Đáp án D

Đáp án D
1) P2O5+ 3H2O→ 2 H3PO4
3) P2O5+ 3H2O→ 2 H3PO4
H3PO4+ NaOH → NaH2PO4+ H2O
H3PO4+ 2NaOH → Na2HP O4+ 2H2O
H3PO4+ 3NaOH → Na3PO4+ 3H2O
4) P2O5+ 3H2O→ 2 H3PO4
3AgNO3+ H3PO4→ Ag3PO4+ 3HNO3

\(n_{H_2}\approx0,35\left(mol\right)\)
\(n_{Cl_2}=0,375\left(mol\right)\)
\(Fe+2HCl-->FeCl_2+H_2\uparrow\)
x.........2x........................x..............x
\(2M+2nHCl-->2MCl_n+nH_2\uparrow\)
4x..........4xn.................4x................2xn
\(2M+nCl_2-->2MCl_n\)
4x.......2xn...................4x
\(2Fe+3Cl_2-->2FeCl_3\)
x..........1,5x..............x
\(x+2xn=\dfrac{7,84}{22,4}\Rightarrow2xn=\dfrac{7,84}{22,4}-x\left(1\right)\)
\(2xn+1,5x=0,375\left(2\right)\)
thay(1) vaog(2) => x=0,05
n=3
Thể tích Cl2 tác dụng vs M
\(V_{Cl_2}=2.3.0,05.22,4=6,72\left(l\right)\)
b) \(M=\dfrac{5,4}{4.0,05}=27\left(\dfrac{g}{mol}\right)\)
=> M: Al
\(n_{H_2}=0,1\left(mol\right)\)
\(V_{HCl}=400\left(ml\right)=0,4\left(l\right)\)
\(Zn+2HCl-->ZnCl_2+H_2\uparrow\)
0,1.......0,2...................0,1.............0,1
\(CM_{HCl}=\dfrac{0,2}{0,4}=0,5\left(M\right)\)
\(m_{ZnCl_2}=0,1.136=13,6\left(g\right)\)
b) \(n_{KOH}=\dfrac{50.22,4\%}{56.100\%}=0,2\left(mol\right)\)
\(n_{HCl}=0,2.0,5=0,1\left(mol\right)\)
\(HCl+KOH-->KCl+H_2O\)
\(\dfrac{0,1}{1}< \dfrac{0,2}{1}\) =>KOH dư
\(V_{KOH}=\dfrac{50}{1,25}=40\left(ml\right)=0,04\left(l\right)\)
\(CM_{KCl}=\dfrac{0,1}{0,2+0,04}=\dfrac{5}{12}\left(M\right)\)
\(CM_{KOH}=\dfrac{0,2-0,1}{0,2+0,04}=\dfrac{5}{12}\left(M\right)\)
Khi tác dụng với NaOH phản ứng xảy ra như sau:
\(2NaOH+Cl_2\rightarrow NaCl+NaClO+H_2O\)
Số oxi hóa của Cl từ 0 lên +1 trong NaClO và xuống -1 trong NaCl. Do vậy vừa xảy ra sự oxi hóa và sự khử Cl.