Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Oxit ở thể rắn: Magie(Mg)
b) Oxit ở thể lỏng: Hidro(H2)
c) Oxit ở thể khí:Cacbon(C), Metan(CH4), Cacbon oxit(CO).
a) Oxit ở thế rắn: Magiê
b) Oxit ở thể lỏng: Hiđro
c) Oxit ở thể khí: Cacbon, Metan, Cacbon oxit

Bài 1: Tính thể tích khí oxi (đktc) cần dùng để đốt cháy hoàn toàn 1 kg than đá chứa 96% cacbon và 4% tạp chất không cháy.
Theo gt ta có: $n_{C}=800(mol)$
$C+O_2\rightarrow CO_2$
Suy ra $n_{O_2}=800(mol)\Rightarrow V_{O_2}=17920(l)$
Bài 2: Cho những chất sau: Ccacbon, hiđro, magie, metan, cacbon oxit. Cho biết sự oxi hóa chất nào sẽ tạo ra:
A. Oxit ở thể rắn: Mg
B. Oxit ờ thể lỏng: $H_2$
C. Oxit ở thể khí: $C;CH_4;CO$

\(C+O_2\rightarrow CO_2\) tạo ra oxit ở thể khí
\(4Al+3O_2\rightarrow2Al_2O_3\) tạo oxit ở thể rắn
\(3Fe+2O_2\rightarrow Fe_3O_4\) tạo oxit ở thể rắn
\(4P+5O_2\rightarrow2P_2O_5\) tạo ra oxit ở thể khí ( là 1 chất khói trắng, 0 mùi)
\(CH_4+2O_2\rightarrow CO_2+2H_2O\) tạo ra oxit ở thể khí
\(C_2H_4+3O_2\rightarrow2CO_2+2H_2O\) tạo ra oxit ở thể khí
\(2C_2H_6O+5O_2\rightarrow2CO_2+6H_2O\) tạo ra oxit ở thể khí
cho hỏi là tại sao 3 cái cuối không phải oxit ở thể khí và lỏng ạ??

Mình nghĩ bạn nhầm đề rồi nhé! :D Ở câu a, b, c, d "oxit" chứ không phải "oxi" nhé!
Lần sau đăng đề nhớ đăng cho đúng đề, kiểm tra lại. Bạn đăng không đúng thì ngta không giúp được đâu =))
a) Oxi hóa sắt tạo ra oxit thể rắn
3Fe + 2O2 =to> Fe3O4
b) Oxi hóa cacbon tạo oxit thể khí
C + O2 =to> CO2
c) Oxi hóa hidro tạo oxit thể lỏng
2H2 + O2 =to> 2H2O
d) Oxi hóa C4H10 tạo oxit thể khí và thể lỏng
2C4H10 + 13O2 =to> 8CO2 + 10H2O

a) PTHH:
CuO + H2 =(nhiệt)=> Cu + H2O (1)
Fe2O3 + 3H2 =(nhiệt)=> 2Fe + 3H2O (2)
b) - Dựa vào định nghĩa chất khử và chất oxi hóa
=> Chất khử: H2
Chất Oxi hóa: CuO và Fe2O3
c) Lượng đồng có trong 6g hỗn hợp 2 kim loại thu được:mCu = 6g - 2,8g = 3,2g.
VH2 cần dùng theo phương trình phản ứng(1) = \(\dfrac{3,2}{64}\cdot64=1,12\left(l\right)\) =
VH2 cần dùng theo phương trình phản ứng(2) = \(\dfrac{2,8}{56}\cdot\dfrac{3}{2}\cdot22,4=1,68\left(l\right)\)
a.Phương trình phản ứng:
CuO + H2 Cu + H2O (1)
1mol 1mol 1mol 1mol
Fe2O3 + 3H2 3H2O + 2Fe (2)
1mol 3mol 3mol 2mol
b. + Chất khử là H2 vì chiếm oxi của chất khác;
+ Chất oxi hóa: CuO, Fe2O3 vì nhường oxi cho chất khác.
c. Số mol đồng thu được là: nCu = = 0,5 (mol)
Số mol sắt là: nFe = = 0,05 (mol)
Thể tích khí H2 cần dùng để khử CuO theo phương trình phản ứng (1) là: nH2 = nCu = 0,05 mol => VH2 = 22,4.0,05 = 1,12 (lít)
Khí H2 cần dùng để khử Fe2O3 theo phương trình phản ứng (2) là:
nH2 = nFe =
.0,05 = 0,075 mol
=>VH2(đktc) = 22,4.0,075 = 1,68 (lít)

a) Phương trình hóa học của các phản ứng:
H2 + CuO → Cu + H2O (1).
3H2 + Fe2O3 → 2Fe + 3H2O (2).
b) Trong phản ứng (1), (2) chất khử H2 vì chiếm oxi của chất khác, chất oxi hóa là CuO và Fe2O3 vì nhường oxi cho chất khác.
c) Khối lượng đồng thu được từ 6g hỗn hợp 2 kim loại thu được:
mCu = 6g - 2,8g = 3,2g, nCu = 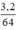 = 0,05 mol
= 0,05 mol
nFe = 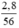 = 0,05 (mol)
= 0,05 (mol)
nH2 (1) = nCu = 0,05 mol ⇒ VH2(1) = 22,4 . 0,05 = 1,12 lít
nH2 (2) = 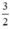 . nFe =
. nFe = 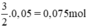 ⇒ VH2 (2) = 22,4 . 0,075 = 1,68 lít khí H2.
⇒ VH2 (2) = 22,4 . 0,075 = 1,68 lít khí H2.
VH2 = VH2(1) + VH2(2) = 1,12 + 1,68 = 2,8(l)

PTHH: \(Fe_3O_4+4CO\xrightarrow[]{t^o}3Fe+4CO_2\uparrow\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\uparrow\)
\(H_2+\dfrac{1}{2}O_2\xrightarrow[]{t^o}H_2O\)
Ta có: \(n_{Fe_3O_4}=\dfrac{23,2}{232}=0,1\left(mol\right)\) \(\Rightarrow n_{Fe}=0,3\left(mol\right)=n_{H_2SO_4}=n_{H_2}=n_{H_2O}\)
\(\Rightarrow\left\{{}\begin{matrix}V_{H_2}=0,3\cdot22,4=6,72\left(l\right)\\V_{ddH_2SO_4}=\dfrac{0,3}{0,5}=0,6\left(l\right)\\V_{H_2O}=\dfrac{0,3\cdot18}{D_{nước}}=5,4\left(ml\right)\end{matrix}\right.\)
*P/s: \(D_{nước}=1g/ml\)

1.Đưa que đóm đang cháy vào 4 chất khí: O2 bùng cháy sáng
Còn lại 3 chất khí CO,CO2,H2
Sục 3 chất khí vào dd \(Ca\left(OH\right)_2\)
-CO2: xuất hiện kết tủa trắng
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3\downarrow+H_2O\)
-H2,CO: không hiện tượng
Đưa 2 chất khí đi qua CuO ở nhiệt độ thích hợp và Ca(OH)2
-CO2: kết tủa trắng
-H2: không hiện tượng
\(CuO+CO\rightarrow\left(t^o\right)Cu+CO_2\)
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3\downarrow+H_2O\)
\(CuO+H_2\rightarrow\left(t^o\right)Cu+H_2\)
2.
\(n_{H_2}=\dfrac{0,448}{22,4}=0,02mol\)
\(Fe+HCl\rightarrow FeCl_2+H_2\)
0,02 0,02 ( mol )
\(m_{Fe}=0,02.56=1,12g\)
\(\Rightarrow m_{Cu}=1,76-1,12=0,64g\)
\(n_{Cu}=\dfrac{0,64}{64}=0,01mol\)
\(CuO+H_2\rightarrow\left(t^o\right)Cu+H_2O\)
0,01 0,01 ( mol )
\(m_{CuO}=0,01.80=0,8g\)
\(\Rightarrow m_{Fe_xO_y}=2,4-0,8=1,6g\)
\(Fe_xO_y+yH_2\rightarrow\left(t^o\right)xFe+yH_2O\)
\(\dfrac{1,6}{56x+16y}\) -----> \(\dfrac{1,6x}{56x+16y}\) ( mol )
Ta có:
\(\dfrac{1,6x}{56x+16y}=0,02\)
\(\Leftrightarrow1,6x=1,12x+0,32y\)
\(\Leftrightarrow3x=2y\)
\(\Leftrightarrow x=2;y=3\)
\(\Rightarrow CTHH:Fe_2O_3\)
\(\%m_{Fe_2O_3}=\dfrac{1,6}{2,4}.100=66,67\%\)
\(\%m_{CuO}=100\%-66,67\%=33,33\%\)
a)Mg
b)H2
c)C,CH4,CO
a, magiê(Mg)
b, hiđro(H2)
c,cacbon(C), mêtan(CH4), cacbon oxit(CO)