Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

- X là anđehit đơn chức
RCHO + 2AgNO3 + 3NH3 + H2O → RCOONH4 + 2Ag + 2NH4NO3
nAg = 0.02 mol => nRCHO = \(\dfrac{1}{2}\) nAg = 0,01 mol
MRCHO = 58,0 g/mol. R là C2H5 , X là CH3CH2CHO.

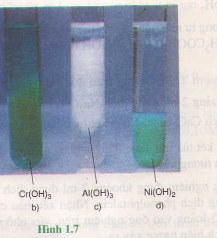
Cr(NO3)3 + 3NaOH(vừa đủ) → Cr(OH)3↓ + 3NaNO3 ;
AlCl3 + 3KOH (vừa đủ) → Al(OH)3↓ + 3KC1 ;
Ni(NO3)2 + 2NaOH → Ni(OH)2↓+ 2NaNO3.
nhìn cái ảnh này là thể hiện tự đăng rồi. Bữa trước môn sinh cũng thế chứ đâu

Hai chất 2,2 - đimetyl butan và 2,3 - đimetyl butan là:
A. Ankan. B. Đồng phân. C. Đồng đẳng. D. A và B.
Vì: Do hai chất này trong phân tử chỉ chứa nối đơn => là RH no => ankan
Do 2 chất này có PTK bằng nhau và có tình chất hoá học tương tự nhau ( vì chỉ thay đổi vị trí đính metyl ở C số 2 và 3 ) nên chúng là đồng phân của nhau.

104,48gam104,48gam
Giải thích các bước giải:
Sơ đồ phản ứng:
⎧⎪ ⎪ ⎪⎨⎪ ⎪ ⎪⎩AlMgFeOFe3O4+HNO3−−−−−→⎧⎪ ⎪ ⎪ ⎪ ⎪ ⎪⎨⎪ ⎪ ⎪ ⎪ ⎪ ⎪⎩NO,N2OH2O⎧⎪⎨⎪⎩Al(NO3)2Mg(NO3)2Fe(NO3)2to→⎧⎨⎩Al2O3MgOFe2O3+NO2+O2{AlMgFeOFe3O4→+HNO3{NO,N2OH2O{Al(NO3)2Mg(NO3)2Fe(NO3)2→to{Al2O3MgOFe2O3+NO2+O2
Oxi chiếm 20,22%20,22% khối lượng hỗn hợp.
mO=25,32%.25,32=5,12gammO=25,32%.25,32=5,12gam
→nO=0,32mol→nO=0,32mol
Gọi số mol của NONO và N2ON2O lần lượt là xx và yy mol
⎧⎨⎩x+y=3,58422,4=0,16mol30x+44y=0,16.2.15,875→{x=0,14y=0,02{x+y=3,58422,4=0,16mol30x+44y=0,16.2.15,875→{x=0,14y=0,02
Quy đổi hỗn hợp X thành các nguyên tố: Al,Mg,Fe,OAl,Mg,Fe,O
→mKl=25,32−5,12=20,2g→mKl=25,32−5,12=20,2g
→mO(cr)=30,92−20,2=10,72gam→mO(cr)=30,92−20,2=10,72gam
→nO=0,67mol→nO=0,67mol
3nAl+3nFe+2nMg=2nO(cr)3nAl+3nFe+2nMg=2nO(cr)
Gọi số mol của NH4NO3NH4NO3 là xx mol
Bảo toàn e:
3nAl+3nFe+2nMg=2nO+8nNH4NO3+3nNO+8nN2O3nAl+3nFe+2nMg=2nO+8nNH4NO3+3nNO+8nN2O
0,67.2=2.0,32+8nNH4NO3+3.0,14+0,02.80,67.2=2.0,32+8nNH4NO3+3.0,14+0,02.8
→nNH4NO3=0,015mol→nNH4NO3=0,015mol
Khối lượng muối:
m=mKl+mNO−3+mNH4NO3m=mKl+mNO3−+mNH4NO3
=20,2+0,67.2.62+0,015.80=104,48gam

Theo thuyết A-rê-ni-ut thì:
– Axit là chất khi tan trong nước phân li ra cation H+
Ví dụ: HCl → H+ + Cl–
– Bazơ là chất khi tan trong nước phân li ra anion OH–
Ví dụ : NaOH → Na+ + OH–
– Hiđroxit lưỡng tính là hiđroxit khi tan trong nước vừa có thể phân li như axit, vừa có thể phân li như bazơ.
Zn(OH)2 ⇔ Zn2+ +20H– ; Zn(OH)2 ⇔ ZnO2-2 + 2H+
2. Những axit mà tan trong nước phân li nhiều nấc ra ion H+ gọi là các axit nhiều nấc.
Ví dụ : H2SO4, H3PO4….
Những bazơ khi tan trong nước phân li nhiều nấc ra ion OH– gọi là các bazơ nhiều nấc. Ví dụ : Mg(OH)2, Ca(OH)2,….
3. Muối là hợp chất, khi tan trong nước phân li ra cation kim loại (hoặc cation NH4+) và anion gốc axit. Ví dụ : Na2CO3 → 2Na+ + CO32-
Muối trung hòa là muối mà anion gốc axit không có khả năng phân li ra ion H+. Muối axit là muối mà anion gốc axit có khá năng phân li ra ion H+.
Sự điện li cùa muối trong nước tạo cation kim loại (hoặc NH4+ , ion phức) và anion gốc axil.

- Tạo thành chất kết tủa: NH4Cl + AgNO3 → NH4NO3 + AgCl\(\downarrow\)
Ag+ + cl‑ \(\rightarrow\) AgCl\(\downarrow\)
- Tạo thành chất điện li yếu: NaOH + HCl \(\rightarrow\)NaCl + H2O
H+ + OH– \(\rightarrow\) H2O
- Tạo thành chất khí: K2CO3 + 2HCl \(\rightarrow\) 2KCl + CO2\(\uparrow\) + H2O
2H+ + CO32– → CO2\(\uparrow\) + H2O
- Tạo thành chất kết tủa: NH4Cl + AgNO3 \(\rightarrow\) NH4NO3 + AgCl\(\downarrow\)
Ag+ + cl‑ → AgCl\(\downarrow\)
- Tạo thành chất điện li yếu: NaOH + HC1 \(\rightarrow\)NaCl + H2O
H+ + OH– \(\rightarrow\)H2O
- Tạo thành chất khí: K2CO3 + 2HC1 \(\rightarrow\) 2KC1 + CO2\(\uparrow\) + H2O
2H+ + CO32– \(\rightarrow\) CO2\(\uparrow\) + H2O
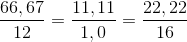 = 4 :8 : 1
= 4 :8 : 1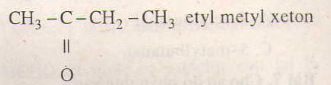
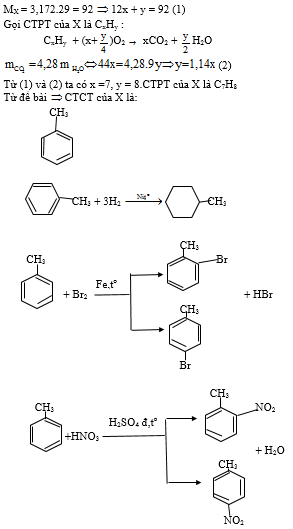
Đáp án D
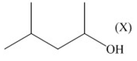
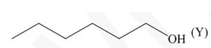
Hai chất X và Y đều có công thức cấu tạo C4H9OH nhưng khác nhau về sự phân bố không gian của nhóm -OH trong phân tử