Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

X: P, N, E ; Y: P’, N’, E’
Ta có: P=N=E và P’=N’=E’
Trong hợp chất XY2, X chiếm 50% về khối lượng nên: X/2Y = 50/50 → (P+N)/2(P’+N’) = 1 → P=2P’.
Số proton trong XY2 là 32 nên P+2P’=32
→ P=2P’ và P+2P’=32 => P=16 và P’=8
→ Hợp chất SO2S: 1s22s22p63s23p4 => Ô 16, chu kì 3, nhóm VIA
O: 1s22s22p4 => Ô 8, chu kì 2, nhóm VIA

Nguyên tố có số thự tự 37 có cấu hình như sau : [Kr] 5s1.
Vậy nguyên tố thuộc chu kì 5 ,nhóm IA

Số mol HCl = V1 mol
Số mol NaOH = 2V2 mol
Trường hợp 1: Dung dịch X chứa HCl dư
HCl + NaOH → NaCl + H2O
2V2 2V2
3HCl + Al(OH)3 → AlCl3 + 3H2O
3a a
Số mol HCl = 2V2 + 3a = V1
Trường hợp 2: Dung dịch X chứa NaOH
HCl + NaOH → NaCl + H2O
V1 V1
Al(OH)3 + NaOH → NaAlO2 + 2H2O
a a
Số mol NaOH = V1 + a = 2V2

Số mol HCl = V1 mol
Số mol NaOH = 2V2 mol
Trường hợp 1: Dung dịch X chứa HCl dư
HCl + NaOH → NaCl + H2O
2V2 2V2
3HCl + Al(OH)3 → AlCl3 + 3H2O
3a a
Số mol HCl = 2V2 + 3a = V1
Trường hợp 2: Dung dịch X chứa NaOH
HCl + NaOH → NaCl + H2O
V1 V1
Al(OH)3 + NaOH → NaAlO2 + 2H2O
a a
Số mol NaOH = V1 + a = 2V2
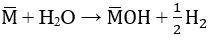

Đáp án B
Ag có Z = 47. Cấu hình của Ag là [Kr]4d105s1
→ Ag ở ô 47, chu kì 5, e cuối cùng điền vào phân lớp 4d nên Ag Є IB