Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
ZX = 11 có cấu hình e lớp ngoài cùng là 3s1
ZY = 11 có cấu hình e lớp ngoài cùng là 3s2
ZZ = 19 có cấu hình e lớp ngoài cùng là 4s1
Trong cùng 1 nhóm tính kim loại tăng dần theo chiều tăng của điện tích hạt nhân do đó tính bazo tương ứng của X’ <Z’
Trong cùng 1 CK tính kim loại giảm dần theo chiều tăng của điện tích hạt nhân do đó tính bazo tương ứng của X’>Y’

Bài này không cần tìm X, Y, Z vì người ta chỉ hỏi thứ tự sắp xếp tính kim loại của chúng. Vì vậy có thể làm như sau:
Vì tổng số hạt của 3 nguyên tử X, Y và Z là 134 nên suy ra cả 3 kim loại này đều thuộc chu kỳ lớn (4, 5, 6, 7).
Số hạt mang điện của Y nhiều hơn của X là 14, điều này chứng tỏ X, Y thuộc 2 chu kỳ liên tiếp và Y thuộc nhóm nhỏ hơn X, tức là Y có tính kl mạnh hơn X.
Số hạt mang điện của Z nhiều hơn của X là 2 chứng tỏ, X và Z thuộc cùng một chu kỳ và tính kl của X > Z.
Như vậy, Z < X < Y (B).
cảm ơn Pham Van Tien những thầy mk bảo phải tìm X , Y , Y

Gọi công thức chung của 3 kim loại là R, vì là kiêm loại kiềm nên R hóa trị I.
R + H2O\(\rightarrow\) ROH +\(\frac{1}{2}\)H2
Ta có: nH2=\(\frac{11,2}{22,4}\)=0,5 mol \(\rightarrow\) nR=2nH2=1mol
\(\rightarrow\)M R=\(\frac{10}{1}\)=10 đvC
\(\rightarrow\)7<10<23\(\rightarrow\) X phải là Li \(\rightarrow\) Y là Na \(\rightarrow\) Z là K

B
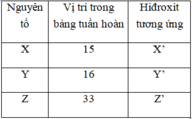
Ta có: X và Y thuộc cùng chu kỳ 3, Z X < Z Y → Tính kim loại X > Y.
X và Z thuộc cùng 1 nhóm IA; Z X < Z Z → Tính kim loại Z > X.
→ Chiều tăng dần tính kim loại là: Y < X < Z;
Chiều tăng dần tính bazơ là: Y’ < X’ < Z’.