Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

nMg = \(\dfrac{4,8}{24}=0,2\left(mol\right)\)
PTHH: Mg + H2SO4 ---> MgSO4 + H2
Theo PT: \(n_{H_2}=n_{Mg}=0,2\left(mol\right)\)
=> \(V_{H_2}=0,2.22,4=4,48\left(lít\right)\)
\(n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\)
PTHH: Mg + 2HCl → MgCl2 + H2
Mol: 0,2 0,2
\(V_{H_2}=0,2.22,4=4,48\left(l\right)\)

nH2 = 4,48 : 22,4 = 0,2 mol
gọi x,y lần lượt là số mol của Fe và Mg
PTHH : Fe + 2HCl → FeCl2 + H2
x mol 2x mol x mol
Mg + 2HCl → MgCl2 + H2
y mol 2y mol y mol
Ta có hệt phương trình:
\(\begin{cases}56x+24y=8\\x+y=0,2\end{cases}\)
Giải hệ phương trình ta có : x= 0,1 ; y = 0,1
Thể tích HCl là : VHCl = ( 2x + 2y ) . 22,4
= ( 2.0,1 + 2.0,1 ) . 22,4 = 8,96 lit
Khối lượng Mg là : mMg = 0,1 . 24 = 2,4 g
Khối lượng Fe là : mFe = 0,1 .56 = 5,6 g
@Vy Kiyllie bài này hình như thầy bảo kh đk giải hệ pt thỳ f

\(n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\\ Mg+2HCl\rightarrow MgCl_2+H_2\\ n_{H_2}=n_{Mg}=0,2\left(mol\right)\\ n_{CuO}=\dfrac{20}{80}=0,25\left(mol\right)\\ CuO+H_2\underrightarrow{^{to}}Cu+H_2O\\ Vì:\dfrac{0,25}{1}>\dfrac{0,2}{1}\\ \Rightarrow CuOdư\\ \Rightarrow n_{Cu}=n_{H_2}=0,2\left(mol\right)\\ m_{Cu}=0,2.64=12,8\left(g\right)\)
\(n_{Mg}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
Pt : \(Mg+2HCl\rightarrow MgCl_2+H_2|\)
1 2 1 1
0,2 0,2
\(n_{H2}=\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
\(n_{CuO}=\dfrac{20}{80}=0,25\left(mol\right)\)
Pt : \(H_2+CuO\rightarrow\left(t_o\right)Cu+H_2O|\)
1 1 1 1
0,2 0,25 0,2
Lập tỉ số so sánh : \(\dfrac{0,2}{1}< \dfrac{0,25}{1}\)
⇒ H2 phản ứng hết , CuO dư
⇒ Tính toán dựa vào số mol của H2
\(n_{Cu}=\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
⇒ \(m_{Cu}=0,2.64=12,8\left(g\right)\)
Chúc bạn học tốt

\(a.Mg+2HCl\rightarrow MgCl_2+H_2\\ b.n_{H_2}=0,2\left(mol\right)\\ TheoPT:n_{Mg}=n_{H_2}=0,2\left(mol\right)\\ \Rightarrow m_{Mg}=0,2.24=4,8\left(g\right)\\ c.n_{HCl}=2n_{H_2}=0,4\left(mol\right)\\ \Rightarrow m_{HCl}=0,4.36,5=14,6\left(g\right)\)

PTHH: \(Mg+H_2SO_4\rightarrow MgsO_4+H_2\uparrow\)
Ta có: \(n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)=n_{MgSO_4}=n_{H_2SO_4}\) \(\Rightarrow\left\{{}\begin{matrix}m_{MgSO_4}=0,2\cdot120=24\left(g\right)\\V_{H_2}=0,2\cdot22,4=4,48\left(l\right)\\C\%_{H_2SO_4}=\dfrac{0,2\cdot98}{294}\cdot100\%\approx6,67\%\end{matrix}\right.\)
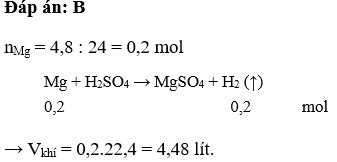
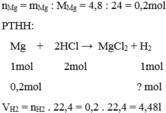
Ta có: \(n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\)
PT: \(Mg+2HCl\rightarrow MgCl_2+H_2\)
____0,2__________________0,2 (mol)
\(\Rightarrow V_{H_2}=0,2.22,4=4,48\left(l\right)\)
Bạn tham khảo nhé!