Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

nCaO=0.098mol;nCO2=0.05mol
PTHH:CaO+H2O->Ca(OH)2(1)
Ca(OH)2+CO2->CaCO3+H2O(2)
Có thể:CaCO3+CO2+H2O->Ca(HCO3)2(3)
Từ (1)->nCa(OH)2=nCaO=0.098mol
Ở (2) nCO2<nCa(OH)2 nên CO2 hết,Ca(OH)2 dư.<=>không xảy ra (3)
Từ (2)->nCaCO3=nCO2=0.05mol<=>5g
nCa(OH)2 dư=0.048mol<=>3.552g

Khối lượng các chất sau phản ứng :
Số mol các chất đã dùng :
n SO 2 = 1,12/22,4 = 0,05 mol; n Ca OH 2 = 0,1x700/1000 = 0,07 mol
Theo phương trình hoá học, lượng Ca OH 2 đã dùng dư. Do đó khối lượng các chất sau phản ứng được tính theo lượng SO 2
0,05 mol SO 2 tác dụng với 0,05 mol Ca OH 2 sinh ra 0,05 mol CaSO 3 và dư 0,07 - 0,05 = 0,02 (mol) Ca OH 2
Khối lượng các chất sau phản ứng là :
m CaSO 3 = 120 x 0,05 = 6 (gam)
m Ca OH 2 = 74 x 0,02 = 1,48 (gam)

a,\(n_{CaO}=\dfrac{3,92}{56}=0,07\left(mol\right);n_{CO_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
PTHH: CaO + H2O → Ca(OH)2
Mol: 0,07 0,07
PTHH: CO2 + Ca(OH)2 → CaCO3 + H2O
Mol: 0,07 0,07 0,07
Ta có:\(\dfrac{0,5}{1}>\dfrac{0,07}{1}\) ⇒ CO2 dư, Ca(OH)2 pứ hết
\(C\%_{ddCa\left(OH\right)_2}=\dfrac{0,07.90.100\%}{3,92+700}=0,89\%\)
b,\(m_{CaCO_3}=0,07.100=7\left(g\right)\)
\(m_{CO_2dư}=\left(0,5-0,07\right).44=18,92\left(g\right)\)

Mình gợi ý nhé ! Bài này cũng tương tự như các bài khác thôi .
Theo đề bài ta có : \(nHCl=1.0,5=0,5\left(mol\right)\)
Gọi x ,y lần lượt là số mol của Na2CO3 và NaHCO3
Ta có PTHH :
\(\left(1\right)Na2CO3+2HCl\rightarrow NaCl+H2O+CO2\)
xmol....................2xmol.....xmol.....................xmol
\(\left(2\right)NaHCo3+HCl\rightarrow NaCl+H2O+Co2\)
ymol.....................ymol.......ymol.....................ymol
Ta có HỆ PT : \(\left\{{}\begin{matrix}\dfrac{x}{1}+\dfrac{y}{1}=0,3\left(a\right)\\2x+y=0,5\left(b\right)\end{matrix}\right.=>\left\{{}\begin{matrix}x=?\\y=?\end{matrix}\right.\)
a) Tìm được x và y rồi thì => giá trị của V
b) Tìm được x và y thì => nCO2 = ( x+ y) = ?
Ta xét T = \(\dfrac{nNaOH}{nCO2}=\dfrac{0,3}{x+y}=?\)
TH 1 : nếu T \(\le1\) => tạo muối axit
TH2 : nếu 1 < T < 2 => tạo 2 muối
TH 3 : nếu T \(\ge\) 2 => tạo muối trung hòa
Rồi sau đó tính được giá trị của m
a) nHCl = \(\dfrac{500.1}{1000}=0,5\left(mol\right)\)
\(n_{Na_2CO_3}\) = \(\dfrac{300.1}{1000}=0,3\left(mol\right)\)
\(n_{NaHCO_3\left(bđ\right)}=\dfrac{300.1}{1000}=0,3\left(mol\right)\)
PTHH:
Na2CO3 + HCl → NaHCO3 + NaCl (1)
0,3..............0,5 (mol)
Tỉ lệ: \(\dfrac{0,3}{1}< \dfrac{0,5}{1}\)
=> HCl dư
=> nHCl (dư) = 0,5 - 0,3 = 0,2 (mol)
và: \(n_{NaHCO_3\left(2\right)}=n_{NaHCO_3\left(bđ\right)}+n_{NaHCO_3\left(1\right)}\) = 0,3 + 0,3 = 0,6 (mol)
PTHH:
HCl + NaHCO3 → NaCl + CO2 ↑ + H2O
0,2.........0,6 (mol)
Tỉ lệ: \(\dfrac{0,2}{1}< \dfrac{0,6}{1}\)
=> NaHCO3 dư
=> \(n_{CO_2}=n_{HCl}=0,2\left(mol\right)\)
Vậy: = VCO2 = 0,2 . 22,4 = 4,48 (l)
b) nCO2 = 0,2 (mol) (theo câu a)
nNaOH = \(\dfrac{300.1}{1000}=0,3\left(mol\right)\)
Đặt T =\(\dfrac{n_{NaOH}}{n_{CO_2}}=\dfrac{0,3}{0,2}=1,5\)
Ta thấy: 1 < T < 2 (vì 1 < 1,5 < 2)
=> Tạo muối Na2CO3 và NaHCO3
Đặt nNa2CO3 = x (mol) ; nNaHCO3= y (mol)
PT:
CO2 + NaOH → Na2CO3 + H2O
x.............2x..............x............x (mol)
CO2 + NaOH → NaHCO3
y..............y..............y (mol)
Ta có hệ phương trình:
\(\left\{{}\begin{matrix}x+y=0,2\\2x+y=0,3\end{matrix}\right.\) => x = y = 0,1 (mol)
=> mNa2CO3= 0,1 . 106 = 10,6 (g)
mNaHCO3 = 0,1 . 84 = 8,4 (gam)
Vậy m = 10,6 + 8,4 = 19 (g)

Fe3O4+4CO=>3Fe+ 4CO2
CuO+CO=>Cu+CO2
Cr B gồm Fe Cu
HH khí D gồm CO dư và CO2
CO2 +Ca(OH)2=>CaCO3+H2O
p/100 mol<= p/100 mol
2CO2+Ca(OH)2 => Ca(HCO3)2
p/50 mol
Ca(HCO3)2+ 2NaOH=>CaCO3+ Na2CO3+2H2O
p/100 mol p/100 mol
Tổng nCO2=0,03p mol=nCO
=>BT klg
=>m+mCO=mCO2+mB=>mB=m+0,84p-1,32p=m-0,48p
c) hh B Fe+Cu
TH1: Fe hết Cu chưa pứ cr E gồm Ag Cu
dd Z gồm Fe(NO3)2
Fe+2Ag+ =>Fe2+ +2Ag
TH2:Cu pứ 1p cr E gồm Cu và Ag
Fe+2Ag+ => Fe2+ +2Ag
Cu+2Ag+ =>Cu2+ +2Ag
Dd Z gồm 2 muối của Fe2+ và Cu2+

\(n_{CO_2}=\dfrac{0.56}{22.4}=0.025\left(mol\right)\)
\(n_{KOH}=0.1\cdot0.6=0.06\left(mol\right)\)
\(2KOH+CO_2\rightarrow K_2CO_3+H_2O\)
\(0.05..........0.025.......0.025\)
\(m_{K_2CO_3}=0.025\cdot138=3.45\left(g\right)\)
\(C_{M_{KOH\left(dư\right)}}=\dfrac{0.01}{0.1}=0.1\left(M\right)\)
\(C_{M_{K_2CO_3}}=\dfrac{0.025}{0.1}=0.25\left(M\right)\)

Chọn C

S O 2 hết, Ca( O H ) 2 dư, phản ứng tạo muối CaS O 3
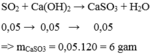

a, \(Na_2SO_3+H_2SO_4\rightarrow Na_2SO_4+SO_2+H_2O\)
\(K_2SO_3+H_2SO_4\rightarrow K_2SO_4+SO_2+H_2O\)
Ta có: \(n_{SO_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
Theo PT: \(n_{H_2SO_4}=n_{SO_2}=0,3\left(mol\right)\)
\(\Rightarrow m_{ddH_2SO_4}=\dfrac{0,3.98}{20\%}=147\left(g\right)\)
b, Ta có: 126nNa2SO3 + 158nK2SO3 = 44,2 (1)
Theo PT: \(n_{SO_2}=n_{Na_2SO_3}+n_{K_2SO_3}=0,3\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{Na_2SO_3}=0,1\left(mol\right)\\n_{K_2SO_3}=0,2\left(mol\right)\end{matrix}\right.\)
Có: m dd sau pư = 44,2 + 147 - 0,3.64 = 172 (g)
\(\Rightarrow\left\{{}\begin{matrix}C\%_{Na_2SO_3}=\dfrac{0,1.126}{172}.100\%\approx7,33\%\\C\%_{K_2SO_3}=\dfrac{0,2.158}{172}.100\%\approx18,37\%\end{matrix}\right.\)
c, \(n_{Ba\left(OH\right)_2}=0,5.1=0,5\left(mol\right)\)
\(\Rightarrow\dfrac{n_{SO_2}}{n_{Ba\left(OH\right)_2}}=0,6< 1\) → Pư tạo BaSO3.
PT: \(SO_2+Ba\left(OH\right)_2\rightarrow BaSO_3+H_2O\)
\(n_{BaSO_3}=n_{SO_2}=0,3\left(mol\right)\Rightarrow m_{BaSO_3}=0,3.217=65,1\left(g\right)\)
Ta có:
\(n_{CaO}=\frac{3,92}{56}=0,07\left(mol\right)\)
\(PTHH:CaO+H_2O\rightarrow Ca\left(OH\right)_2\)
\(\Rightarrow n_{Ca\left(OH\right)2}=n_{CaO}=0,07\left(mol\right)\)
\(\Rightarrow CM_{Ca\left(OH\right)2}=\frac{0,07}{0,8}=0,0875M\)
\(\left\{{}\begin{matrix}n_{Ca\left(OH\right)2}=0,0875.0,5==0,04375\left(mol\right)\\n_{CO2}=\frac{1,12}{22,4}=0,05\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow T=\frac{n_{Ca\left(OH\right)2}}{n_{CO2}}=0,875\)
\(0,5< T< 0,75\Rightarrow\) Chỉ tạo 2 muối
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\)
0,04375____0,05______0,04375______
\(CaCO_3+H_2O+CO_2\rightarrow Ca\left(HCO_3\right)_2\)
0,00625___________0,00625____0,00625
\(\Rightarrow\left\{{}\begin{matrix}m_{CaCO3}=3,75\left(g\right)\\m_{Ca\left(HCO3\right)2}=1,0125\left(g\right)\end{matrix}\right.\)