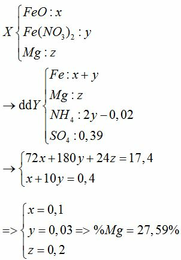Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Tóm tắt:
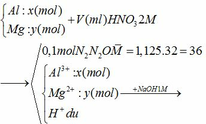
Gọi số mol của N2 và N2O lần lượt là
a và b (mol)
Ta có:
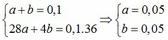


ne (KL nhường) = ne(N+5 nhận)
=> 2x + 3y = 0,5 + 0,4 (1)
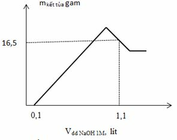
Từ đồ thị ta thấy tại giá trị V= 0,1 (lít) tức nNaOH = 0,1 (mol) mới bắt đầu xuất hiện kết tủa=> lượng NaOH này chính là lượng để trung hòa HNO3 dư sau phản ứng=> nHNO3 dư = nNaOH0,1 (mol) Ta thấy tại giá trị V= 1,1 (lít) tức nNaOH = 1,1 (lít) đồ thị đi lên cực đại sau đó lại đi xuống => kết tủa đạt cực đại sau đó bị hòa tan 1 phần ( chỉ có Al(OH)3 bị hoàn tan) Khi cho NaOH từ từ vào dung dich .Z xảy ra phản ứng:
H+ + OH- → H2O
0,1 → 0,1 (mol)
Mg2+ + 2OH- → Mg(OH)2↓
x → 2x (mol)
Al3+ + 3OH- → Al(OH)3↓
y → 3y →y (mol)
Al(OH)3↓ + OH- → AlO2- + 2H2O
(y – z ) → (y –z) (mol)
Gọi số mol của Al(OH)3 còn lại không bị hoàn tan là z (mol)
=> ta có: ∑ nNaOH = nH+dư + 2nMg2+ + 4nAl3+ - nAl(OH)3
=> 0,1 +2x + 4y – z = 1,1 (2)
Mặt khác: ∑ mkết tủa = mMg(OH)2 + mAl(OH)3 chưa hòa tan
=> 58x + 78z = 16,5 (3)
Từ (1), (2) và (3) => x = 0,2 ; y = 0,15 và z = 0,1 (mol)
=> m = mAl + mMg = 0,2.27 + 0,15.24 = 9 (g)
nHNO3 = nHNO3 dư + 2nN2 + 2nN2O + 3nAl(NO3)3 + 2nMg(NO3)2 = 0,1 + 2.0,05 + 2. 0,05 + 3.0,2 + 2.0,15 = 1,2 (mol)
=> VHNO3 = n : CM = 1,2 : 2 = 0,6 (lít) = 600 (ml)

(a)- Khi cho E tác dụng với NaHCO3 sinh ra V lít khí (CO2) và muối natri của X => X là axit
- Ta thấy thể tích khí sinh ra khi cho E tác dụng với Na (khí H2) lớn hơn 0,5 lần thể tích khí khi cho E tác dụng với NaHCO3 (khí CO2) => Y là ancol
Vậy E gồm axit X, ancol Y và este Z (tạo bởi X, Y)
Giả sử V lít tương ứng với 1 (mol) khí
+ nCO2 = n-COOH = 1 (mol)
+ nH2 = 0,5n-COOH + 0,5n-OH => 0,75 = 0,5.1 + 0,5n-OH => n-OH = 0,5 (mol)
+ n hỗn hợp = 2nH2 = 1,5 mol => nX = nY = nZ = 1,5:3 = 0,5 mol
Số chức của axit X là: 1 : 0,5 = 2
Số chức của ancol Y là: 0,5 : 0,5 = 1
=> Este Z có 2 chức
* Đốt cháy muối natri của X:
Muối natri của X có dạng RO4Na2
Gọi số mol muối của X là x (mol)
BTNT Na: nNa2CO3 = n muối = x (mol)
BTNT O: 4n muối + 2nO2 = 2nCO2 + nH2O + 2nNa2CO3
=> 4x + 2nO2 = 0,03.2 + 0,02 + 3x => nO2 = 0,04 – 0,5x (mol)
BTKL: m muối + mO2 = mCO2 + mH2O + mNa2CO3
=> 1,62 + 32(0,04 - 0,5x) = 0,03.44 + 0,02.18 + 106x
=> x = 0,01 mol
=> M muối = 162 => R + 16.4 + 23.2 = 162 => R = 28 => CTPT của X là C4H6O4
* Đun nóng Y với H2SO4 đặc thu được Y1 có tỉ khối so với Y là 34/43 => phản ứng tách nước tạo anken
=> MY1 = MY – 18
=> dY1/Y = (MY-18)/MY = 34/43 => MY = 86 (C5H10O)
Mà khi đun Y1 với KMnO4/H2SO4 thu được Y2 duy nhất, không có khí thoát ra, Y2 có cấu tạo mạch thẳng và là điaxit nên Y1 có cấu tạo mạch vòng, chứa 1 liên kết đôi.
- Cấu tạo Y1:
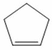
- Cấu tạo Y2: HOOC-(CH2)3-COOH
- Cấu tạo Y: 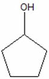
- Cấu tạo X:
HOOC-CH2-CH2-COOH hoặc HOOC-CH(CH3)-COOH
- Cấu tạo Z:
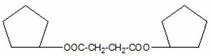
Hoặc
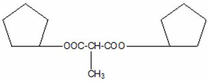
(b)Giả sử số mol mỗi chất trong ½ hỗn hợp G:
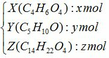
- Khối lượng của ½ hỗn hợp G:
118x + 86y + 254z = 7,8 (1)
- Đốt cháy phần 1 cần nO2 = 9,408 : 22,4 = 0,42 mol:
C4H6O4 + 3,5 O2 → 4CO2 + 3H2O
x 3,5x
C5H10O + 7O2 → 5CO2 + 5H2O
y 7y
C14H22O4 + 17,5O2 → 14CO2 + 11H2O
z 17,5z
Ta có: nO2 = 0,42 => 3,5x + 7y + 17,5z = 0,42 (2)
- Phần 2 tác dụng vừa đủ với nNaOH = 0,04.2 = 0,08 mol:
C2H4(COOH)2 + 2NaOH → C2H4(COONa)2 + 2H2O
x 2x x
C2H4(COOC5H9)2 + 2NaOH → C2H4(COONa)2 + 2C5H9OH
z 2z z 2z
nNaOH = 2nX + 2nZ => 2a + 2c = 0,08 (3)
Từ (1) (2) (3) ta có hệ phương trình:
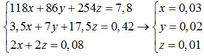
Sau phản ứng thu được:
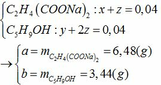

\(n_{CO_2}=a;n_{NO_2}=b;M_B=1,425.32=45,6\left(g\cdot mol^{^{ }-1}\right)\)
Từ sơ đồ đường chéo, rút ra được:
\(\dfrac{a}{b}=\dfrac{1}{4}\\ b=4a\\ n_{FeCO_3}=n_{CO_2}=a\left(mol\right)\\BTe^{^{ }-}:a+15n_{FeS_2}=b\\ n_{FeS_2}=\dfrac{b-a}{15}=\dfrac{3a}{15}=0,2a\left(mol\right)\\ \%n_{FeCO_3}=\dfrac{a}{a+0,2a}.100\%=83,33\%\\ \%n_{FeS_2}=16,67\%\)
Phương trình thiếu sản phẩm H2SO4, FeCO3 + HNO3 dư cho ra muối Fe 3+ và NO2.
Rồi đáp án cuối cùng là gì?

Ta có : C1=2C2
=> Gọi nH2SO4 =x
=> n HCl = 2x
Bảo toàn nguyên tố H :\(n_{HCl}.1+n_{H_2SO_4}.2=n_{H_2}.2\)
\(\Rightarrow2a+2a=\dfrac{13,44}{22,4}=0,6.2\)
=>a = 0,3(mol)
=> CMHCl = \(\dfrac{0,6}{0,3}=2M\); CMH2SO4 = \(\dfrac{0,3}{0,3}=1M\)
Dung dịch B gồm : Mg 2+ , Al3+ , Cl- , SO4 2-
\(n_{Cl^-}=n_{HCl}=0,6\left(mol\right);n_{SO_4^{2-}}=n_{H_2SO_4}=0,3\left(mol\right)\)
Bảo toàn điện tích cho dung dịch B:
\(n_{Mg}.2+n_{Al}.3=0,6+0,3.2\) (1)
Theo đề bài : \(24.n_{Mg}+27.n_{Al}=12,6\) (2)
Từ (1), (2)=> \(\left\{{}\begin{matrix}n_{Mg}=0,3\\n_{Al}=0,2\end{matrix}\right.\)
=> \(\%m_{Mg}=\dfrac{0,3.24}{12,6}.100=57,14\%\)
=> % m Al = 100 -57.14 = 42,86%

m dd A = 4 . 79,3 = 317,2g
Qui đổi hỗn hợp FeO, Fe2O3, Fe3O4về Fe3O4 có số mol là a
Ta có 232a + (a . 4 . 1,5 . 98) : 0,2 = 317,2
=> a = 0,1 mol
Dd ban đầu
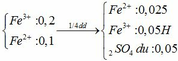
Phần 1:
8H2SO4 + 2KMnO4 + 10FeSO4 → 5Fe2(SO4)3 + 8H2O + 2MnSO4 + K2SO4
0,05 0,025
=> FeSO4 phản ứng hết
=> nKMnO4 = 0,005mol
=> V1= 0,1 lít = 100ml
Phần 2:
2Fe2+ + Br2 → 2Fe3+ + 2Br-
0,025 0,0125
=> V2 = 0,25 lít = 250ml
Phần 3:
2Fe3+ + 2I- → 2Fe2+ + I2
0,05 0,05
=> V3 = 1 lít = 1000ml
Phần 4:
Fe2+ + CO32- → FeCO3↓
0,025 0,025 0,025
2Fe3+ + 3CO32- + 3H2O → 2Fe(OH)3 + 3CO2
0,05 0,075 0,05 0,075
2H+ + CO32- →CO2 + H2O
0,1 0,05 0,05
=> nCO2 = 0,125
=> V4 = 2,8 lít
m kết tủa = mFeCO3 + mFe(OH)3 = 8,25g

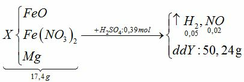
Vì Mg có tính khử rất mạnh nên trong Y có thể có muối (NH4)2SO4
BTNT N: 2nFe(NO3)2 = nNO + nNH4 => 2y = 0,02 + nNH4 => nNH4 = 2y – 0,02
BTNT H: 2nH2SO4 = 2nH2 + 4nNH4 + 2nH2O => 2 . 0,39 = 2 . 0,05 + 4 (2y – 0,02) + 2nH2O
=> nH2O = 0,38 – 4y
BTNT O: nFeO + 6nFe(NO3)2 = nNO + nH2O
=> x + 6y = 0,02 + 0,38 – 4y => x + 10y = 0,4