Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Fe + H2SO4 → FeSO4 + H2↑
nH2SO4 = 0,1 mol; nH2SO4 dư = 0,01 mol
=> nH2SO4 phản ứng đem dùng = 0,11 mol
=> VH2SO4 đem dùng = 0,11/2 = 0,055 lít
nFeSO4 = 0,1 mol => Nồng độ mol FeSO4 = 0,1/0,055 = 1,8M

mddCuSO4 = 1,12 x 100 = 112 (g)
mCuSO4 = 10% x 112 = 11,2 (g)
=> nCuSO4 = 11,2 / 160 = 0,07 (mol)
nFe = 1,96 / 56 = 0,035 (mol)
PTHH : Fe + CuSO4 -----> FeSO4 + Cu
Lập tỉ lệ : \(\frac{nFe\left(\text{đề}\right)}{n\left(pt\right)}=\frac{0,035}{1}< \frac{nCuSO_4\left(\text{đề}\right)}{nCuSO_4\left(pt\right)}=\frac{0,07}{1}\)
Vậy CuSO4 dư 0,07 - 0,035 = 0,035 (mol)
=> mCuSO4 (dư) = 0,035 x 160 = 5,6 (g)
b/ Từ pthh suy ra nFeSO4 = 0,035 (mol)
Vì thể tích dung dịch thay đổi không đáng kể nên :
CM = \(\frac{0,035}{0,1}=0,35\left(M\right)\)

a) 500ml = 0,5l
\(n_{NaOH}=\dfrac{12}{40}=0,3\left(mol\right)\)
\(C_{M_{ddNaOH}}=\dfrac{0,3}{0,5}=0,6\left(M\right)\)
b) \(2NaOH+H_2SO_4\rightarrow Na_2SO_4+2H_2O|\)
2 1 1 2
0,3 0,15
\(n_{H2SO4}=\dfrac{0,3.1}{2}=0,15\left(mol\right)\)
\(m_{H2SO4}=0,15.98=14,7\left(g\right)\)
\(m_{ddH2SO4}=\dfrac{14,7.100}{10}=147\left(g\right)\)
Chúc bạn học tốt

Gọi số mol của BaO, BaCO3, NaHCO3 trong 30,19g hh lần lượt là x, y, z
Có 153x + 197y + 84z = 30,19
Phần 1:
BaO + H2O → Ba(OH)2
x x
OH- + HCO3- → CO32- + H2O
Ba2+ + CO32- → BaCO3
n kết tủa = 0,11
Phần 2:
BaCO3 →BaO + CO2
y y
2NaHCO3 → Na2CO3 + H2O + CO2
z z/2 z/2
=> mCO2 + mH2O = 30,19 – 26,13 = 4,06
=> 44 (y + z/2) + 18 . z/2= 4,06
TH1: Ba tạo kết tủa hoàn toàn thành BaCO3 và NaHCO3 dư
=> nBaCO3 = nBaCO3 + nBaO = 0,11 => Không thỏa mãn
TH2: Ba(OH)2 dư và NaHCO3 hết
=> x + y = 0,11 và y + z = 0,11
=> x = 0,1; y = 0,05 và z = 0,06
a.
hh Y gồm BaO: 0,15 mol; Na2CO3: 0,03 mol
BaO + H2O → Ba(OH)2
0,15 0,15
Ba(OH)2 + Na2CO3 → BaCO3 + 2NaOH
0,15 0,03 0,03 0,06
=> m kết tủa = 0,03 . 197 = 5,91g
m dd = m chất rắn + mH2O – mBaCO3 = 26,13 + 79,78 – 5,91 = 100
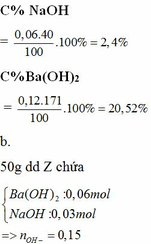
nAl2(SO4)3 = 0,02 => nAl3+ = 0,04; nSO42- = 0,06
Ba2+ + SO42- → BaSO4
0,06 0,06 0,06
nAl(OH)3 = 0,01 => mAl(OH)3 = 0,78g
m = 0,78 + 0,06 . 233 = 14,76g

a, Hiện tượng: có kết tủa trắng.
\(n_{KCl}=0,4\cdot2=0,8\left(mol\right);n_{AgNO_3}=2\cdot0,1=0,2\left(mol\right)\\ PTHH:KCl+AgNO_3\rightarrow KNO_3+AgCl\downarrow\\ ....0,2....0,2.....0,2....0,2\left(mol\right)\)
Vì \(\dfrac{n_{KCl}}{1}>\dfrac{n_{AgNO_3}}{1}\) nên sau phản ứng KCl dư, tính theo AgNO3
\(\Rightarrow m_{AgCl}=0,2\cdot143,5=28,7\left(g\right)\)
\(b,V_{dd\left(sau.p/ứ\right)}=V_{KNO_3}=V_{KCl}+V_{AgNO_3}=0,4+0,1=0,5\left(l\right)\\ \Rightarrow C_{M_{KNO_3}}=\dfrac{0,2}{0,5}=0,4M\)

Ta có: \(n_{Na_2O}=\dfrac{3,1}{62}=0,05\left(mol\right)\)
PTHH: Na2O + H2O ---> 2NaOH (1)
a. Theo PT(1): \(n_{NaOH}=2.n_{Na_2O}=2.0,05=0,1\left(mol\right)\)
=> \(C_{M_{NaOH}}=\dfrac{0,1}{2}=0,05M\)
b. PTHH: 2NaOH + H2SO4 ---> Na2SO4 + 2H2O
Theo PT: \(n_{H_2SO_4}=\dfrac{1}{2}.n_{NaOH}=\dfrac{1}{2}.0,1=0,05\left(mol\right)\)
=> \(m_{H_2SO_4}=0,05.98=4,9\left(g\right)\)
Ta có: \(C_{\%_{H_2SO_4}}=\dfrac{4,9}{m_{dd_{H_2SO_4}}}.100\%=20\%\)
=> \(m_{dd_{H_2SO_4}}=24,5\left(g\right)\)