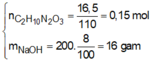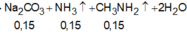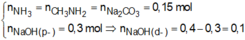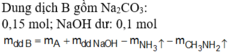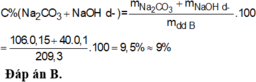Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
+ C 2 H 10 O 3 N 2 ( A ) + N a O H → k h í C . Suy ra A là muối amoni.
+ Trong A có 3O nên gốc axit cảu A là N O 3 - hoặc C O 3 2 - hoặc H C O 3 - .
- Nếu gốc axit N O 3 - thì gốc amoni là C 2 H 10 N + (loại).
- Nếu gốc axit là H C O 3 - thì gốc amoni là C H 9 N 2 + (loại).
- Nếu gốc axit là C O 3 2 - thì 2 gốc amoni là C H 3 N H 3 + v à C H 3 N H 3 + ( t h ỏ a m ã n ) .
+ Vậy A là C H 3 N H 3 C O 3 H 4 N .
+ Phương trình phản ứng:
C H 3 N H 3 C O 3 H 4 N + 2 N a O H → C H 3 N H 2 ↑ + N H 3 ↑ + N a 2 C O 3 m o l : 0 , 15 → 0 , 3 → 0 , 15 → 0 , 15 → 0 , 15
+ Dung dịch sau phản ứng chứa:
N a 2 C O 3 : 0 , 15 m o l ; N a O H d ư : 0 , 1 m o l C % ( N a 2 C O 3 , N a O H ) t r o n g B = 0 , 15 . 106 + 0 , 1 . 40 16 , 5 + 200 - 0 , 15 ( 17 + 31 ) = 9 , 5 % g ầ n n h ấ...

MgCO3 + 2HCl → MgCl2 + CO2 + H2O (1)
BaCO3 + 2HCl → BaCl2 + CO2 + H2O (2)
CO2 + Ca(OH)2 → CaCO3↓ + H2O. (3)
Theo (1), (2) và (3), để lượng kết tủa B thu được là lớn nhất thì:
nCO2 = nMgCO3 + nBaCO3 = 0,2 mol
Ta có:  = 0,2
= 0,2
=> a = 29,89.

Bạn chú ý, gửi từng câu hỏi một, không nên gửi nhiều câu hỏi một lúc
Câu 1.
Bài này có thể gọi M là kim loại chung của 3 kim loại trên:
M + HNO3 ---> M(NO3)n + NO + N2O + H2O (chú ý với bài tính toán kiểu này ko cần cân bằng pt).
Ta có số mol HNO3 = 1,5.0,95 = 1,425 mol.
Ta có khối lượng của hh khí (NO và N2O) = 16,4.2.số mol = 16,4.2.0,25 = 8,2 gam.
Áp dụng ĐLBTKL ta có: 29 + 63.1,425 = m + 8,2 + 18.0,7125 (chú ý số mol H2O luôn bằng 1/2 số mol HNO3).
Tính ra m = 97,75 g

-\(n_{Fe}=\frac{11,2}{56}=0,2mol\) \(n_{Al}=\frac{m}{27}mol\) |
-khi thêm \(Fe\) vào cốc đựng \(HCl\) ( cốc A ) có phản ứng: \(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\) 0,2 0,2 |
theo định luật bảo toàn khối lượng, khối lượng cốc \(HCl\) tăng thêm: \(11,2-\left(0,2.2\right)=10,8g\) |
khi thêm \(Al\) vào cốc đựng dd \(H_2SO_4\) có phản ứng: \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\uparrow\) \(\frac{m}{27}mol\) \(\rightarrow\) \(\frac{3.m}{27.2}mol\) |
| khi cho \(m\) gam \(Al\) vào cốc B, cốc B tăng thêm : \(m-\frac{3.m}{27.2}mol\) |
để cân thăng bằng, khối lượng ở cốc đựng \(H_2SO_4\) cũng phải tăng thêm 10,8g.Có: \(m-\frac{3.m}{27.2}.2=10,8\)
|
| giải ra được \(m=\) \(\left(g\right)\) |

C2H2 + 2AgNO3 + 2NH3 → C2Ag2 ↓ + 2NH4NO3
CH3CHO + 2AgNO3 + 3NH3 + H2O → CH3COONH4 + 2Ag ↓ + 2NH4NO3
C2Ag2 + 2HCl → 2AgCl ↓ + C2H2 ↑
Y(AgCl, Ag) + HNO3 --> ...
Ag + 2HNO3 → AgNO3 + NO2 ↑ + H2O