Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,2___ 0,4_____0,2_____0,2
\(n_{Zn}=\frac{13}{65}=0,2\left(mol\right)\)
\(n_{HCl}=\frac{300.7,3}{10.36,5}=0,6\left(mol\right)\)
Lập tỉ lệ hết với dư:
\(\frac{0,2}{1}< \frac{0,6}{2}\)
Vậy Zn hết, HCl dư
\(a,V_{H2}=0,2.22,4=4,48\left(l\right)\)
b, Dd A: ZnCl2
\(m_{Dd}=300-\left(0,2.2\right)=299,6\left(g\right)\)
\(m_{ZnCl2}=0,2.136=27,2\left(g\right)\)
\(\rightarrow C\%_{ZnCl2}=\frac{27,2}{299,6}=9,08\%\)

\(a)n_{H_2}=\dfrac{2,24}{22,4}=0,1mol\\
Fe+2HCl\rightarrow FeCl_2+H_2\)
0,1 0,2 0,1 0,1
\(n_{Fe_2O_3}=\dfrac{21,6-56.0,1}{160}=0,1mol\\
Fe_2O_3+6HCl\rightarrow2FeCl_3+3H_2\)
0,1 0,6 0,2 0,3
\(V_{ddHCl}=\dfrac{0,2+0,6}{1}=0,8l\\
b.C_{M_{FeCl_2}}=\dfrac{0,1}{0,8}=0,125M\\
C_{M_{FeCl_3}}=\dfrac{0,2}{0,8}=0,25M\)

a)\(Fe+2HCl-->FeCl2+H2\)
\(n_{H2}=\frac{6,72}{22,4}=0,3\left(mol\right)\)
\(n_{Fe}=n_{H2}=0,3\left(mol\right)\)
\(m=m_{Fe}=0,3.56=16,8\left(g\right)\)
b)\(n_{HCl}=2n_{H2}=0,6\left(mol\right)\)
\(V_{HCl}=\frac{0,6}{2}=0,3\left(l\right)\)
c)\(n_{FeCl2}=n_{H2}=0,3\left(mol\right)\)
\(C_{M\left(FeCl2\right)}=\frac{0,3}{0,3}=1\left(M\right)\)

\(n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\)
Pt : \(Mg+2HCl\rightarrow MgCl_2+H_2|\)
1 2 1 1
0,2 0,4 0,2 0,2
a) \(n_{H2}=\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
\(V_{H2\left(dktc\right)}=0,2.22,4=4,48\left(l\right)\)
Câu b : hình như đề bị sai bạn xem lại giúp mình
c) \(n_{MgCl2}=\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
⇒ \(m_{MgCl2}=0,2.95=19\left(g\right)\)
Chúc bạn học tốt

a) Theo đề bài ta có : nAl = \(\dfrac{24,3}{27}=0,9\left(mol\right)\)
PTHH :
\(2Al+6HCl->2AlCl3+3H2\)
0,9mol...2,7mol....0,9mol.......1,35mol
b) VH2(đktc) = 1,35.22,4 = 30,24(l)
c) mddHCl = \(\dfrac{2,7.36,5.100}{14,6}=675\left(g\right)\)
d) Ta có :
mdd(sau) = 24,3 + 675 - 1,35.2 = 696,6(g)
=> C%ddAlCl3 = \(\dfrac{0,9.133,5}{696,6}.100\approx17,25\%\)
2Al+6HCl\(\rightarrow\)2AlCl3+3H2
n Al=24,3:27=0,9mol theo pt nH2=3/2nAl=1,35 mol
suy ra vH2=1,35*22,4=30,24l
theo pt nHCl=3nAl=2,7 mol suy ra mHCL=98,55 G
\(\Rightarrow\)mdd HCl=675 ml
mdd sau pứ=24,3+675-2,7=696,6 ml
ta có mAlCl3==,9*133,5=120,15
suy ra c%AlCl3=17,2%

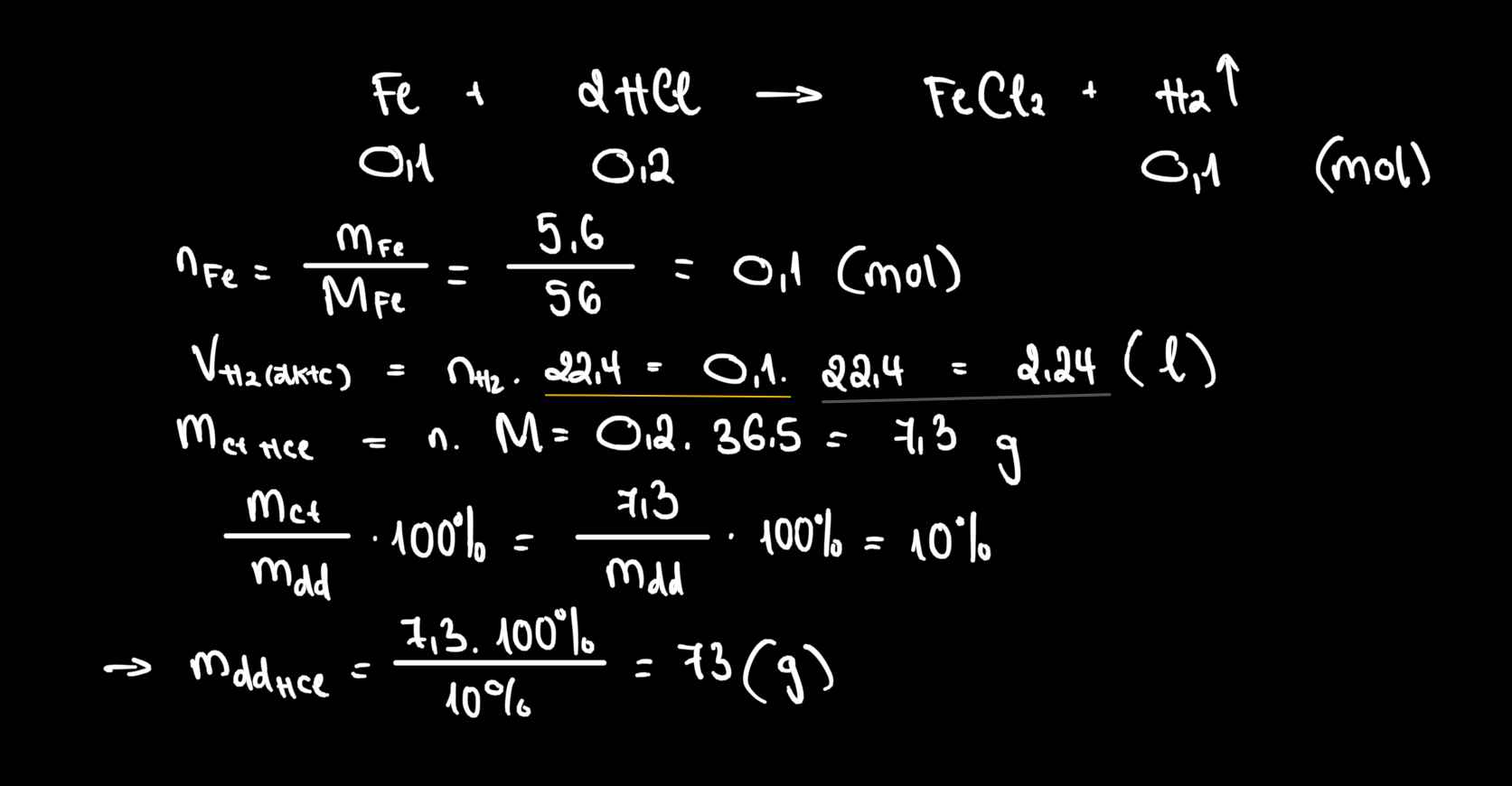
Fe+2HCl------>FeCl2+H2
a) n Fe=11,2/56=0,2(mol)
m HCl=182,5.10/100=18,25(g)
n HCl=18,25/36,5=0,5(mol)
Lập tỉ lệ
n Fe=0,2/1=0,2(mol)
n HCl=0,5/2=0,25(mol)
-->HCl dư
Theo pthh
n H2=n Fe=0,2(mol)
V H2=0,2.22,4=4,48(l)
b) m dd sau pư=11,2+182,5-0,4=193,3(g)
dd sau pư gồm HCl dư và FeCl2
m HCl dư=0,1.36,5=3,65(g)
C% HCl dư=3,65/193,3.100%=1,89%
m FeCl2=0,2.127=25,4(g)
C% FeCl2=25,4/193,3.100%=13,14%
Chúc bạn học tốt
\(PTHH:Fe+2HCl\rightarrow FeCl_2+H_2\)
Ban đầu : 0,2 ___0,5 ___________________
Phản ứng :0,2 ____0,4 ____0,2_____0,2
Sau phứng : 0 ___0,1____________________
Ta có : \(n_{Fe}=\frac{11,2}{56}=0,2\left(mol\right)\)
\(m_{HCl}=182,5.10\%=18,25\left(g\right)\)
\(\rightarrow n_{HCl}=\frac{18,25}{36,5}=0,5\left(mol\right)\)
\(\rightarrow V_{H2}=0,2.22,4=4,48\left(l\right)\)
\(\rightarrow C\%_{FeCl2}=\left[\frac{0,2.\left(56+71\right)}{182,5+11,2-0,2.2}\right]=13,14\%\)