Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) \(n_{CuO}=\dfrac{2,4}{80}=0,03\left(mol\right)\)
\(m_{H_2SO_4}=100.29,4\%=29,4\left(g\right)\Rightarrow n_{H_2SO_4}=\dfrac{29,4}{98}=0,3\left(mol\right)\)
PTHH: CuO + H2SO4 → CuSO4 + H2O
Mol: 0,03 0,03 0,03
Ta có: \(\dfrac{0,03}{1}< \dfrac{0,3}{1}\) ⇒ CuO hết, H2SO4 dư
b) \(m_{H_2SO_4}=0,03.98=2,94\left(g\right)\)
c) mdd sau pứ = 2,4+100 = 102,4 (g)
\(C\%_{ddCuSO_4}=\dfrac{0,03.160.100\%}{102,4}=4,6875\%\)
\(C\%_{ddH_2SO_4dư}=\dfrac{\left(0,3-0,03\right).98.100\%}{102,4}=25,84\%\)
Bài 4 :
\(n_{CuO}=\dfrac{2,4}{80}=0,03\left(mol\right)\)
\(m_{ct}=\dfrac{29,4.100}{100}=29,4\left(g\right)\)
\(n_{H2SO4}=\dfrac{29,4}{98}=0,3\left(mol\right)\)
a) Pt : \(CuO+H_2SO_4\rightarrow CuSO_4+H_2O|\)
1 1 1 1
0,03 0,3 0,03
Câu khối lượng của dng dịch H2SO4 đề cho rồi nên mình làm câu c thôi nhé
c) Lập tỉ số so sánh : \(\dfrac{0,03}{1}< \dfrac{0,3}{1}\)
⇒ CuO phản ứng hết , H2SO4 dư
⇒ Tính toán dựa vào số mol của CuO
\(n_{CuSO4}=\dfrac{0,03.1}{1}=0,03\left(mol\right)\)
⇒ \(m_{CuSO4}=0,03.160=4,8\left(g\right)\)
\(n_{H2SO4\left(dư\right)}=0,3-0,03=0,27\left(mol\right)\)
⇒ \(m_{H2SO4\left(dư\right)}=0,27.98=26,46\left(g\right)\)
\(m_{ddspu}=2,4+100=102,4\left(g\right)\)
\(C_{CuSO4}=\dfrac{4,8.100}{102,4}=4,6875\)0/0
\(C_{H2SO4\left(dư\right)}=\dfrac{26,46.100}{102,4}=25,84\)0/0
Chúc bạn học tốt

\(a,PTHH:H_2SO_4+BaCl_2\rightarrow BaSO_4\downarrow+2HCl\\ \left\{{}\begin{matrix}m_{H_2SO_4}=\dfrac{300\cdot9,8\%}{100\%}=29,4\left(g\right)\\m_{BaCl_2}=\dfrac{200\cdot26\%}{100\%}=52\left(g\right)\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}n_{H_2SO_4}=\dfrac{29,4}{98}=0,3\left(mol\right)\\n_{BaCl_2}=\dfrac{52}{208}=0,25\left(mol\right)\end{matrix}\right.\)
Vì \(\dfrac{n_{H_2SO_4}}{1}>\dfrac{n_{BaCl_2}}{1}\) nên H2SO4 dư
\(\Rightarrow n_{BaSO_4}=n_{BaCl_2}=0,25\left(mol\right)\\ \Rightarrow a=m_{BaSO_4}=0,25\cdot233=58,25\left(g\right)\\ b,n_{HCl}=n_{BaCl_2}=0,25\left(mol\right)\\ \Rightarrow m_{CT_{HCl}}=0,25\cdot36,5=9,125\left(g\right)\\ m_{dd_{HCl}}=300+200-58,25=441,75\left(g\right)\\ \Rightarrow C\%_{HCl}=\dfrac{9,125}{441,75}\cdot100\%\approx2,07\%\)

a) Vì: mA < 400 (g) nên phải có khí thoát ra → muối có dạng MHSO4 và khí là: CO2
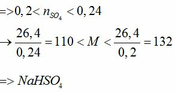
b)
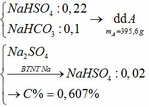
c) Tác dụng được với: MgCO3, Ba(HSO3)2, Al2O3, Fe(OH)2, Fe, Fe(NO3)2
Pt: 2NaHSO4 + MgCO3 → Na2SO4 + MgSO4 + CO2↑ + H2O
2NaHSO4 + Ba(HSO3)2 → BaSO4 + Na2SO4 + SO2↑ + 2H2O
6NaHSO4 + Al2O3 → 3Na2SO4 + Al2(SO4)3 + 3H2O
2NaHSO4 + Fe(OH)2 → Na2SO4 + FeSO4 + 2H2O
2NaHSO4 + Fe → Na2SO4 + FeSO4 + H2↑
12NaHSO4 + 9Fe(NO3)2 → 5Fe(NO3)3 + 2Fe2(SO4)3 + 6Na2SO4 + 3NO↑ + 6H2O

a, PT: \(Mg+H_2SO_4\rightarrow MgSO_4+H_2\)
\(Fe_2O_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3H_2O\)
b, Ta có: \(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
Theo PT: \(n_{Mg}=n_{H_2}=0,1\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Mg}=\dfrac{0,1.24}{34,4}.100\%\approx6,98\%\\\%m_{Fe_2O_3}\approx93,02\%\end{matrix}\right.\)
c, Ta có: \(m_{Fe_2O_3}=34,4-0,1.24=32\left(g\right)\Rightarrow n_{Fe_2O_3}=\dfrac{32}{160}=0,2\left(mol\right)\)
Theo PT: \(\left\{{}\begin{matrix}n_{MgSO_4}=n_{Mg}=0,1\left(mol\right)\\n_{Fe_2\left(SO_4\right)_3}=n_{Fe_2O_3}=0,2\left(mol\right)\end{matrix}\right.\)\(n_{H_2SO_4}=n_{Mg}+3n_{Fe_2O_3}=0,7\left(mol\right)\Rightarrow m_{H_2SO_4}=0,7.98=68,6\left(g\right)\)
\(\Rightarrow m_{ddH_2SO_4}=\dfrac{68,6}{10\%}=686\left(g\right)\)
Ta có: m dd sau pư = 34,4 + 686 - 0,1.2 = 720,2 (g)
\(\Rightarrow\left\{{}\begin{matrix}C\%_{MgSO_4}=\dfrac{0,1.120}{720,2}.100\%\approx1,67\%\\C\%_{Fe_2\left(SO_4\right)_3}=\dfrac{0,2.400}{720,2}.100\%\approx11,11\%\end{matrix}\right.\)
Bạn tham khảo nhé!

a. Các phản ứng có thể xảy ra :
P2O5 + 3H2O -> 2H3PO4
KOH + H3PO4 -> KH2PO4 + H2O
2KOH + H3PO4 -> K2HPO4 + 2H2O
3KOH + H3PO4 -> K3PO4 + 3H2O
b.Gọi nP2O5 = x mol
=> nH3PO4(X) = 0,01+ 2x (mol)
, nKOH = 0,1 mol
+) TH1 : Nếu KOH dư => chất rắn gồm : (0,01 + 2x) mol K3PO4 ; (0,07 – 6x) mol KOH
=> 6,48 = 212(0,01 + 2x) + 56(0,07 – 6x) => x = 0,005 mol => m = 0,71g
=> 6,48g X gồm : 4,24g K3PO4 và 2,24g KOH
+) TH2 : Nếu chất rắn gồm : (0,08 – 2x) mol K3PO4 ; (4x – 0,07) mol K2HPO4
, mK3PO4 < 6,48g => 0,08 – 2x < 0,03 => x > 0,025
=> 6,48 = 212(0,08 - 2x) + 174(4x – 0,07) => x = 0,00625 mol (L)
+) TH3 : Nếu chất rắn gồm : (0,09 - 2x) mol K2HPO4 ; (4x – 0,08) mol KH2PO4
,mK2HPO4 < 6,48g => 0,09 – 2x < 0,037 => x > 0,043
=> 6,48 = 174(0,09 - 2x) + 136(4x – 0,08) => x = 0,0086 mol (L)
+) TH4 : Nếu H3PO4 dư => nKH2PO4 = 0,1 mol => mKH2PO4 = 13,6g > 6,48g (L)

\(a)CuO+H_2SO_4\rightarrow CuSO_4+H_2O\\ b)n_{CuO}=\dfrac{4}{80}=0,05mol\\ n_{H_2SO_4}=\dfrac{100.20}{100.98}=\dfrac{10}{49}mol\\ \Rightarrow\dfrac{0,05}{1}< \dfrac{10:49}{1}\rightarrow H_2SO_4.dư\\ n_{CuSO_4}=n_{H_2SO_4}=n_{CuO}=0,05mol\\ C_{\%CuSO_4}=\dfrac{0,05.160}{100+4}\cdot100=7,69\%\\ C_{\%H_2SO_4}=\dfrac{\left(10:49-0,05\right)98}{100+4}\cdot100=14,52\%\)
\(n_{Al_2O_3}=\dfrac{10,2}{102}=0,1\left(mol\right)\\ m_{H_2SO_{\text{ 4}}}=\dfrac{100.9,8}{100}=9,8g\\ n_{H_2SO_4}=\dfrac{9,8}{98}=0,1\left(mol\right)\\ pthh:Al_2O_3+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2O\)
0,1 0,1
\(m_{\text{dd}}=10,2+100-\left(0,3.18\right)=104,8g\\ C\%=\dfrac{0,1.342}{104,8}.100\%=32,633\%\)
\(a,n_{Al_2O_3}=\dfrac{10,2}{102}=0,1\left(mol\right)\\ m_{H_2SO_4}=9,8\%.100=9,8\left(g\right)\\ \rightarrow n_{H_2SO_4}=\dfrac{9,8}{98}=0,1\left(mol\right)\)
PTHH: \(Al_2O_3+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2O\)
Ban đầu: 0,1 0,1
Phản ứng: \(\dfrac{1}{30}\) 0,1
Sau pư: \(\dfrac{1}{15}\) 0 \(\dfrac{1}{30}\) 0,1
b, \(\rightarrow m_{dd}=\dfrac{1}{30}.102+100=103,4\left(g\right)\)
\(\rightarrow C\%_{Al_2\left(SO_4\right)_3}=\dfrac{\dfrac{1}{30}.342}{101,6}.100\%=11,22\%\)