Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

2)
a. Gọi công thức chung (tổng quát) của cả hai kim loại là X.
PTHH: \(X+H_2O\rightarrow XOH+\dfrac{1}{2}H_2\)
1 (mol) .................................. 0.5 (mol)
Theo đề: \(n_{H_2}=\dfrac{3.36}{22.4}=0.15\left(mol\right)\)
Theo phương trình có: \(n_X=2n_{H_2}=2.0.15=0.3\left(mol\right)\)
\(\Rightarrow M_X=\dfrac{5.6}{0.3}=18.667\)
Vậy một kim loại phải là Liti (7 đvC) và Na (23 đvC).
b. \(\Rightarrow\)Dung dịch A có 0.3 (mol) XOH. (vì nX = nXOH = 2nH2 ).
PTHH: \(2XOH+H_2SO_4\rightarrow X_2SO_4+2H_2O\)
0.3 (mol) .... 0.15(mol)
Theo phương trình ta được: \(n_{H_2SO_4}=0.15\left(mol\right)\)
\(\Rightarrow V_{H_2SO_4}=\dfrac{0.15}{2}=0.075\left(l\right)\)
1)
a. Vì R thuộc nhóm VIIA nên công thức oxit cao nhất của R có dạng:
R2O7.
R chiếm 47.02% về khối lượng \(\Leftrightarrow\dfrac{2R}{2R+16.7}.100=47.02\Leftrightarrow R=50\left(đvC\right)\)
\(\Rightarrow\) R là thiếc (Sn) nhưng thiếc thuộc chu kì VIA cơ?????????
ĐỀ SAI!!!!!

4Na + O2 ------------> 2Na2O ( cần nhiệt độ )
2. Na2O + H2SO4 ------> Na2SO4 + H2O
3. Na2O + H2O -----> 2NaOH
4. Na2O + H2CO3 ------> Na2CO3 + H2O
5. 2NaOH + H2SO4 ---> Na2SO4 + 2H2O
6. Na2SO4 + Ba(OH)2 ----> BaSO4 + 2NaOH
7. Na2CO3 + Ca(OH)2 ----> 2NaOH + CaCO3
8. 2NaOH + H2CO3 ----> Na2CO3 +2H2O
9. NaOH + HCl ---> NaCl +H2O
10. Na2CO3 + BaCl2 -----> 2NaCl + BaCO3
11. Na2SO4 + BaCl2------> 2NaCl + BaSO4
bổ sung phương trình 12. từ NaCl thành Na2SO4 :
2NaCl + Ag2SO4 ---> Na2SO4 + 2AgCl

Tham khảo:
Số khối trung bình của Cl = ( 35.75 +37.25) :100 = 35,5
Gọi a là số khối trung bình của Cu
=> %Cu = a : ( a + 35,5 . 2 ) = 47,228%
=> a = 63,54
Đồng vị 63 Cu chiếm 73 % --> Đồng vị còn lại có số khối x chiếm 27%
--> ( 63.73 + x.27 ) : 100 = 63,54
--> x = 65
Vậy đồng vị còn lại là 65 Cu
+) Tính \(\overline{A_{Cl}}=\frac{35,75+37,25}{100}\)
+) Tính \(\%M_{Cu}=\frac{a}{a+35,5.2}.100\)
+) Đồng vị 63Cu chiếm 73%
=> đồng vị còn lại có số khối là x chiếm 27%

Bài 1:
Gọi x là số khối của đồng vị thứ 2, ta có:
\(\frac{107.56\%+x44\%}{100\%}=107,88\)
\(\Rightarrow x=109\)
Vậy số khối của đồng vị thứ 2 là 109
Nếu có 500 nguyên tử Ag thì số nguyên tử của đồng vị thứ 2 là: \(\frac{44\%.500}{100\%}=220\) (nguyên tử)
\(M_{Ag^{ }_2O}=\left(107,88.2\right)+16=231,76\)
\(\Rightarrow n=\frac{57,94}{231,76}=0,25\left(mol\right)\)
Xét trong 1 mol Ag2O có \(\begin{cases}2molAg\\1molO\end{cases}\)
\(\Rightarrow\) trong 0,25 mol Ag2O có 0,5 mol Ag
\(\Rightarrow\) trong 0,5 mol Ag có \(\frac{56\%.0,5}{100\%}=0.28\left(mol\right)\) đồng vị 107Ag
\(\Rightarrow m_{^{107}Ag}\) = 107 . 0,28 = 29,96 (gam)
Bài 2:
a) Gọi x, y lần lượt là % về số nguyên tử của 2 đồng vị 35Cl và 37Cl, ta có:
\(\begin{cases}x+y=100\\\frac{35x+37y}{100}=35,5\end{cases}\)\(\Leftrightarrow\)\(\begin{cases}x=75\\y=25\end{cases}\)
Vậy đồng vị 35Cl chiếm 75%; đồng vị 37Cl chiếm 25%
b) Tính % về gì vậy bạn?
c) \(M_{AlCl_3}\) = 27 + (35,5 .3) = 133,5
\(\Rightarrow n_{AlCl_3}\) = \(\frac{13,35}{133,5}=0,1\left(mol\right)\)
Xét trong 1 mol AlCl3 có \(\begin{cases}1molAl\\3molCl\end{cases}\)
=> trong 0,1 mol AlCl3 có 0,3 mol Cl
=> trong 0,3 mol Cl có \(\frac{75\%.0,3}{100\%}=0,225\left(mol\right)\) đồng vị 35Cl
=> Số nguyên tử 35Cl có trong 13,35g AlCl3 là:
0,225 . 6,02 . 1023 = 1,3545.1023 (nguyên tử)
1)Cách 1: nhẩm nhanh cho các bài có Z nhỏ, Z lớn vẫn có thể áp dụng nếu bạn gần như đã thuộc bảng tuần hoàn-để có thể suy ra đáp án :d) lấy 10/3 xấp xỉ 3,333 => lấy số gần nhất là 3 tương đương với Z của Nguyên tử cần tìm => Li (giải thích: tổng 3 hạt là E,N,P trong đó E P bằng nhau(, N thì lớn hơn hoặc bằng P, nên muốn tìm Z (Z = E =P) thì chia 3 ra (3 hạt), lấy số đó hoặc phần nguyên nếu lẻ), Z nhỏ thì NP không khác nhau nhiều, còn Z lớn ví dụ (Fe Z=26, N=30, tổng số hạt là 82 chia 3 ra thì là 27,333...không còn đúng nữa.!
Cách 2: cách chính quy dùng cho Kt trên lớp, kiếm điểm:D:
3≤ (2Z+N)/Z < 3,5 (*)=> 2,8...<Z<3,33... => Z=3 (Li) cách này áp dụng cho mọi bài tập dạng này. để hiểu rõ hơn vì sao có công thức (*) bạn nghiên cứu thêm bài tập 1.19 trong sách bài tập hóa lớp 10 trang 6.
2)Mtb= 109*44%+X*(100-44)%=107,88 => X=107

1.
a) Gọi p là số proton của nguyên tố X
Đồng vị X1 có 3 loại hạt bằng nhau nên 3p = 18 suy ra p = 6
Đồng vị X2 có tổng số hạt 20 nên 2p + n’ = 20 suy ra n’ = 8
Số khối của các đồng vị X1, X2 lần lượt là 12, 14
Phần trăm hai đồng vị bằng nhau suy ra mỗi đồng vị chiếm 50%
Atb = (12.50 + 14.50) / 100 = 13 đvC
b)
Gọi số khối của hai đồng vị X, Y là A1 và A2; phần trăm số nguyên tử của hai đồng vị này là x1 và x2. Theo giả thiết ta có:
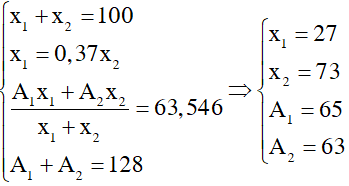
1
a , các loại hạt trong X1 bằng nhau <=> p=n1=e=6 (hạt) => A1 = 12
=> n2 = 20-6.12=8(hạt) => A2 = 8+6=14
%X1 = %X2 = 50%
\(\overline{\text{A}}=\frac{14.50+12.50}{100}=13\)
2 , gọi 2 đồng vị A1p Y và A2p Z , phần trăm của 2 đồng vị lần lượt la x1 , x2
Theo bài ra
A1 + A2 =128
x1 + x2 = 100
\(\overline{M}=\frac{A_1x_1+A_2x_2}{100}=\) 63,54
x1 - 0,37x2 = 0
=> A1 = 65 , A2 = 63

Nguyên tử khối trung bình:
\(79.54,5\%+A\left(100\%-54,5\%\right)=79,91\)
\(\Rightarrow A=81\)


a) R thuộc nhóm VIIA nên CT oxit cao nhất có dạng: R2O7
Ta có: \(\%m_R=47,02\%\Leftrightarrow\dfrac{2M_R}{2M_R+7M_O}\cdot100\%=47,02\%\\ \Leftrightarrow\dfrac{2M_R}{2M_R+112}=0,4702\\ \Leftrightarrow2M_R=0,9404M_R+52,6624\\ \Leftrightarrow1,0596M_R=52,6624\Leftrightarrow M_R=49,7\)
Vậy không có nguyên tố R nào thỏa mãn điều kiện đề bài.
BẠN XEM LẠI ĐỀ NHÁ! HIẾM KHI MÀ ĐỀ KHÔNG CÓ NGHIỆM ĐÂU!
b) Phải làm được phần (a)
R chiếm 38,7978% nha bạn
giả hộ mk vs