Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(d_{O_2/kk}=\dfrac{M_{O_2}}{M_{kk}}=\dfrac{32}{29}>1\)
Vậy khí oxi nặng hơn không khí
\(d_{H_2/kk}=\dfrac{M_{H_2}}{M_{kk}}=\dfrac{2}{29}< 1\)
vậy khí hidro nhẹ hơn không khí
\(d_{CO_2/kk}=\dfrac{M_{CO_2}}{M_{kk}}=\dfrac{44}{29}>1\)
Vậy khí `CO_2` nặng hơn không khí

- Có 1 cặp toàn đơn chất: Nhóm a
- Có 1 cặp toàn hợp chất: Nhóm f
- Có 4 cặp gồm 1 đơn chất và 1 hợp chất:
+ Nhóm b có đơn chất Nitơ N2 và hợp chất là khí Cacbonic CO2.
+ Nhóm c có đơn chất Oxi O2 và hợp chất là khí Cacbonic CO2.
+ Nhóm d có đơn chất Oxi O2 và hợp chất là hơi nước H2O(hơi).
+ Nhóm e có đơn chất Nitơ N2 và hợp chất là hơi nước H2O(hơi).

C
\(d_{CO_2/H_2}=\dfrac{44}{2}=22\)
=> Khí CO2 nặng gấp 22 lần khí H2

1) \(C+O_2\rightarrow CO_2\\
C+CO_2\rightarrow2CO\)
2)
\(pthh:C+O_2\rightarrow CO_2\)
=> số mol bằng nhau
\(n_{O_2}=\dfrac{6,4}{16}=0,4\left(mol\right)\)
áp vào pt trên ta có : nCO2 = 0,4 (mol)
=> \(m_{CO_2}=0,4.44=17,6\left(g\right)\)
=> dCO2/H2 = 44/2 = 22
dCO2/H2 = 44/2 = 22

\(M_{O_2}=32\left(đvC\right)\)
a) \(M_{CO_2}=44\left(đvC\right)\)
O2 nhẹ hơn CO2 và bằng \(\dfrac{32}{44}=0,73\) lần CO2
b) \(M_{SO_2}=64\left(đvC\right)\)
O2 nhẹ hơn SO2 và bằng \(\dfrac{32}{64}=0,5\) lần SO2
c) \(M_{NH_3}=17\left(đvC\right)\)
O2 nặng hơn NH3 và bằng \(\dfrac{32}{17}=1,88\) lần NH3

a)
\(C + O_2 \xrightarrow{t^o} CO_2\\ n_{CO_2} = n_{O_2} = \dfrac{6,4}{32} = 0,2(mol)\\ \Rightarrow m_{CO_2} = 0,2.44 = 8,8(gam)\)
b)
\(n_C = \dfrac{6}{12} = 0,5(mol)\\ n_{O_2} =\dfrac{19,2}{32} = 0,6(mol)\\ C + O_2 \xrightarrow{t^o} CO_2\)
\(n_C = 0,5 < n_{O_2} = 0,6 \Rightarrow\) Oxi dư.
\(n_{CO_2} = n_C = 0,5(mol)\\ \Rightarrow m_{CO_2} = 0,5.44 = 22(gam)\)

Thành phần theo khối lượng:
Thành phần phần trăm theo thể tích:

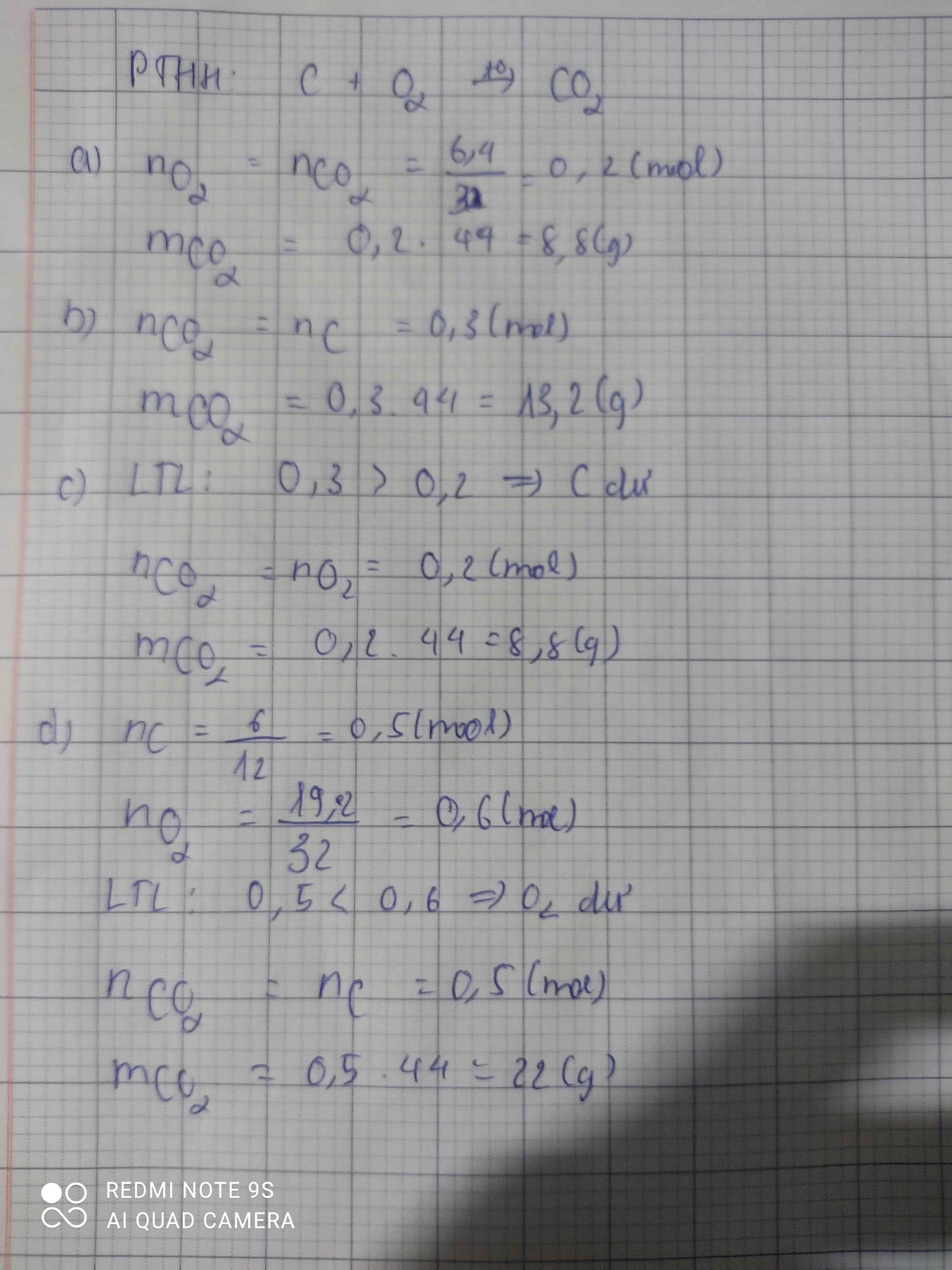
C
C