Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Sách giáo khoaa cần cải cách vấn đề này, chứ dạy học sinh theo sách mà đáp án lại ra theo thí nghiệm thì căn cứ ở đâu mà chấm? Hồi đó tỉnh em cũng bị cái này :v trong sgk bảo màu vàng :v nhưng thi ra lại là màu nâu đất :v mọi người đều nói là lấy sgk làm căn cứ :))) nhưng người ra đề lấy thực tế và học sinh đều bị trừ câu đó 0,25 đ (trừ mấy người làm sai ^_^). 0,25 đ :))) đủ khiến một vài ai đó rớt tốt nghiệp cấp II và tuyển sinh lớp 10 :v
nói tóm tác vấn đề của cô giáo đã nói :
| muối tạo bởi | bazơ mạnh | bazơ yếu |
| axit mạnh | không đổi màu quì tím | đổi màu quì tím sang màu đỏ |
| axit yếu | đổi màu quì tím sang màu xanh | trường hợp này thì chưa chắc được và độ pH của nó gần bằng 7 |

TRẢ LỜI:
CO - Cacbon monoxit
CO2 - Cacbon đioxit
HNO3 - Axit nitric
Cl2O - Điclo monoxit
B2H6 - Điboran
PH3 - Photphin
PH5 - Photphoran
C6H12 - Xiclohexan
CO : cacbon oxit
\(CO_2\): cacbon đioxit
\(HNO_3\): axit nitric
\(Cl_2O\): điclo monooxxit
\(B_2H_6\): điboran
\(PH_3\): photphin
\(PH_5\): ??? làm g có
\(C_6H_{12}\): xiclohexan

bài 1:
- Trích mỗi chất 1 ít làm mẫu thử
- Nhỏ vài giọt các dd trên vào mẫu giấy quỳ tím
+ quỳ tím chuyển sang xanh : Ba(OH)2 , NaOH (I)
+ Không có hiện tượng gì : NaCl , Na2SO4 (II)
- Trích từng chất dd ở nhóm I vào nhóm II , thấy xuất hiện kết tủa trắng thì đó là Ba(OH)2 và Na2SO4
Ba(OH)2 + Na2SO4 → BaSO4↓ + 2NaOH
- Hai dd còn lại là NaCl(không làm quỳ tím đổi màu)
Và NaOH ( quỳ làm tím hóa xanh )

Câu 1 :
\(a.CH_4+Cl_2\underrightarrow{as,1:1}CH_3Cl+HCl\)
\(b.C_2H_4+H_2O\underrightarrow{^{H^+,t^0}}C_2H_5OH\)
\(c.CaC_2+2H_2O\rightarrow Ca\left(OH\right)_2+C_2H_2\)
\(d.C_2H_5OH+Na\rightarrow C_2H_5ONa+\dfrac{1}{2}H_2\)
\(e.CH_3COOH+NaOH\rightarrow CH_3COONa+H_2O\)
\(f.\left(RCOO\right)_3C_3H_5+3NaOH\rightarrow3RCOONa+C_3H_5\left(OH\right)_3\)
Câu 2 :
a) CTCT C2H2 và C2H6 :
\(CH\equiv CH\)
\(CH_3-CH_3\)
b) Nhận biết CH4, C2H4 :
Sục lần lượt các khí qua dung dịch Br2 dư :
- Mất màu : C2H4
- Không HT : CH4
\(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
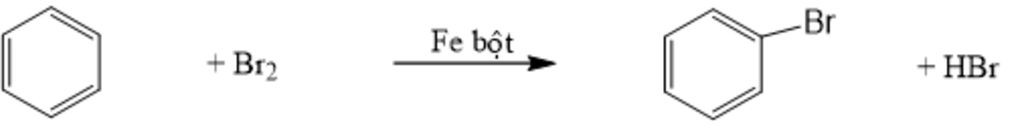
c)
TN1 : Mất màu nâu đỏ Br2 và có khí HBr thoát ra.
 TN2 :
TN2 :
Dầu ăn không tan trong nước , nổi trên bề mặt
Câu 3 :
\(n_{CH_4}=a\left(mol\right),n_{C_2H_6}=b\left(mol\right)\)
\(n_X=\dfrac{4.48}{22.4}=0.2\left(mol\right)\)
\(\Rightarrow a+b=0.2\left(1\right)\)
\(n_{CaCO_3}=\dfrac{30}{100}=0.3\left(mol\right)\)
\(CH_4+2O_2\underrightarrow{^{t^0}}CO_2+2H_2O\)
\(C_2H_6+\dfrac{7}{2}O_2\underrightarrow{^{t^0}}2CO_2+3H_2O\)
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\)
\(..............0.3......0.3\)
\(n_{CO_2}=a+2b=0.3\left(mol\right)\left(2\right)\)
\(\left(1\right),\left(2\right):a=b=0.1\)
\(\%V_{CH_4}=\%V_{C_2H_6}=\dfrac{0.1}{0.2}\cdot100\%=50\%\)
Câu 4 :
\(\text{ Trong 100 ml cồn 70 độ có 70 ml rượu etylic và 30 ml nước.}\)
\(V_{C_2H_5OH}=\dfrac{70}{100}\cdot50=35\left(ml\right)\)
\(n_{C_2H_5OH}=\dfrac{9.2}{46}=0.2\left(mol\right)\)
\(n_{CH_3COOH}=\dfrac{6}{60}=0.1\left(mol\right)\)
\(CH_3COOH+C_2H_5OH\underrightarrow{H^+,t^0}CH_3COOC_2H_5+H_2O\)
\(0.1.........................0.1....................0.1\)
\(H\%=\dfrac{5.28}{0.1\cdot88}\cdot100\%=60\%\)

Cho một lượng dư muối Na2CO3 vào 200ml dd H2SO4 thấy thoát ra 1 chất khí, cho toàn bộ khí đó hấp thụ hoàn toàn vào 98g dd KOH 40%. Sau phản ứng làm bay hơi dung dịch thì thu được 57.6g hóa học 2 muối khan.
a, Tính khối lượng mỗi muối thu được
b. Xác định nồng độ mol của dung dịch H2SO4
___________________________________________________________________________
Na2CO3 + H2SO4 --> Na2SO4 + H2O + CO2
__a________a_________a______a_____a_
CO2 + 2KOH --> K2CO3 + H2O
_x_____2x_______x______x_
CO2 + KOH --> KHCO3
_y_____y_______y_
mKOH = 98 * 40 / 100 = 39.2 (g)
nKOH = 39.2 / 56 = 0.7 (mol)
=> 2x + y = 0.7 (1)
mmuốikhan = 138x + 100y = 57.6 (2)
giải (1) và (2) ta được
x = 0.2
y = 0.3
mà x + y = a => a = 0.5
a)
mNa2SO4 = 0.5 * 142 = 71 (g)
mK2CO3 = 0.2 * 138 = 27.6 (g)
mKHCO3 = 0.3 * 100 = 30 (g)
b)
CMddH2SO4 = 0.5 / 0.2 = 2.5 (M)
thánh chép mạng đã xuất hiện, muốn biết chi tiết câu trả lời vào: @https://diendan.hocmai.vn/threads/hoa-9-muoi-axit-bazo.274750/

CaCO3 + 2HCl -> CaCl2 + H2O + CO2
Hok
tốt!!!!!!!!!!!!!!

a. Đặt CTTQ của kim loại là R
\(R+H_2SO_4\rightarrow RSO_4+H_2\)
b. \(n_{H_2}=\frac{22,4}{22,4}=1mol\)
\(n_R=\frac{65}{R}mol\)
Từ phương trình \(n_R=n_{H_2}\)
\(\rightarrow1=\frac{65}{R}\)
\(\rightarrow R=65\)
\(\rightarrow R:Zn\)
c. Từ phương trình \(n_{H_2SO_4}=n_{H_2}=1mol\)
\(m_{H_2SO_4}=1.98=98g\)
\(m_{ddH_2SO_4}=\frac{98}{35\%}=280g\)

3. CuO +H2SO4 -->CuSO4 +H2O
nCuO=64/80=0,8(mol)
theo PTHH :nCuO =nH2SO4=nCuSO4=0,8(mol)
=>mddH2SO4 20%=0,8.98.100/20=392(g)
mCuSO4=0,8.160=128(g)
mdd sau phản ứng =64 +392=456(g)
mH2O=456 -128=328(g)
giả sử có a g CuSO4.5H2O tách ra
trong 250g CuSO4 tách ra có 160g CuSO4 và 90g H2O tách ra
=> trong a g CuSO4.5H2O tách ra có : 160a/250 g CuSO4 và 90a/250 g H2O tách ra
=>mCuSO4(còn lại)=128 -160a/250 (g)
mH2O (còn lại)=328 -90a/250 (g)
=>\(\dfrac{128-\dfrac{160a}{250}}{328-\dfrac{90a}{250}}.100=25\)
=>a=83,63(g)

a) CO2 +Ba(OH)2---->BaCO3 +H2O
b)n CO2 =0,1
nCO2 = nBa(OH)2 =0,1
----->Cm =0,5M
c)nCO2 = nBa(OH)2 =0,1
--->mBa(OH)2 =17,1
a ) \(CO_2+Ba\left(OH\right)_2--->BaCO_3+H_2O\)
b ) \(n_{CO_2}=0,1\)
\(n_{CO_2}=n_{Ba}\left(OH\right)_2=0,1\)
\(--->Cm=0,5M\)
c ) \(n_{CO_2}=n_{Ba}\left(OH\right)_2=0,1\)
\(--->m_{Ba}\left(OH\right)_2=17,1\).

-lấy mỗi chất một ít làm mẫu thử , cho tác dụng với Ca phản ứng nào xuất hiện kết tủa thì chất ban đầu là BaCo3và Na2Co3(1),phản ứng nào không cho kết tủa thì chất ban đầu là MgCl2 , CaCl2 , NaCl(2)
BaCo3+Ca\(\rightarrow\)CaCo3\(\downarrow\) +Ba
Na2Co3+Ca\(\rightarrow\) CaCo3\(\downarrow\) +2Na
-cho nhóm (1) tác dụng với H2SO4 , phản ứng nào xuất hiên kết tủa thì chất ban đầu là BaCo3 , phản ứng nào không xuất hiện kết tủa thì chất ban đầu là Na2Co3
BaCo3+H2SO4 \(\rightarrow\) BaSO4\(\downarrow\) +H2O+CO2\(\uparrow\)
Na2CO3+H2SO4 \(\rightarrow\) Na2SO4+ H2O+CO2\(\uparrow\)
-cho nhóm (2) tác dụng với KOH , phản ứng nào xuất hiện kết tủa thì chất ban dầu là MgCl2 , phản ứng nào không thấy hiện tượng gì thì chất ban dầu là CaCl2 và NaCl (3) :
MgCl2+ 2KOH \(\rightarrow\) Mg(OH)2\(\downarrow\) + 2KCl
- cho nhóm (3) tác dụng với H2SO4,phản ứng nào xuát hiện kết tủa thì chất ban đầu là CaCl2 , phản ứng nào không thấy có hiện tượng gì thì chất ban đầu là NaCl
CaCl2+H2SO4\(\rightarrow\) CaSO4\(\downarrow\) + 2HCl
- Trích thành những mẫu thư nhỏ
- Cho các mẫu thử trên vào nước
+ Mẫu thử không tan trong nước là BaCO3
+ 3 mẫu thử tan dần ra trong nước là MgCl2, CaCl2 và Na2CO3
- Cho HCl lần lượt vào 3 mẫu thửu còn lại
+ Mẫu thử có bọt khí không màu xuất hiện là Na2CO3
Na2CO3+2HCl→2NaCl+CO2\(\uparrow\)+H2O
+ Hai mẫu thử không có hiện tượng gì là MgCl2 và CaCl2
- Cho dung dịch NaOH lần lượt vào hai mẫu thử còn lại
+ Mẫu thử xuất hiện kết tủa trắng trong dung dịch là MgCl2
MgCl2+2NaOH→2NaCl+Mg(OH)2↓
+ Mẫu thử không có hiện tượng gì là CaCl2

ok bn
2.
- Trích mẫu thử và đánh số thứ tự:
- Cho nước vào từng mẫu thử
+ Mẫu thử không tan trong nước CaCO3CaCO3
+ Mẫu thử tan trong nước: CaOCaO
PTHH: CaOCaO + H2OH2O → Ca(OH)2Ca(OH)2
3.
a, nCO2=2,2422,4=0,1(mol)nCO2=2,2422,4=0,1(mol)
PTHH: CO2 + 2KOH → K2CO3 + H2O
Mol: 0,1 0,2 0,1
b, CMddKOH=0,20,1=2MCMddKOH=0,20,1=2M
c, mK2CO3=0,1.138=13,8(g)
4.
Gọi CTHH của oxit là X2O3
X2O3 + 6HCl -> 2XCl3 + 3H2O
nHCl=0,24.1=0,24(mol)
Theo PTHH ta có:
1616nHCl=nX2O3=0,04(mol)
MX2O3=6,40,04=1606,40,04=160
=>MX=160−482=56
5.H2O + K2O -----> 2KOH
H2O + CO2 -----> H2CO3 (axit yếu nên vừa tạo ra bị phân hủy ngay thành CO2 và H2O)
2KOH + CO2 ------> K2CO3 + H2O ( nKOH/ nCO2 >=2)
KOH + CO2 ------> KHCO3 (nKOH/ nCO2 <= 1) </span>
K2O + CO2 ------> K2CO3